Clear Sky Science · zh
通过调节IGF-1R/PI3K/AKT信号通路抑制星形胶质细胞凋亡,IGF-2对视神经脊髓炎谱系障碍的治疗作用
在一种鲜为人知的自身免疫性疾病中保护大脑
视神经脊髓炎谱系障碍(NMOSD)是一种罕见但破坏性极强的自身免疫病,会攻击视神经和脊髓,常使患者出现失明、瘫痪或严重的认知问题。现有药物主要抑制免疫反应,价格昂贵,且不能直接保护脑细胞免受损伤。本研究探讨血液中一种与生长相关的天然分子IGF‑2能否在NMOSD中帮助保护脑细胞免受损害,并为该病提供一种新的治疗思路。
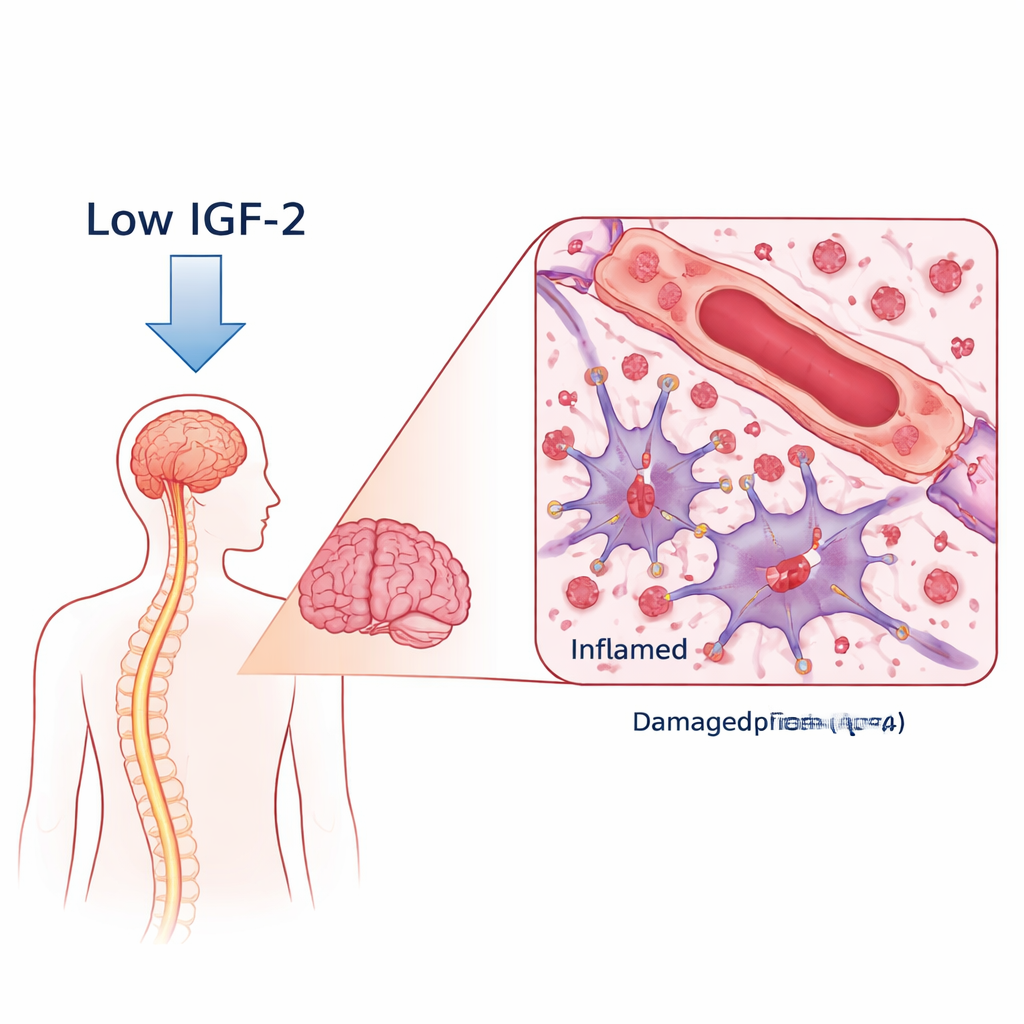
有害抗体与缺失的防护因子
在NMOSD中,体内产生针对一种名为AQP4的水通道蛋白的抗体,该蛋白位于大脑中被称为星形胶质细胞的放射状支持细胞表面。当这些抗体结合时,会触发免疫攻击,损伤星形胶质细胞、剥离神经髓鞘(神经的绝缘层),并可能伤害神经元。研究者将AQP4抗体阳性的NMOSD女性患者的血液与健康志愿者进行比较。通过广泛的蛋白质筛查,他们发现NMOSD患者的IGF‑2水平明显降低,而两种可捕获IGF‑2的结合蛋白水平升高。重要的是,IGF‑2最低的患者往往残疾更严重,在认知和记忆测试中得分更差,将该分子与疾病严重程度和认知健康联系起来。
标准治疗有助于IGF-2恢复
许多NMOSD患者接受利妥昔单抗治疗,这种药物可清除产生抗体的B细胞。研究团队在利妥昔单抗治疗前后测量了血液中的蛋白质。治疗后,IGF‑2水平上升,结合蛋白下降,趋向于健康人群的模式。这表明平抑免疫反应可能使机体恢复某些自身的保护因子。尽管利妥昔单抗并非专门针对IGF‑2,但IGF‑2的这种变化暗示它可能是机体恢复反应的一部分,监测IGF‑2或可用于追踪患者随访时的状况。
在小鼠疾病模型中测试IGF-2
为了验证IGF‑2是否不仅仅是疾病严重度的标志,科学家们转向小鼠模型。他们将人体AQP4抗体和人源补体注入小鼠大脑,复制出NMOSD的关键特征:星形胶质细胞上AQP4的丧失、炎症、髓鞘损伤以及四肢无力。另一组小鼠先接受一种无害病毒,使其脑细胞产生额外的IGF‑2。那些IGF‑2增强的小鼠体重下降较少,运动功能障碍更轻,并且在脑与脊髓组织中表现出较少的髓鞘丧失和炎症。标准的利妥昔单抗治疗也有帮助,但IGF‑2过表达似乎更直接保护脑组织,提示其主要发挥的是神经保护作用,而不仅仅是免疫抑制。
IGF-2如何抑制细胞死亡与炎症
研究组随后在体外培养的星形胶质细胞上暴露NMOSD抗体进行研究。通常,这些抗体会降低一种关键受体IGF‑1R的水平,并抑制下游的保护性通路PI3K/AKT,同时激活“自毁”蛋白和炎性信号。当研究者促使星形胶质细胞产生更多IGF‑2时,这条保护通路重新被激活,细胞死亡标志物下降,且细胞释放的炎性因子如IL‑1β、IL‑6和TNF‑α减少。阻断IGF‑1R受体会部分消除这些益处,表明IGF‑2主要通过激活星形胶质细胞内的IGF‑1R/PI3K/AKT通路来发挥作用。在活体小鼠中,增强IGF‑2还减少了小胶质细胞(大脑的免疫哨兵)的活化,并降低了血液中炎性信号的水平。
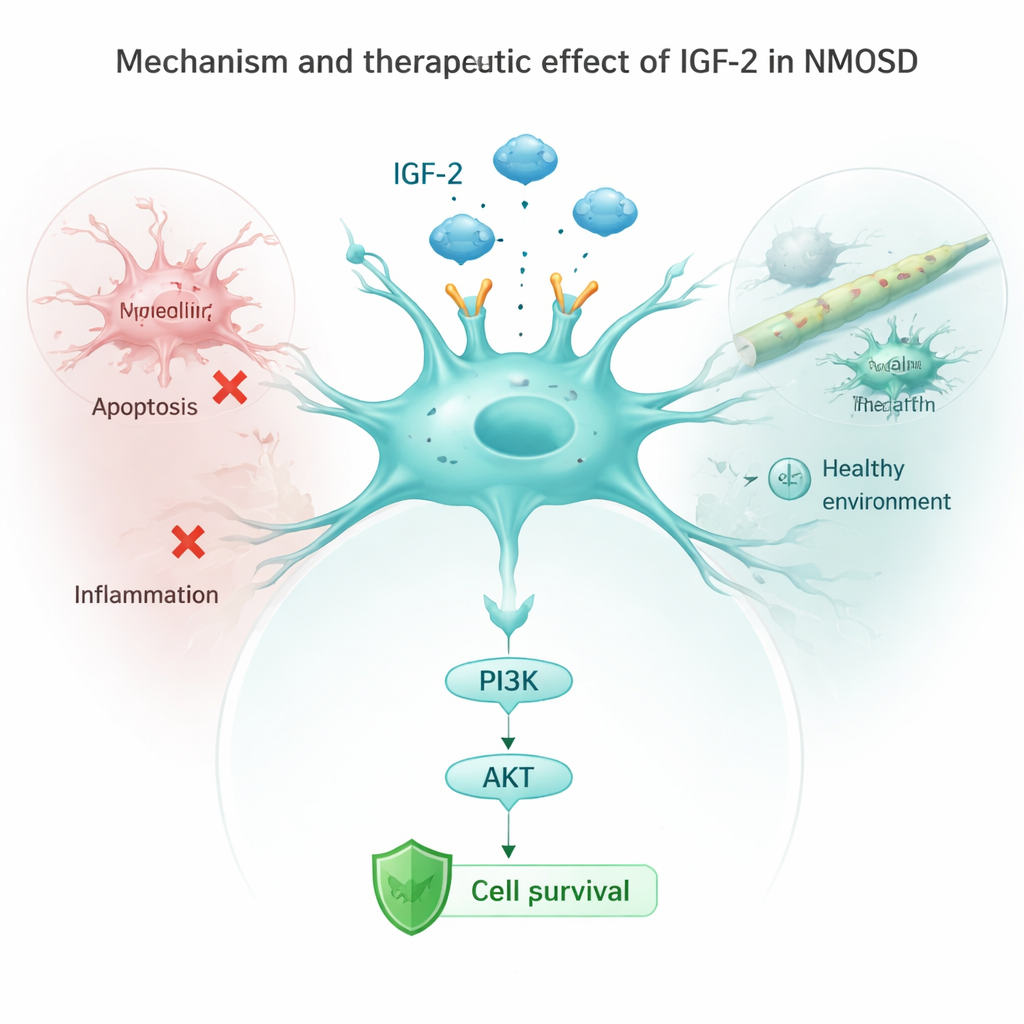
这对患者可能意味着什么
综合来看,这些发现表明低IGF‑2既是一个警示信号,也是NMOSD中被忽视的机会。IGF‑2含量较低的患者往往残疾更严重、认知能力下降,而在实验模型中恢复或增强IGF‑2有助于星形胶质细胞存活、减少脑部炎症并减轻神经损伤。尽管这项工作仍处于早期,且基于有限的患者数量和动物研究,但它把IGF‑2指向了一个有前景的治疗靶点,未来的治疗或可在抑制免疫攻击的同时直接保护脆弱的脑细胞。
引用: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
关键词: 视神经脊髓炎, 星形胶质细胞, IGF-2, 神经炎症, 神经保护