Clear Sky Science · zh
软珊瑚来源微生物的海洋天然产物对SARS-CoV-2主蛋白酶和刺突蛋白的分子对接与动力学模拟
来自海洋生命的隐秘帮助
即便疫苗已面世,导致COVID-19的病毒仍不断出现新变体,给治疗带来挑战并延长了大流行。本研究提出了一个出人意料但具有现实意义的问题:生活在软珊瑚中的微生物产生的化学化合物,能否帮助阻断冠状病毒,包括像德尔塔和奥密克戎这样的主要变体?研究人员采用基于计算的筛选方法,而非动物或患者实验,探讨这些海洋分子是否可能附着于关键病毒位点并减缓感染过程。
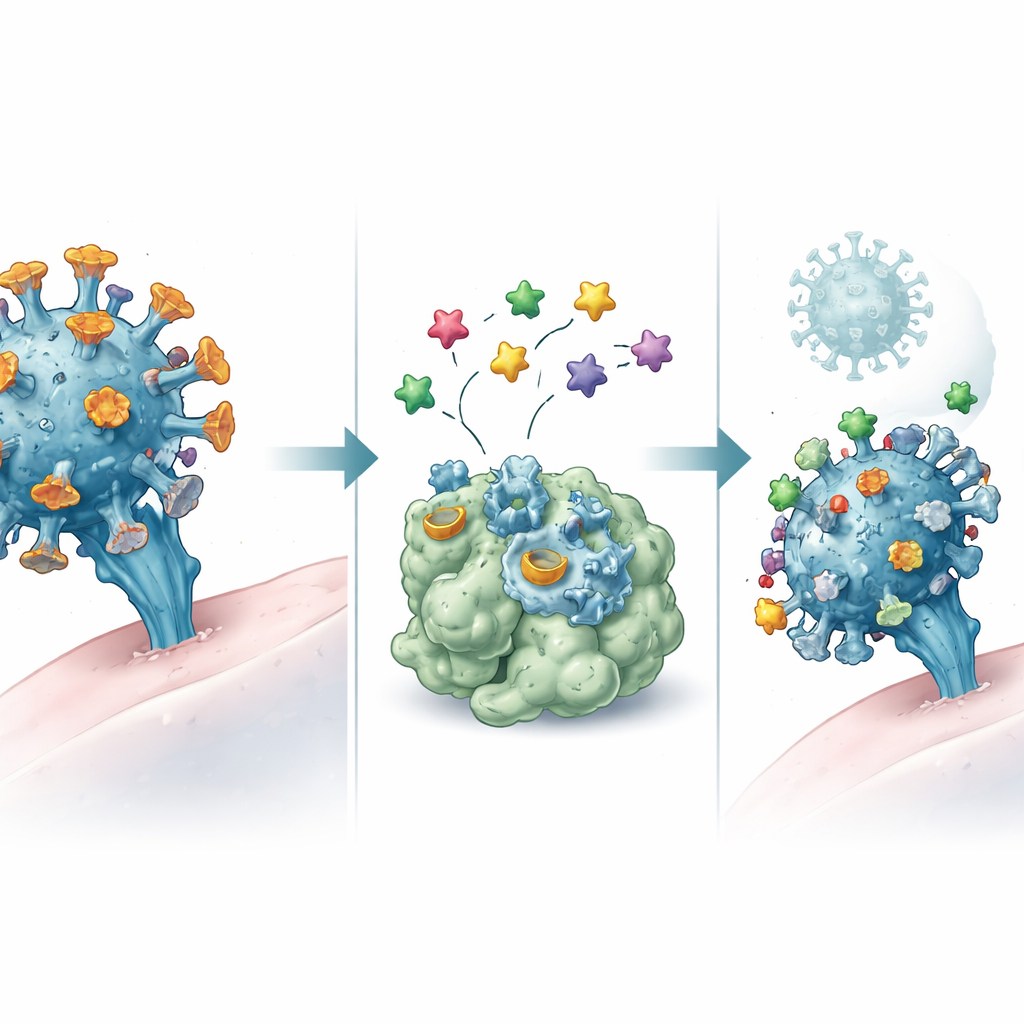
病毒如何入侵
引发COVID-19的病毒依赖两种主要工具侵入细胞并复制。其一是病毒表面的刺突蛋白,像一把钥匙匹配人细胞表面的锁,起始于称为受体结合域的区域。其二是主蛋白酶,这是病毒用来切割自身蛋白并组装新病毒颗粒的内部加工工具。值得关注的变体——Alpha、Beta、Gamma、Delta 和 Omicron——在刺突区带有小的变化,可能使病毒更易传播或绕过部分免疫反应,而蛋白酶则更为稳定。由于现有抗病毒药物并非对这些变体一律有效,刺突蛋白和主蛋白酶都是新疗法的主要靶点。
珊瑚礁中的寻宝
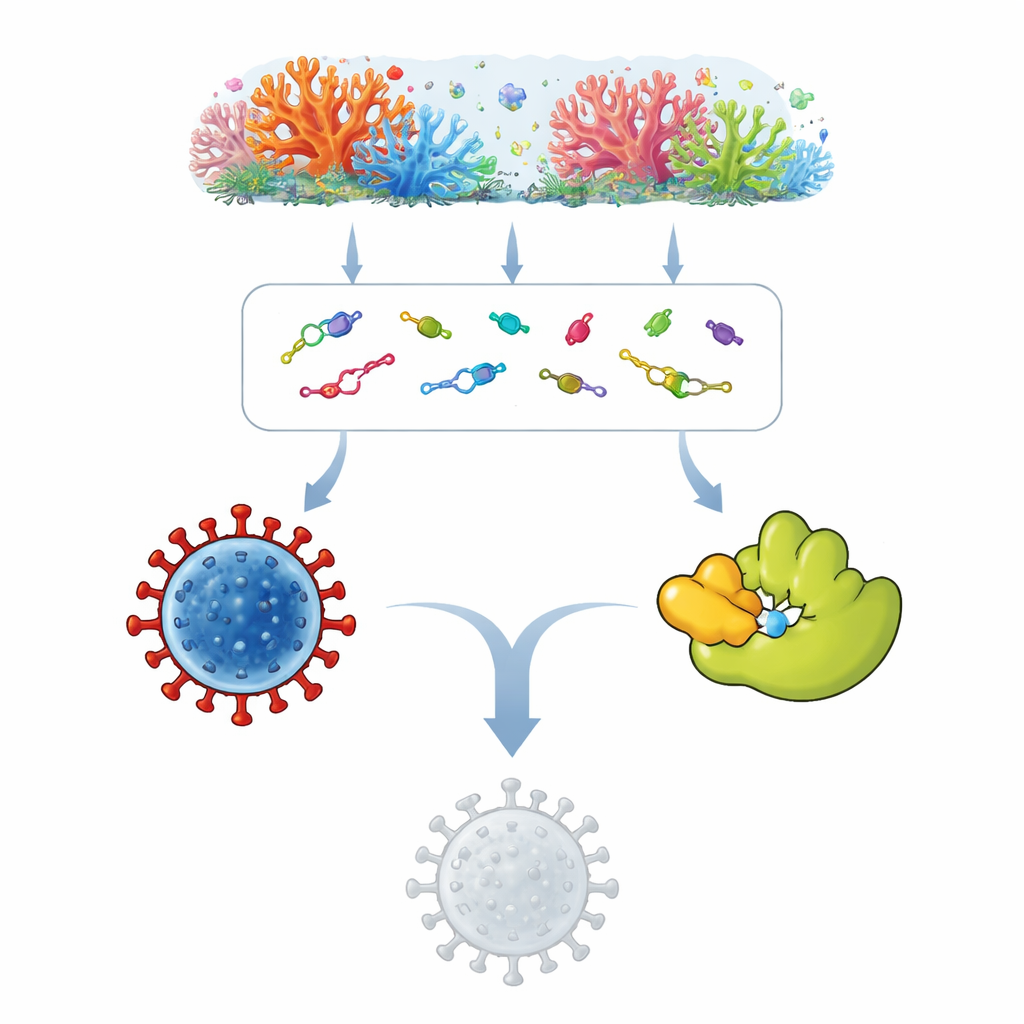
软珊瑚构成色彩斑斓的水下栖息地,寄居着丰富的微生物群落,如真菌和细菌。这些微小共生体会产生大量天然物质,作为其生存策略的一部分,其中一些已催生抗癌或抗微生物药物。研究团队收集了119种此类海洋天然产物的信息,并构建了它们的三维构象模型。接着他们使用分子对接技术——一种虚拟配对试验——评估哪些化合物能比已知抗病毒药物(如瑞德西韦或尼尔芬韦)与刺突蛋白和主蛋白酶形成更强的预测结合。
与病毒的虚拟配对
计算对接显示若干突出分子,包括 Cottoquinazoline B 和 D、Tetraorcinol A、Versicoloritide A 与 C、Fumiquinazoline K 以及 Pencillanthranin A。预测显示这些化合物能比对照药物更强地与原始病毒及多个变体的主蛋白酶和刺突区域结合。许多化合物在病毒参与细胞进入或复制的关键位点形成多重稳定相互作用,例如氢键和疏水相互作用。为了超越静态快照,研究人员进行了长时程分子动力学模拟,模拟这些蛋白—化合物复合体在水相环境中随时间的运动。若干顶级候选,尤其是 Cottoquinazoline B、Tetraorcinol A 和 Versicoloritide A,在数百纳秒的模拟中仍与其病毒靶点紧密结合,暗示为稳定附着而非短暂接触。
数字画板上的早期安全检查
研究还使用既定预测工具评估了基本的类药性特征。这些测试估算化合物是否可能被吸收、分布、代谢和排除,是否符合未来药物的要求,以及是否可能具有毒性。许多有前景的珊瑚来源分子符合口服药物的一些常见经验规则,并被标记为非致癌,尽管少数引发了潜在毒性或可能干扰实验检测的化学行为方面的担忧。总体而言,最有吸引力的候选者在对病毒蛋白的强预测结合与可接受的虚拟安全特征之间取得了平衡,使它们成为值得后续研究的重点。
这对未来治疗意味着什么
这项研究并不宣称发现了可立即使用的COVID-19药物,而是提供了一份经过精筛的海洋化合物清单,这些化合物在计算机模拟中表现出色:它们似乎能够粘附于病毒的刺突蛋白和主蛋白酶,包括主要变体,且许多通过了早期的类药性检测。下一步需要在真实世界中开展实验室试验和动物研究,以验证这些分子是否确实阻断感染并在生物体内安全。不管怎样,这项工作强调了像珊瑚礁这样常被忽视的生态系统可能蕴藏对快速变异病毒有价值的化学工具,以及计算方法如何迅速从大自然的“资料库”中筛选出有前景的线索,指导更聪明、更快速的药物发现。
引用: Anthikapalli, N.V.A., Patil, V.S., Alugoju, P. et al. Molecular docking and dynamic simulation of marine natural products from soft coral-derived microbes against SARS-CoV-2 main protease and spike protein. Sci Rep 16, 8252 (2026). https://doi.org/10.1038/s41598-026-37446-6
关键词: 海洋天然产物, 珊瑚礁微生物, SARS-CoV-2 刺突蛋白, 主蛋白酶抑制剂, COVID-19 药物发现