Clear Sky Science · zh
迟发性运动障碍精神分裂症患者尾状核中N-乙酰天冬氨酸及N-乙酰天冬氨酸-天冬氨酰胺酸水平降低
这对日常生活的重要性
迟发性运动障碍是长期使用抗精神病药物后常见且令人困扰的副作用,可能导致无法控制的面部鬼脸、舌头运动或四肢抽动。对患有精神分裂症的人及其家庭而言,这些不自主的动作会令人尴尬、致残且难以治疗。本研究提出了一个简单但重要的问题:迟发性运动障碍只是药物的副作用,还是反映了大脑运动回路中更深层、长期存在的变化?
聚焦一个看不见的运动枢纽
研究者将注意力集中在尾状核,这是位于脑深处的一个体积虽小但非常关键的结构,参与运动、动机和习惯形成的协调。先前的脑成像提示该区域在迟发性运动障碍患者中可能存在改变,但其化学成分尚未被精确测量。研究团队使用一种无创技术——质子磁共振波谱(可理解为内嵌在MRI扫描仪中的化学“探听器”)——在尾状核中测量了三组对象的关键脑化学物质:患有精神分裂症并合并迟发性运动障碍的患者、患有精神分裂症但无异常运动的患者,以及健康志愿者。
脑内化学信号揭示的内容
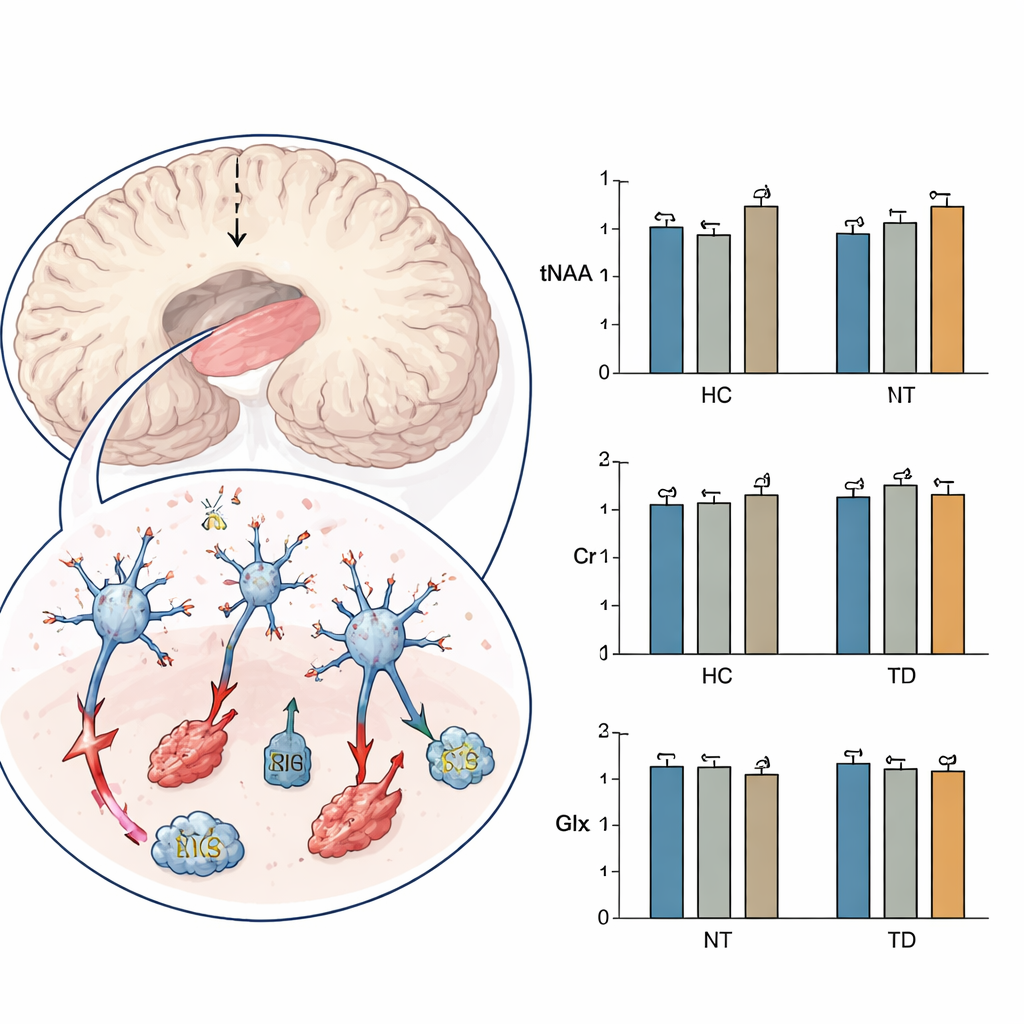
主要关注的化学标志物是总N-乙酰天冬氨酸(tNAA),它反映神经细胞的健康与能量状态。研究团队还测量了参与细胞能量供给的肌酸,以及代表兴奋性神经传递相关的谷氨酸/谷氨酰胺组合信号。总体来看,三组在年龄、性别、教育程度、症状严重性和抗精神病药剂量方面相似,但合并迟发性运动障碍的患者病程更长。将脑成像数据比较后,有一项信号尤为突出:与无异常运动的患者相比,迟发性运动障碍患者尾状核的tNAA水平显著降低,而肌酸和与谷氨酸相关的信号在各组间并无显著差异。
受压与易损神经细胞的迹象
tNAA降低提示尾状核内的神经细胞可能长期处于应激状态或有部分损伤。作者讨论了几种可能的成因:长期氧化应激(即大脑内的“锈蚀”过程)、线粒体负担(细胞内的能量工厂受损)、血流降低以及由谷氨酸等神经递质引起的过度兴奋。他们指出,在其他运动障碍(包括亨廷顿病和某些遗传性共济失调)中也观察到类似的tNAA下降,这些疾病中神经细胞缓慢退变。在本研究中,tNAA在迟发性运动障碍患者中最低、无运动患者次之、健康人相对较高——提示以尾状核为中心存在一条脆弱性梯度。
不仅仅是可见的动作
有趣的是,按标准量表测量的不自主运动严重程度并不与tNAA水平呈直接对应关系。换言之,动作更明显的人并不一定比症状较轻的人具有更低的tNAA。这表明tNAA降低并非日常评估运动严重性的即时指标,而更像是反映一种潜在脑状态的背景信号。作者提出,这种化学成分的改变可能代表一种长期、性状化的易感性,使得某些人在暴露于抗精神病药时更容易发生迟发性运动障碍,而不是单纯由当前症状强度所致。
对未来的意义
对患者、家庭和临床医生而言,这些发现强化了这样的观点:迟发性运动障碍不仅仅是不幸的药物副作用,可能与控制运动的脑回路中微妙且持久的改变有关。尾状核中较低的tNAA信号似乎标志着该区域神经细胞健康的下降,有助于解释为何一些人在调整药物后仍会出现持续的异常运动。尽管仍需更多长期和以治疗为导向的研究,但这项工作将该领域向发现生物学标志物的方向推进了一步,未来有望帮助早期识别高危患者、指导更安全的处方实践并激发旨在保护或修复易损神经细胞的新治疗方法。
引用: Yu, T., Li, Y., Li, N. et al. Decreased N-acetylaspartate plus N-acetyl-aspartyl-glutamate levels in the caudate of schizophrenia patients with tardive dyskinesia. Sci Rep 16, 6773 (2026). https://doi.org/10.1038/s41598-026-37396-z
关键词: 精神分裂症, 迟发性运动障碍, 脑成像, 运动障碍, 抗精神病药副作用