Clear Sky Science · zh
三维异源性胶质母细胞瘤模型揭示小神经胶质细胞对细胞组织结构和独特分泌组的影响
为什么培养皿里的微小脑肿瘤很重要
胶质母细胞瘤是最致命的脑癌之一,部分原因在于它对医生使用的几乎所有治疗手段都有高度抵抗性。这种失败的一个重要原因是常规实验室测试无法再现真实脑肿瘤的全部复杂性。本研究构建了更接近生理的三维“微型肿瘤”,不仅包含癌细胞,还包括小神经胶质细胞——脑内的常驻免疫细胞——以揭示这些“辅助者”如何悄然使肿瘤更强韧、更具侵袭性并更难被消灭。
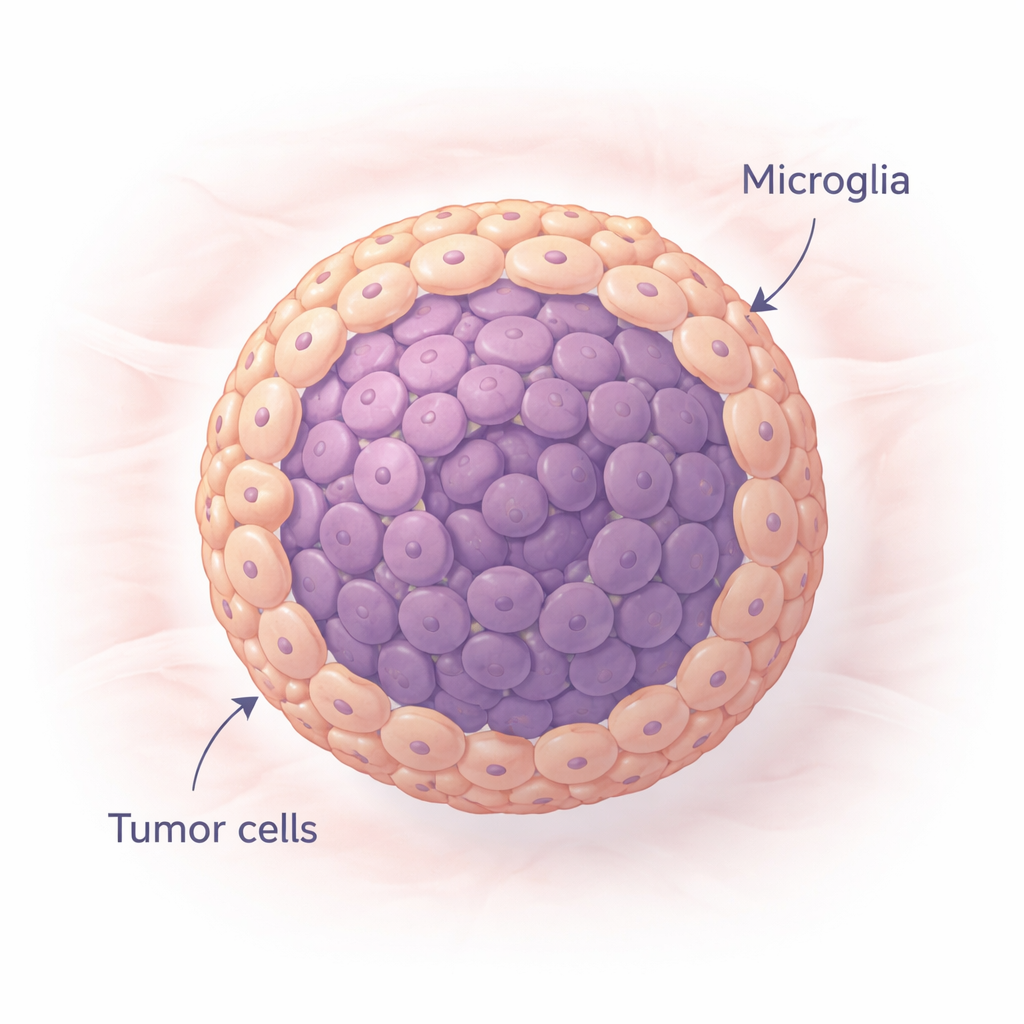
构建更像真实肿瘤的微型肿瘤
研究者构建了小型球状细胞群称为球体,使用的是常用的胶质母细胞瘤细胞系或来自患者的类干肿瘤细胞。有些球体仅由肿瘤细胞组成,另一些则按患者中观察到的比例将肿瘤细胞与小神经胶质细胞混合。在特殊的低附着培养皿中,这些细胞在一周内自然聚集成致密球体,并在很大程度上保持存活。通过比较“仅肿瘤”与“肿瘤+小神经胶质”球体,团队能够观察到这些脑内免疫细胞如何重塑生长、结构与行为。
小神经胶质细胞:生长助推器与入侵向导
加入小神经胶质细胞改变了微型肿瘤的特性。混合球体比仅肿瘤球体生长得更大、细胞密度更高,表明小神经胶质细胞助推了总体扩张。在患者来源的模型中,这些混合球体甚至形成多个致密中心,这是与侵袭性疾病相关的特征。当将球体置于模拟脑组织的软凝胶上时,来自混合球体的细胞更持久地扩散开来,尤其在某一肿瘤细胞系中更明显。追踪移动细胞显示小神经胶质细胞常在边缘带头,就像它们在真实胶质母细胞瘤周围聚集并帮助开辟进入邻近脑组织通路的方式一样。
钝化化疗作用的保护外壳
团队随后测试了标准药物替莫唑胺,这是一种广泛用于胶质母细胞瘤治疗的药物。仅肿瘤球体在药物暴露后失去了许多细胞,显示出显著损伤。相比之下,混合球体保留了更多细胞,在某些情况下在48小时后细胞数量甚至回升。高分辨率成像揭示了原因:在混合模型中,胶质瘤细胞集中在中心,而小神经胶质细胞形成了环绕的外壳。这种核心-外壳结构似乎像一个活体屏障,使药物更难到达并杀伤肿瘤核心。治疗前后对细胞类型的测量显示肿瘤细胞优先丧失,而小神经胶质细胞存活并相对增多,从而强化了这一保护效应。
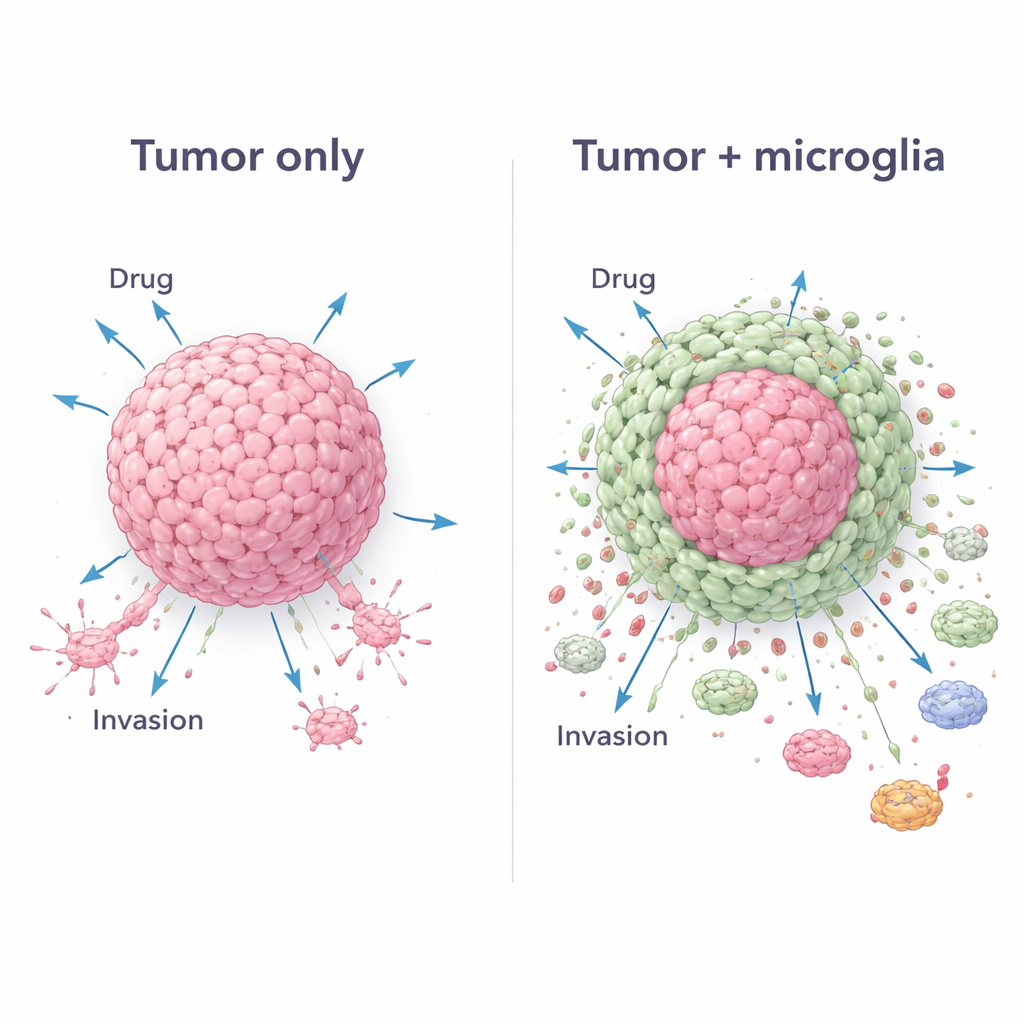
将机体防御重写为有利于肿瘤
胶质母细胞瘤还通过劫持免疫系统来存活。为探究此点,研究者将来自球体培养的培养上清液暴露给人类血源免疫细胞。来自混合肿瘤-小神经胶质球体的液体促使许多这些细胞定居并采用“M2样”状态——一种已知支持肿瘤生长而非攻击它的抗炎模式。在迁移实验中,更多循环免疫细胞朝向混合球体移动,而不是朝向仅肿瘤球体,表明存在更强的化学诱引。对分泌蛋白的广泛调查证实,混合球体释放出一组与侵袭、治疗耐受和免疫抑制相关的独特信号分子组合——当任一细胞类型单独培养时并不存在这种特征性分泌谱。
这对未来脑癌治疗意味着什么
对非专业读者来说,关键结论是:仅研究孤立的癌细胞不足以理解胶质母细胞瘤。这项工作表明,当肿瘤细胞与小神经胶质细胞在三维中共同生长时,它们会自组织成由小神经胶质细胞包裹的肿瘤核心,这种结构促进生长、助长扩散、削弱化疗并误导外来免疫细胞转而助纣为虐。这些更逼真的微型肿瘤捕捉了许多真实胶质母细胞瘤的特征,尤其是在使用患者来源的细胞时。因此,它们为设计不仅针对肿瘤细胞而且破坏肿瘤与小神经胶质细胞危险联盟的药物提供了强有力的试验平台,可能将更有效的疗法更快带到患者身边。
引用: García-Sáez, C., Alonso-Marañón, J., García-Puga, M. et al. 3D heterotypic models of glioblastoma reveal the impact of microglia on cellular organization and the production of a distinct secretome. Sci Rep 16, 7246 (2026). https://doi.org/10.1038/s41598-026-37395-0
关键词: 胶质母细胞瘤, 小神经胶质细胞, 三维肿瘤模型, 药物耐受性, 肿瘤微环境