Clear Sky Science · zh
GJB2 c.109G > A 突变激活 IFI27 介导的线粒体凋亡通路导致遗传性非综合征性听力损失
为什么微小的耳细胞关系到儿童的未来
出生时即存在的听力损失影响全球数百万儿童,常常决定他们如何学说话、在学校的表现以及与他人的交流方式。最常见的遗传元凶之一是名为 GJB2 的基因,但医生尚未完全弄清该基因的突变如何具体损害内耳。本研究利用斑马鱼和人类细胞追踪从 GJB2 单一 DNA 变异到脆弱的感音细胞死亡的事件链,并指出了一个新的分子 IFI27,作为未来治疗的潜在靶点。
一种导致儿童沉寂的常见基因变化
研究者首先筛查了中国福建省 1,199 名疑似遗传性听力损失儿童的血液样本。他们着重检测了数个已知的致聋基因,发现 GJB2 的改变占主导地位,覆盖了 85% 的检测到的突变。在这些突变中,称为 c.109G>A(也称 p.Val37Ile)的特定变体最为常见。该变体在普通人群中相对常见,但在听力受损人群中被强烈富集,表明它在非综合征性听力损失(即没有伴随其他医学问题的听力障碍)中发挥重要作用。
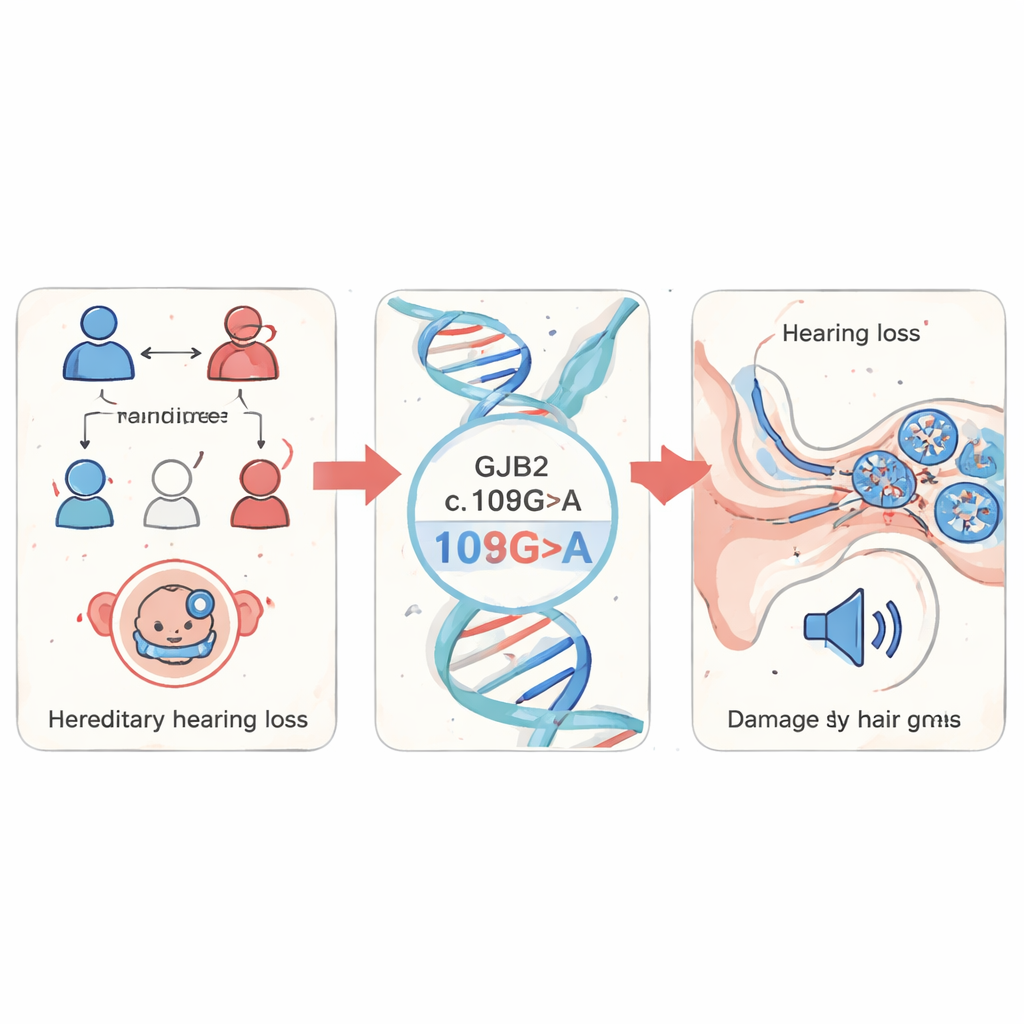
在透明小鱼体内追踪损伤
为了观察该突变在活体中的作用,团队转向斑马鱼——一种胚胎透明且与人类共享许多基因和耳部结构的小型淡水鱼。他们构建了表达正常人类 GJB2 或 c.109G>A 突变版本的斑马鱼胚胎,并采用“基因沉默”方法降低鱼自身 gjb2 基因的表达。携带突变或基因表达降低的胚胎表现出生长迟缓、尾部弯曲和心脏周围肿胀等发育异常迹象。更重要的是,它们的内耳明显异常:称为卵石(otolith)的关键结构更小且间距更远,充满液体的耳蜗区域体积减小。当科学家在携带突变的胚胎中同时补入正常 GJB2 时,许多结构性问题得到改善,表明突变本身在驱动这些缺陷。
从受损的耳朵到较差的听觉行为
由于听觉依赖将声波振动转化为神经信号的微小“毛细胞”,团队对斑马鱼的这些细胞进行了染色。携带 GJB2 突变或基因沉默的鱼在内耳和沿体表(斑马鱼也用于感知水流)毛细胞数量明显减少。研究者随后测试鱼对声音的反应能力。使用自动化追踪系统,他们测量了暴露于短促声刺激时 5 天龄幼鱼游动的距离和速度。正常及野生型 GJB2 的鱼会通过更远、更快的游动做出反应,而突变和基因沉默的鱼几乎没有行为变化,表明听力受损。同样,补入正常 GJB2 部分恢复了毛细胞数量和声音驱动的运动反应。
发生在细胞能量工厂内的一条致命通路
为了解细胞内部发生了什么,科学家使用 RNA 测序比较了正常斑马鱼与 gjb2 表达降低的斑马鱼间的基因活性。与“线粒体凋亡通路”相关的一组基因——以细胞能量工厂为中心的自毁路径——被强烈激活。特别是,IFI27 家族的若干成员尤为突出,以及已知的细胞死亡参与者如 Bax、细胞色素 c、Apaf1 和 caspase 等。随后在人体 HEK293 细胞中的实验证实了这一模式:携带突变 GJB2 的细胞产生更多活性氧(ROS,一种氧化应激形式)、从线粒体释放更多细胞色素 c,并启动凋亡蛋白,导致细胞死亡增加。当研究者在携带突变基因的细胞中沉默 IFI27 时,ROS 水平下降,死亡信号减弱,发生凋亡的细胞减少。
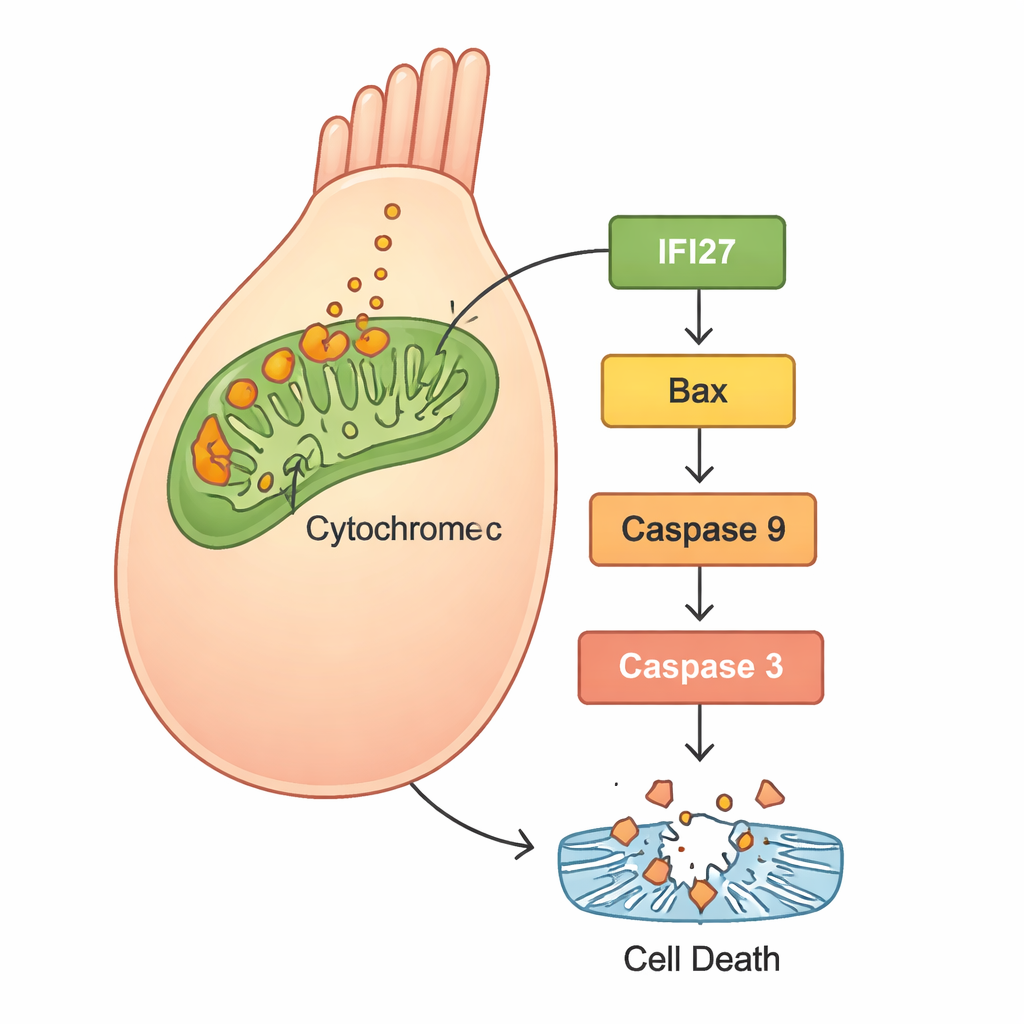
这对未来治疗意味着什么
综合来看,研究结果勾勒出一条清晰的故事线:GJB2 c.109G>A 突变不仅通过改变细胞间通讯破坏内耳的正常发育与功能,还通过触发线粒体内的应激反应加剧损害。这种应激上调 IFI27 及相关基因,促使细胞色素 c 释放并激活推动毛细胞走向程序性死亡的蛋白级联反应。由于人在耳内的毛细胞难以再生,其丧失导致永久性听力缺陷。研究表明在人体细胞中下调 IFI27 能减缓这一路径,强调 IFI27 作为药物或基因疗法潜在靶点的前景。尽管此类治疗仍遥远——且很可能需在生命早期就递送——但这项工作为将这一曾经神秘的基因突变转化为可预防的儿童耳聋原因提供了具体的分子路线图。
引用: Chen, Y., Zhao, P., Lin, Q. et al. GJB2 c.109G > A mutation activating IFI27-mediated mitochondrial apoptosis pathway leading to hereditary non-syndromic hearing loss. Sci Rep 16, 6240 (2026). https://doi.org/10.1038/s41598-026-37393-2
关键词: 遗传性听力损失, GJB2 突变, 斑马鱼模型, 线粒体凋亡, IFI27