Clear Sky Science · zh
通过整体与单细胞测序分析揭示的与氧化应激相关的基因 TPPP3 和 VEGFA 在慢性阻塞性肺病中的作用
这项肺部研究与你为何相关
慢性阻塞性肺病(COPD)会使呼吸多年逐步变得困难,目前是全球第三大死因。吸烟和空气污染是公认的罪魁祸首,但临床上仍缺乏精确工具来早期发现疾病或阻止肺内的持续性损伤。本研究利用大规模基因数据集、单细胞分析及实验室验证,揭示了若干与“氧化应激”相关的特定基因——即当有害氧代谢产物超过机体防御时产生的损伤——并展示了这些基因如何可能驱动 COPD 中的肺部瘢痕形成与重塑。
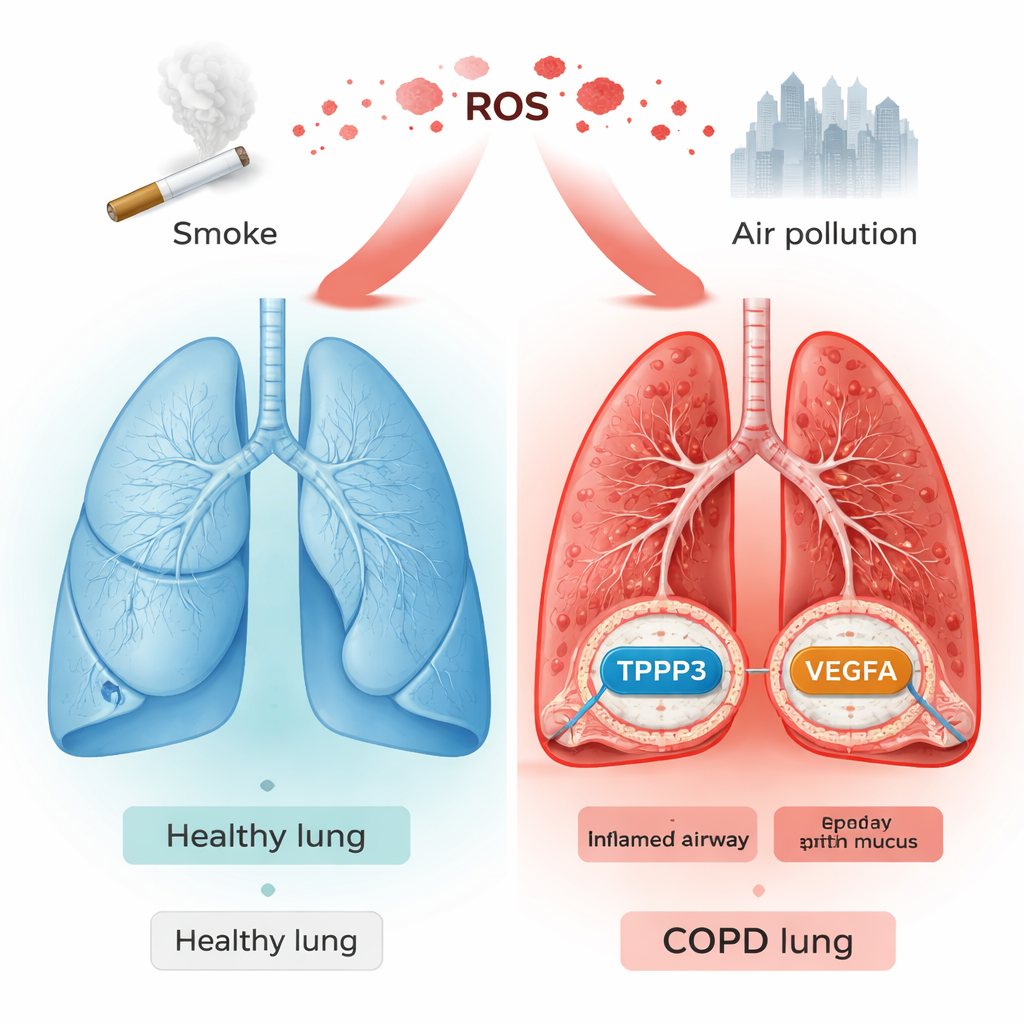
肺内的有害火花
每次呼吸不仅带入氧气,还会吸入颗粒与化学物质,尤其来自香烟烟雾的成分。这些物质可生成活性氧(ROS)——不稳定的分子,像微小火花一样损伤细胞并触发慢性炎症。在 COPD 中,这些“火花”似乎持续多年,逐渐导致气道变窄和气囊破坏。作者旨在找出哪些人类基因与 COPD 中的氧化应激最密切相关,希望确定能更早标记疾病的生物标志物以及未来药物可安全干预的靶点。
利用大数据挖掘高风险基因
研究团队首先收集了来自吸烟者(有 COPD 与无 COPD)的肺组织公开基因表达数据,聚焦已知与氧化应激相关的基因,比较这些基因在 COPD 肺组织中是上调还是下调。借助类似现代图像识别中使用的先进统计与机器学习工具,他们从数千个候选基因中筛选出 76 个在 COPD 患者与对照间差异显著的氧化应激相关基因。在此基础上,两种独立算法进一步交汇出一组核心 12 个“枢纽”基因,这些基因最能区分病变肺与健康肺,表明它们位于 COPD 分子网络的重要节点。
逐细胞观察气道内部
传统组织样本将多种细胞混合,但肺由多种特化细胞组成的马赛克构成。为确定枢纽基因在何处发挥作用,研究者转向单细胞 RNA 测序数据,读取单个细胞的基因活性。他们识别出主要肺细胞类型,如衬里气道的上皮细胞、免疫细胞和血管细胞。两种基因 TPPP3 和 VEGFA 脱颖而出:它们在气道上皮细胞中表达最强,并与涉及 ROS 的通路密切相关。由于这些表层细胞构成对烟雾和污染的第一道屏障,其异常的基因活性提示长期刺激如何演变为持续的结构性损伤。
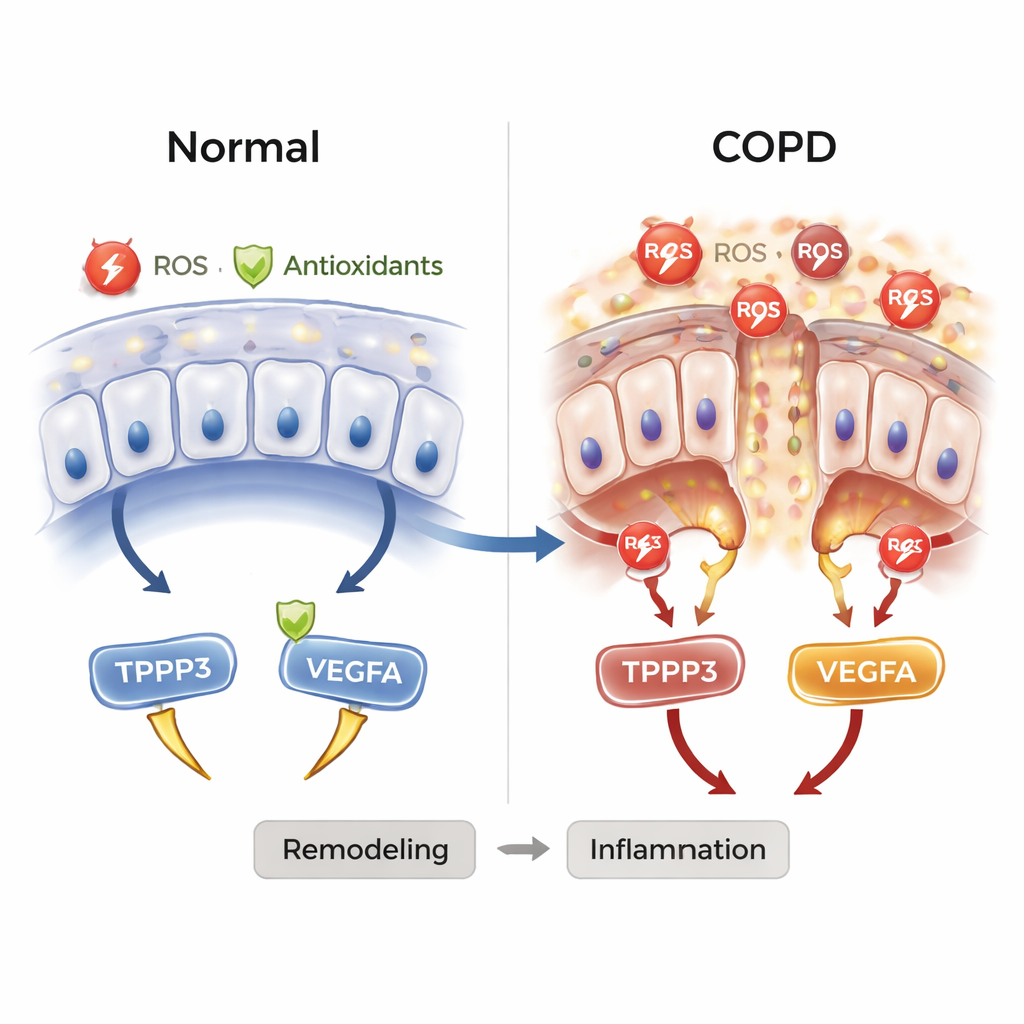
在实验室中重现烟雾损伤
为验证计算预测,团队将体外培养的人支气管上皮细胞暴露于香烟烟雾提取物,模拟吸烟者的气道。在显微镜下,受烟雾处理的细胞显示出显著增加的 ROS,同时天然抗氧化防御下降。典型的 COPD 炎症分子也大幅上升。重要的是,受压应激的细胞中 TPPP3 与 VEGFA 的表达显著提高,证实烟雾诱导的氧化应激能促使这些基因升高。该实验模型支持 TPPP3 与 VEGFA 将氧化损伤与炎症及气道结构重塑联系起来的观点。
对未来护理的意义
对于非专业读者,核心信息是:本研究描绘了多年来烟雾与污染暴露如何通过分子线路导致永久性呼吸问题。通过锁定 12 个关键的氧化应激相关基因,尤其是气道上皮细胞中的 TPPP3 与 VEGFA,这项工作突出了未来可能用于血液或组织检测以更早诊断 COPD 或将患者分型的潜在标志物。它也指出了未来药物可能干预的新分子开关,旨在减缓甚至预防导致 COPD 严重残疾的气道增厚与瘢痕形成。
引用: Choi, W., Wu, Y., Chen, W. et al. Oxidative stress-associated genes TPPP3 and VEGFA in COPD revealed by bulk and single-cell sequencing analysis. Sci Rep 16, 6801 (2026). https://doi.org/10.1038/s41598-026-37375-4
关键词: 慢性阻塞性肺病(COPD), 氧化应激, TPPP3, VEGFA, 气道重塑