Clear Sky Science · zh
设计与免疫原性的重组布拉迪酵母分泌P2‑VP8亚单位轮状病毒疫苗
为何一种肠道友好型酵母可能对儿童健康至关重要
轮状病毒是导致幼儿严重腹泻的主要原因,尤其在医疗资源难以获得的低收入国家更为严重。现有疫苗挽救了许多生命,但在这些地区效果较差,而且需要从工厂到诊所全程冷链保存。本研究探讨了一种非常不同的疫苗思路:将一种常见的益生酵母改造成微小工厂,在肠道中释放轮状病毒蛋白,从而希望以一种便于投递且稳定的形式诱导保护性免疫。
把有益微生物变成疫苗递送载体
研究者将注意力集中在布拉迪酵母(Saccharomyces boulardii)上,这是一种已用于预防或治疗腹泻的益生酵母。他们的想法是对该酵母进行工程改造,使其分泌轮状病毒表面蛋白的一段片段——称为VP8的区域,该区域为病毒附着于人体细胞所用。他们将VP8与先前被证明能增强疫苗反应的一段短助剂肽P2融合,形成名为P2‑VP8的组合蛋白。因为只使用了病毒的一小段且无感染性,这种方法属于“亚单位”疫苗范畴,旨在比整病毒疫苗更安全、更易处理。
先在计算机上设计疫苗候选体
在开展动物实验前,团队使用一系列计算工具预测P2‑VP8蛋白的性能。他们绘制出VP8中免疫细胞可能识别的片段,并检查这些片段在不同人类遗传背景下是否具有广泛效力。随后他们构建了P2‑VP8的三维模型,并模拟其与免疫细胞上的感受器TLR3的相互作用,该受体有助于检测病毒感染。模拟结果表明P2‑VP8稳定、可溶、无毒,并能够与该免疫受体形成较强、持久的结合,这些都是作为疫苗候选体的积极信号。
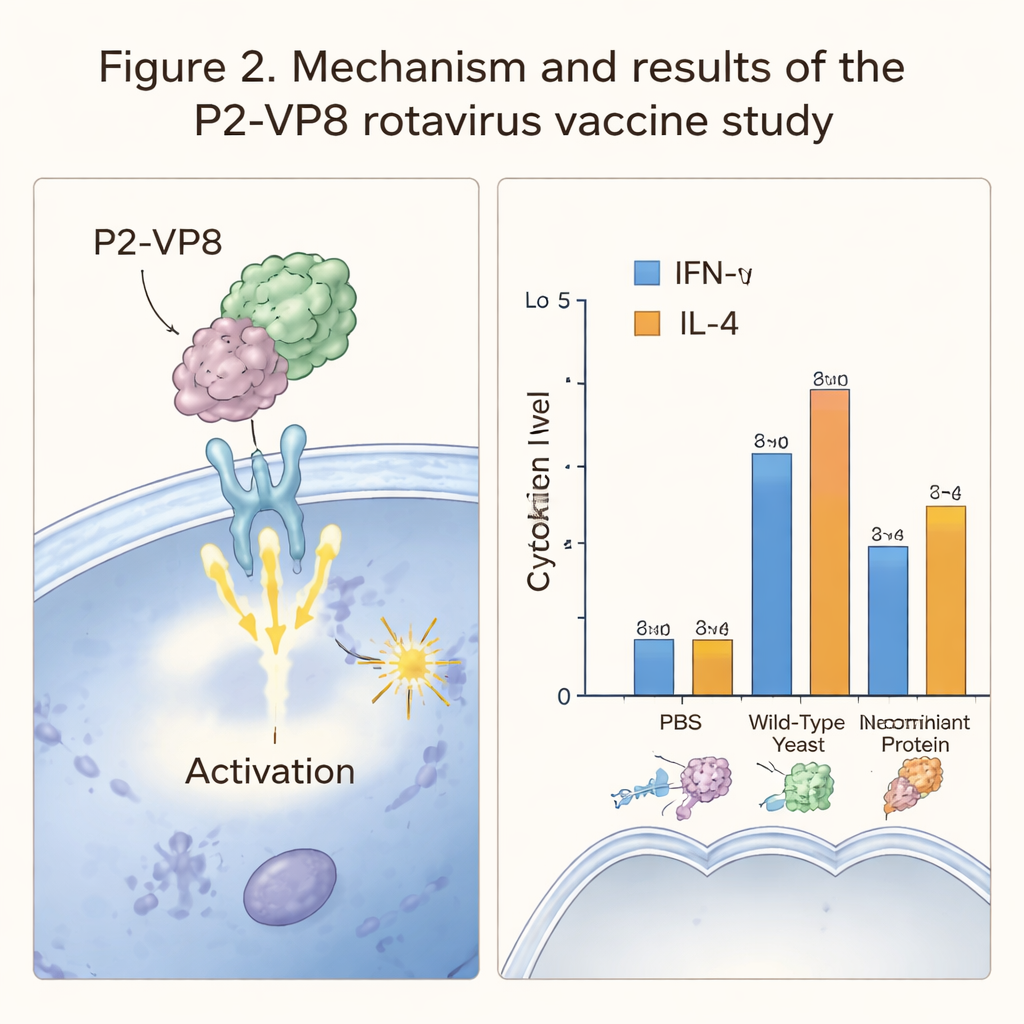
工程化酵母以分泌轮状病毒蛋白
为使益生酵母高效产生该蛋白,研究者对P2‑VP8基因进行了密码子优化——使用布拉迪酵母更易识读的三联密码子。这种优化类似于把食谱翻译成酵母的母语,使其合成机器能更快更准确地执行。随后他们将优化后的基因插入酵母表达载体并转化入S. boulardii。在体外培养中,研究者通过标准的蛋白电泳(SDS‑PAGE)和用定制抗体进行的西方印迹确认了工程酵母分泌出与预期大小一致的蛋白,证明该益生菌确实可以充当疫苗片段的“活体生产者”。
在小鼠中检测免疫反应
接下来团队考察了这种基于酵母的疫苗在活体中的表现。小鼠在数周内口服给予包埋的重组酵母,对照组则分别给予普通酵母、生理盐水或经注射给予的纯化P2‑VP8蛋白。免疫接种后,研究者测量了反映不同类型免疫激活的关键细胞因子IFN‑γ和IL‑4。接受工程酵母或注射蛋白的小鼠显示这些细胞因子水平均高于对照动物,表明其免疫系统对轮状病毒片段产生了识别和反应。然而,在口服酵母组未观察到强烈的T细胞增殖或显著的抗体水平,这表明口服给药诱导的免疫反应相对较弱。
这项工作意味着什么以及仍需改进之处
总体而言,这项研究表明可以将一种益生酵母改造成分泌主要轮状病毒疫苗片段的“工厂”,且该构建体在详尽的计算测试中表现如预期。在小鼠中,工程酵母引发了部分免疫活性,但未能产生达到有效疫苗所需的强烈、具有保护性的反应。对非专业读者的结论是:利用友好微生物作为可食用疫苗的概念在技术上可行,但目前的设计尚不足够强大。未来工作需要改进蛋白设计、剂量和递送策略,并在投入实际应用前进行针对轮状病毒感染的直接保护性试验。
引用: Farhani, I., Yamchi, A., Nikoo, H.R. et al. Design and immunogenicity of a recombinant Saccharomyces boulardii secreting the P2-VP8 subunit rotavirus vaccine. Sci Rep 16, 6932 (2026). https://doi.org/10.1038/s41598-026-37374-5
关键词: 轮状病毒疫苗, 益生酵母, 亚单位疫苗, 口服免疫, 疫苗设计