Clear Sky Science · zh
通过高场宽带太赫兹波的非热效应在人体上皮细胞中诱导的DNA双链断裂实现高效凋亡
关于杀灭癌细胞的新视角
癌症治疗经常走在一条钢丝上:既要摧毁肿瘤细胞,又不能严重损害健康组织或免疫系统。本研究探索了一种不寻常的工具——强烈的太赫兹(THz)波,这是一种位于微波与红外之间的看不见光。研究者表明,精心调控的高场THz脉冲可以在不加热组织或导致易引发炎症的混乱性细胞死亡的情况下,诱导癌细胞以受控方式“自杀”(凋亡)。
为什么温和的细胞死亡很重要
许多常见的癌症疗法会推动细胞走向死亡,但常伴随附带损伤。药物和生物制剂随着肿瘤产生耐药性可能失效,并可能削弱免疫系统。X射线、放射性或基于热的消融等物理方法可能损伤周围健康组织,常导致坏死——一种剧烈的细胞死亡形式,会引发炎症和疼痛。一种能够驱动凋亡的方式——一种细胞安静地自我拆解的整洁自毁过程——可能为缩小肿瘤提供一种创伤更小的途径,尤其适用于靠近皮肤的肿瘤。
太赫兹波遇到乳腺癌细胞
研究团队将重点放在人体乳腺癌细胞(MCF‑7)上,这是一种常用于实验室研究的上皮细胞。他们在维持正常体温的条件下,用非常强的宽带脉冲THz波照射这些细胞长达四小时。场强达到每厘米数百万伏特,远高于日常设备的水平。在这些条件下,随着照射时间延长,发生凋亡的细胞比例稳步上升。在测试的最高THz强度下,近99%的癌细胞进入凋亡,而死于坏死的不到1%。这一大规模且清洁的程序性细胞死亡浪潮表明,THz脉冲的作用不仅仅是加热细胞。
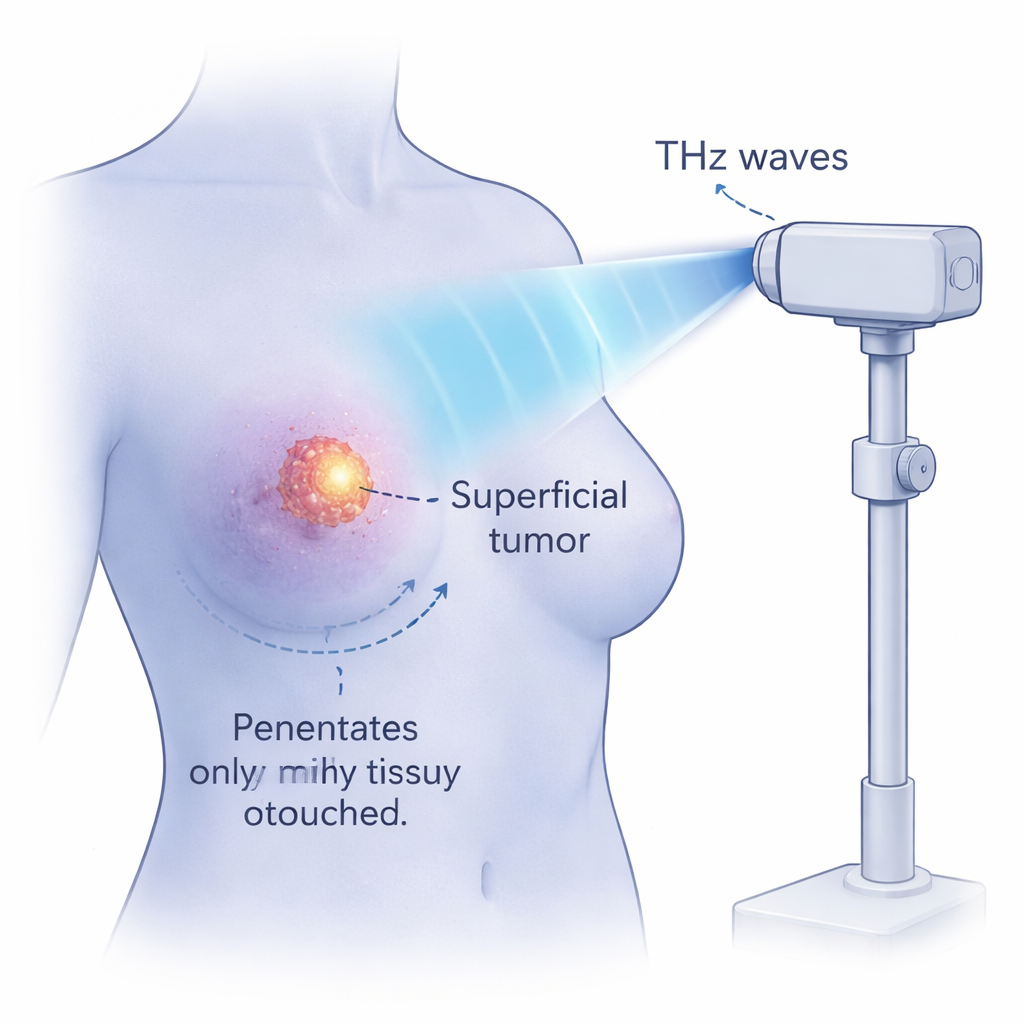
非加热效应与安全温度上限
由于水对THz辐射有强烈吸收,明显的担忧是意外加热。科学家们使用热成像跟踪照射过程中的温度变化。即使在中等强度下照射四小时,癌细胞温度也仅上升约3 °C,坏死率仍低于4%。单独的对照实验中,仅通过加热处理四小时表明,低于41 °C时几乎无细胞死亡,而在超过43 °C时坏死率出现急剧上升。即便在最强的THz设定下,研究者也将细胞温度保持在此43 °C阈值或以下,同时仍观察到几乎全部的凋亡且坏死最少。通过降低脉冲的重复频率,他们表明可以在控制温度的同时保持强效的抗肿瘤作用,强调了非热机制在起作用。
搅动DNA并启动死亡基因
为找出该机制,团队观察了细胞内部。在电子显微镜下,接受THz处理的细胞表现出典型的早期凋亡征象:遗传物质浓缩、细胞核改变且外膜完整。利用称为γ‑H2AX的荧光标记,他们检测到大量DNA双链断裂——在受照射细胞中这种损伤显著多于未处理或轻度加热的对照组。损伤分布与THz束的强度轮廓一致,向中心变强。基因和蛋白分析显示,一组应激与损伤响应分子(如GADD45B和c‑Jun)被强烈激活,而传统细胞死亡路径中的著名参与者,包括p53和多种caspase,变化不大。作者提出,高强度THz场可能在DNA中驱动剧烈的振动“共振”,从物理上拉伸并断裂双螺旋,进而触发一种不同于p53和caspase的凋亡通路。
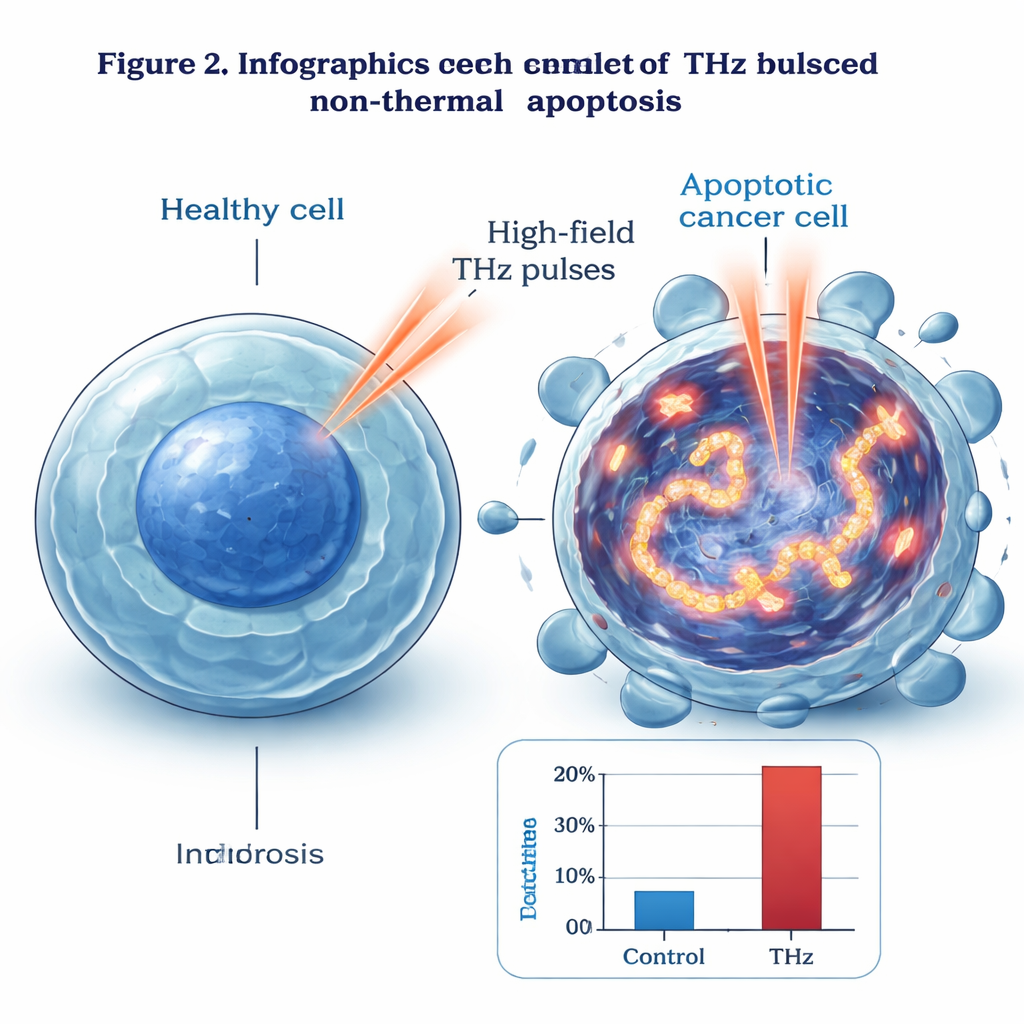
从培养皿到未来疗法
尽管这些实验在细胞培养中进行,但它们暗示了一种新的物理癌症疗法思路。高场THz波似乎能够穿透潮湿组织数毫米——足以到达浅表肿瘤——但衰减迅速,可能保护更深层器官。因为这种效应主要是非热性的,理论上它可以一层层地杀死癌细胞而不灼伤周围组织或引发强烈炎症。仍有大量工作要做:提出的DNA“共振”机制需要确认,对正常细胞的安全性需彻底测试,并需开展动物与临床研究。尽管如此,这项研究为这样一种构想打开了大门:精心设计的光脉冲,调谐至生物分子的天然运动,可能有一天为消融某些癌症提供一种精确且相对温和的方法。
引用: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
关键词: 太赫兹癌症治疗, 非热性凋亡, DNA双链断裂, 乳腺癌细胞, 物理肿瘤消融