Clear Sky Science · zh
基于磁性纳米颗粒的肿瘤学通用血管模型:几何与微流体特性
引导体内微小磁体
想象能够用磁场把抗癌药物直接拉进肿瘤,从而让身体其他部位免受强烈副作用的侵害。本研究探讨微小磁性颗粒如何在类似血管的网络中移动,并提出一个看似简单却耐人寻味的问题:在真实的流动条件下,磁场是否真的能把这些颗粒按医生的意愿引导到目标部位?
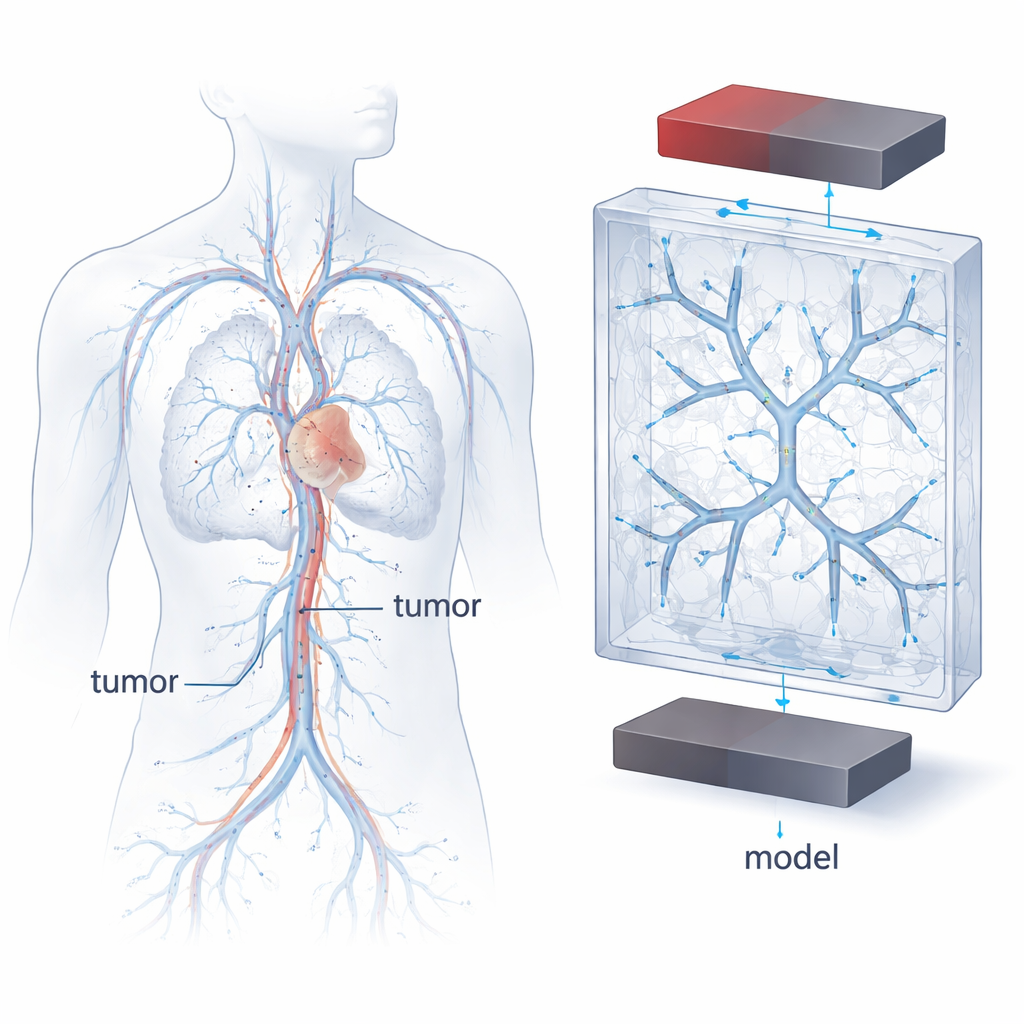
为何血管几何与流动重要
磁性肿瘤治疗依赖超顺磁性氧化铁纳米颗粒(SPIONs),这些颗粒在血流中携带药物时可被磁场牵引。但血管并非简单的直管:它们会分支、变窄、弯曲和分裂,血流速度也会随之加快或减慢。这些形状和速度的变化会影响颗粒的运动轨迹、聚集位置以及它们与血管壁接触并足够停留以便粘附的可能性。真实患者的血管差异极大,这使得比较实验或预测新疗法的行为变得困难。因此,作者着手构建一种高度可控、可重复的“模型血管”,同时尽可能保留肿瘤供血血管的关键特征。
构建理想化的肿瘤供血网络
为设计这些模型血管,研究团队借鉴了描述真实动脉如何分支的经典规则。其中一个规则是穆雷定律,它将母血管与子血管的直径联系在一起,反映出能量效率的网络设计。研究者结合乳腺肿瘤的临床测量数据和这些比例定律,数学生成了模拟肿瘤供血血管向毛细血管床收缩的分支树。随后,他们用高分辨率3D打印在透明塑料块中嵌入两级、三级或四级分支的空心通道网络。通道遵循对称分支模式并在三维空间延伸,提供了一个简化但具有生理启发性的环境来研究颗粒运动。
观察磁性颗粒的运动
在这些打印的网络中,团队用水作为血液的替代物泵送,然后在上游注入含SPION的液体,并在模型周围施加静态磁场。高速成像记录了暗色颗粒云通过不同分支的过程,计算机分析则将亮度变化转换为反映局部颗粒存在的时间分辨信号。通过改变背景流速、颗粒浓度、分支复杂性以及有无磁场等条件,研究人员能够解析每个因素如何影响颗粒分布、停留时间以及最终在通道壁上的沉积。
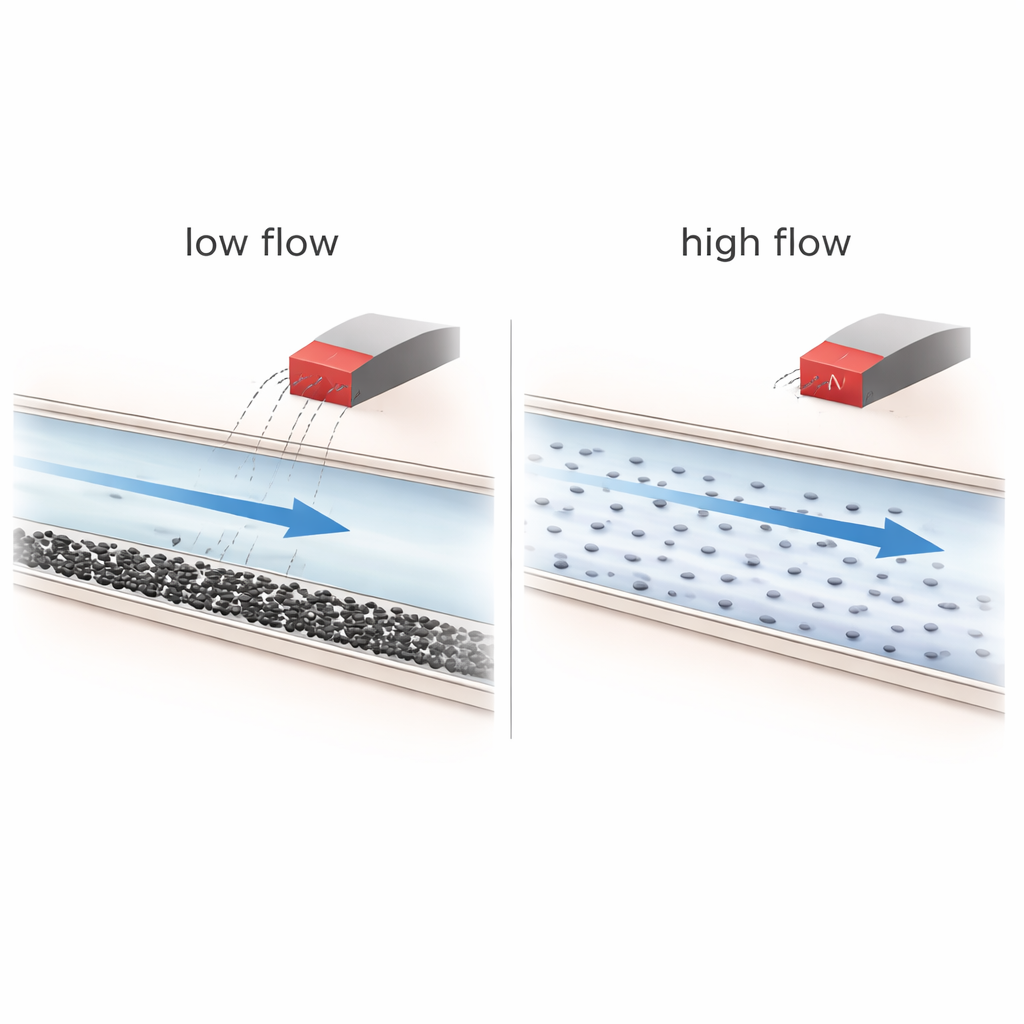
磁场何时有用——何时无效
实验表明,流动条件是决定性因素。在较高流速下,流体混合良好,纳米颗粒随流快速移动;在这种情况下,磁场几乎不起作用,颗粒只是沿流线通过网络。然而在低流速下,重力和浓度效应会使颗粒向通道底部沉降,形成分层,有时还出现松散的团聚。在这种已经不均匀的情况下,磁场可以将更多颗粒引导进某些分支并略微延长它们的停留时间,尤其是在更复杂、分支更多的网络中。但计算表明,在实验条件下,单个40纳米颗粒所受的磁力比流体的粘性阻力小好多数量级,因此实现真正的“单颗粒操控”在物理上并不现实。
这对未来癌症疗法意味着什么
对非专业读者而言,主要结论是:仅靠磁场无法可靠地将自由悬浮的纳米颗粒从快速流动的血流中拉出。明显的磁效应只会在颗粒已经减速、沉降或聚集时才出现——这些情形会放大它们对磁场的响应。本文介绍的通用3D打印血管模型为在不同网络几何和流动状态下系统研究此类效应提供了标准化方法。对未来的磁性药物靶向策略而言,本研究提示成功的做法更可能需要利用群体行为(如受控聚集或载体系统),而不是单靠在大型、灌流快速的血管中操控孤立纳米颗粒。
引用: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
关键词: 磁性药物靶向, 纳米颗粒, 肿瘤血管, 微流体模型, 药物输送