Clear Sky Science · zh
跨体外与体内模型的富里酸制剂的综合安全性与微生物群谱分析
古老土壤化合物的现代健康潜力
如果一种由植物残体在数百万年中分解形成的物质,能够悄然支持你的肠道、免疫系统,甚至帮助组织自我修复,会怎样?本研究探讨了富里酸——土壤与泥炭中腐殖质的有机成分——作为一种潜在的“多功能”补充剂。研究者在实验室培养的人类与动物细胞以及豚鼠体内,提出了一个看似简单但关键的问题:经过精心制备的富里酸溶液是否既安全又能真正对细胞与肠道微生物产生有益影响?
什么是富里酸及其重要性
富里酸是由微生物缓慢分解植物与动物残体所产生的一类小型、可溶于水的混合分子。由于其复杂的化学性质,早期研究提示它可能具有抗氧化、调节炎症、促进伤口愈合并影响土壤、动物与人体微生物的作用。然而,过去的研究通常只关注单一效应,且使用的制剂差异大、难以比较。本研究聚焦于两种标准化的化石来源液体制剂,称为MLG‑50(酸性)和MLG‑A50(碱性)。两者均取自美国南部的一处古老富有机质矿床,含有富里酸及镁、钙、钠、钾、硫等矿物质。研究团队旨在以协调一致的方式评价这些制剂:检测对哺乳动物细胞的安全性、潜在的DNA损伤、对炎症与组织修复的影响,以及在体外与体内对肠道细菌群落的改变。
安全优先:对细胞及其DNA的影响
为评估安全性,研究者将小鼠皮肤细胞与人类肠道和肝细胞系暴露于广泛浓度范围的富里酸。于非常高浓度(几乎未经稀释)时,酸性制剂MLG‑50降低了细胞存活率;但在较高稀释度——也就是补充剂相关的浓度范围内,MLG‑50与MLG‑A50均被良好耐受,在某些情况下甚至轻微增强细胞活性。随后他们使用敏感的“彗星”实验检测单细胞DNA断裂。与未处理细胞相比,富里酸制剂引发可测的微量DNA损伤增加,但水平远低于用于判定化合物有致突变性的标准阈值。事实上,在相同条件下,维生素C与阿司匹林等常见参比化合物造成的DNA损伤更高,这表明这些富里酸制剂处于典型安全边际之内。
促进细胞增殖、伤口闭合与抑制炎症
除了单纯的存活评估外,团队还研究富里酸是否能促进肠道细胞生长与修复。在增殖试验中,稀释的MLG‑50,尤其是MLG‑A50,在最初几天内暂时增加了肠上皮细胞的数量,相较于未处理培养物和几乎无效的参比富里酸标准表现更好。在“划痕”伤口愈合实验(在细胞层上制造缺口以模拟组织损伤)中,MLG‑A50表现突出:它加速了早期伤口闭合,并在72小时内维持了这一优势,显示出促进再生的作用。研究者随后转向免疫系统,使用类似单核细胞的细胞模型,这类细胞在接触细菌内毒素(LPS)时会激活一个关键的炎症开关NF‑κB。单独使用富里酸配方并不会触发该警报系统——这从安全角度是好消息。但在LPS与富里酸共同处理时,NF‑κB的激活约降低60%,强效炎症介质TNF与IL‑6的产生约减半,而具有镇静作用的细胞因子IL‑10则被保留或甚至上调。这一模式表明富里酸并非使免疫系统瘫痪;相反,它似乎抑制过度反应,同时保留保护性调节。
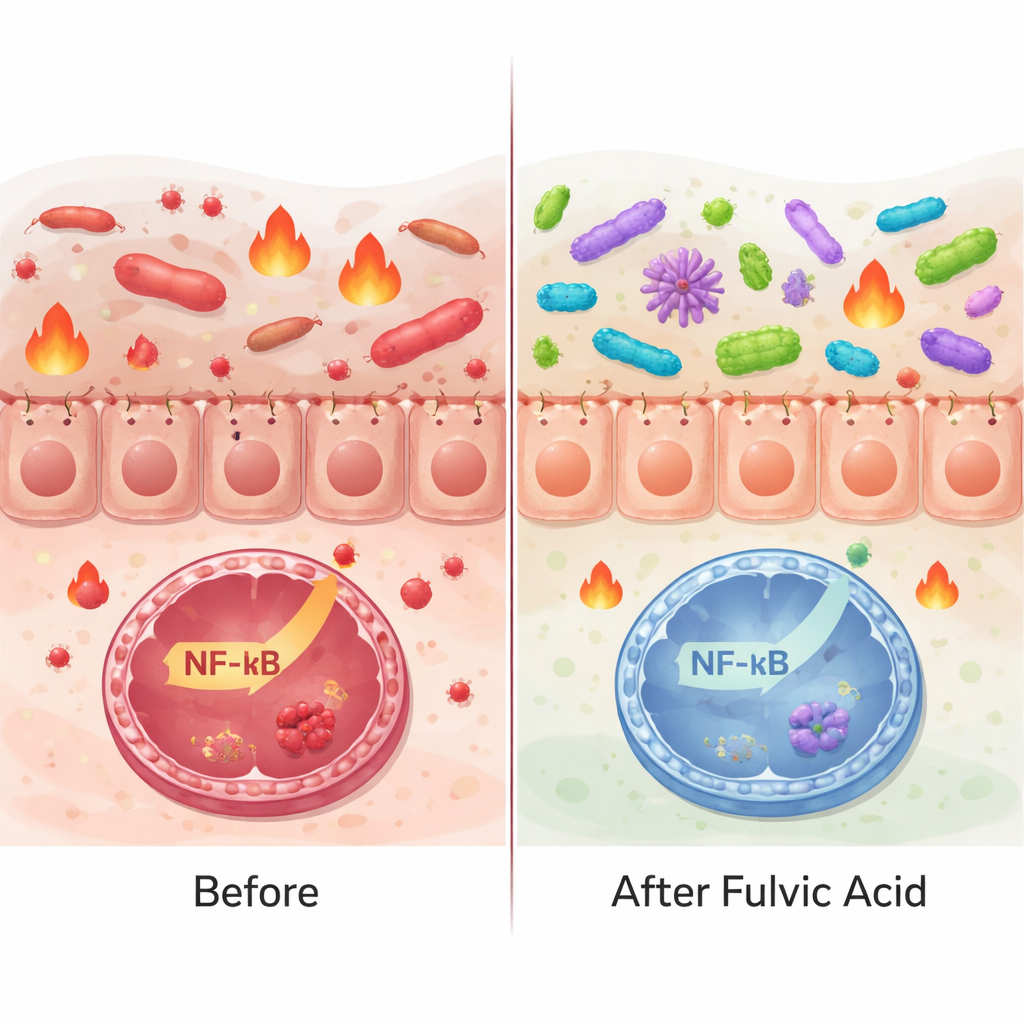
养护有益微生物,同时抑制病原
由于富里酸能结合矿物质并影响氧化还原(电子转移)反应,它也可能塑造微生物群落。在试管实验中,MLG‑50显著促进了益生乳酸菌属的生长与代谢活性,而对与疾病相关的细菌如大肠杆菌与沙门氏菌则没有增强作用,甚至略有抑制。MLG‑A50虽然支持作用更温和,但仍选择性地有利于有益菌株。为观察在活体肠道中的表现,研究者给豚鼠连续三周低剂量喂服两种制剂。粪便DNA测序显示总体微生物多样性增加——这一特征通常与更有韧性的肠道有关。某些与肠道健康相关的细菌类群,如部分梭菌纲(Clostridia)和乳酸菌近缘种呈上升趋势,而潜在问题菌属如幽门螺杆菌(Helicobacter)与弯曲杆菌(Campylobacter)则显著减少。这些体内发现与体外观察到的选择性“利好益菌、抑制坏菌”效应相呼应,表明富里酸能够温和地重塑肠道生态,而不是简单地作为广谱抗菌剂。
对未来健康应用的可能意义
综上所述,该研究并非将富里酸描绘为万能灵药,而是显示其作为一种有前景的多功能辅助因子。在适当稀释下,经测试的制剂表现出低毒性与极少的DNA损伤,促进肠道细胞生长与伤口闭合,抑制过度的炎症信号同时保留保护性机制,并引导肠道微生物向更为多样且益生菌友好的平衡发展。对普通读者而言,这暗示经细致表征的富里酸产品未来或可成为“免疫营养”策略的一部分——支持肠道屏障、微生物组与免疫平衡,尤其在慢性炎症或康复情境中具有潜在价值。作者强调仍需更多机制研究与人体试验,尤其是用于优化剂量与长期安全性的细化工作。但来自细胞与动物的综合证据为某些富里酸制剂作为温和、全身性支持工具的进一步考量提供了有力依据。
引用: Szwed-Georgiou, A., Płociński, P., Włodarczyk, M. et al. Integrated safety and microbiota profiling of fulvic acid formulations across in vitro and in vivo models. Sci Rep 16, 6166 (2026). https://doi.org/10.1038/s41598-026-37331-2
关键词: 富里酸, 肠道微生物组, 抗炎, 益生菌, 伤口愈合