Clear Sky Science · zh
靶向 Akt–EphA2 轴与细胞–细胞粘附以增强癌细胞对失锚性凋亡的敏感性
为什么游离漂浮的癌细胞很重要
当癌细胞脱离肿瘤并通过血流迁移时,按理它们应该会因为失去与周围组织的依附而死亡。这种内建的安全程序称为脱落诱导细胞死亡,有助于防止健康组织在不该生长的地方生长。然而,转移性癌细胞常常学会无视这一信号,在漂浮时存活,从而更容易播种新肿瘤。本研究提出了一个看似简单的问题:如果我们在侵袭性乳腺癌细胞中恢复一项关键的机械“触觉”能力,能否迫使这些游离的细胞走向死亡?如果不能,它们又会用何种备选手段求生?
唤回丢失的触觉
细胞不断测试周围环境的刚度,通过牵拉锚定它们的结构来感知。在健康组织中,失去接触或降落在非常柔软的表面上往往会触发自毁程序。蛋白质 Tropomyosin 2.1 (Tpm2.1) 是这种内部张力机械装置的重要组成部分,并且在癌细胞中常常缺失或表达降低。研究人员使用一个被广泛研究的转移性乳腺癌细胞系,并对其进行工程改造以产生更多的 Tpm2.1,从而恢复了很大一部分刚性感知。当这些被改造的细胞被迫在专门的不粘培养皿中生长以防止附着时,它们确实表现出更多的细胞死亡、增殖减慢并且运动能力降低。然而,即便在悬浮几天后,约仍有 70% 表达 Tpm2.1 的细胞存活,表明仅仅恢复触觉并不能完全解决问题。
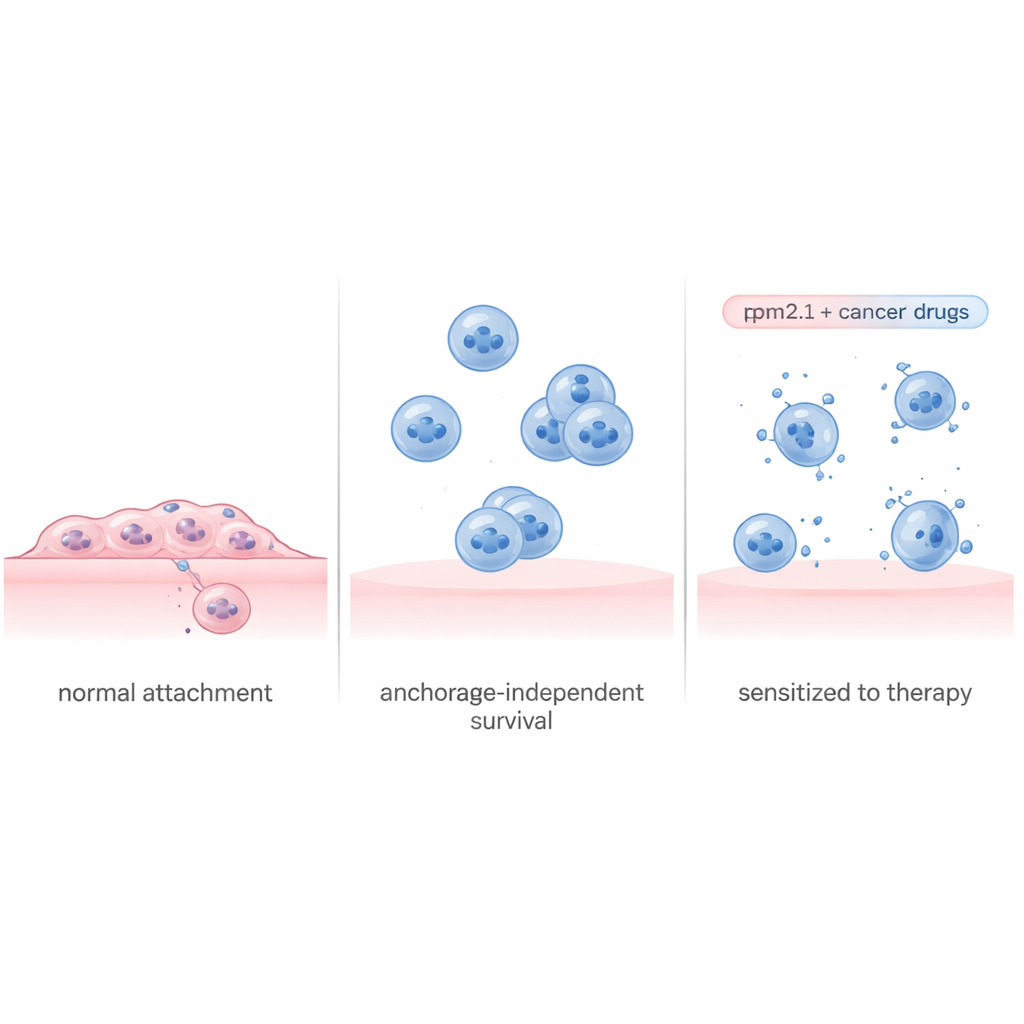
解读癌细胞的生存手册
为了解为何部分细胞死亡而另一些存活,研究团队将漂浮的表达 Tpm2.1 的细胞分为两组:一组显示细胞死亡的早期征象,另一组看起来健康。随后他们测量了两组在四天内基因的开关情况。濒死细胞表现出与细胞分裂、DNA 修复和附着相关程序的广泛关闭,以及类似单向通往自毁的应激信号。相反,存活的细胞激活了一套协调的生存计划。脱落早期,它们开启了炎症和免疫相关通路,随后增强了主要的生长与存活回路,包括以蛋白 Akt 为中心的著名通路。与此同时,它们强烈上调了促进细胞相互粘附的基因,使其即便在不能附着于基质时也能形成保护性的细胞团簇。
集体的力量:细胞簇如何抵抗死亡
因为基因数据指向细胞–细胞粘附的增加,研究者检验了简单的人群集中是否能帮助细胞在悬浮中存活。当表达 Tpm2.1 的细胞在高密度下生长、易于形成簇时,死亡的细胞明显比稀疏培养时少。一个粘附分子 ICAM1 在存活细胞中尤为升高,它已知有助于循环肿瘤细胞簇的形成并在远端组织着床。用小分子抑制剂阻断 ICAM1 会使更多表达 Tpm2.1 的细胞在悬浮中死亡,而对常规附着培养影响甚微。这些发现支持这样一种观点:一旦其内部力学部分恢复,癌细胞仍可通过彼此紧密相依而不是依附于环境来逃避死亡。
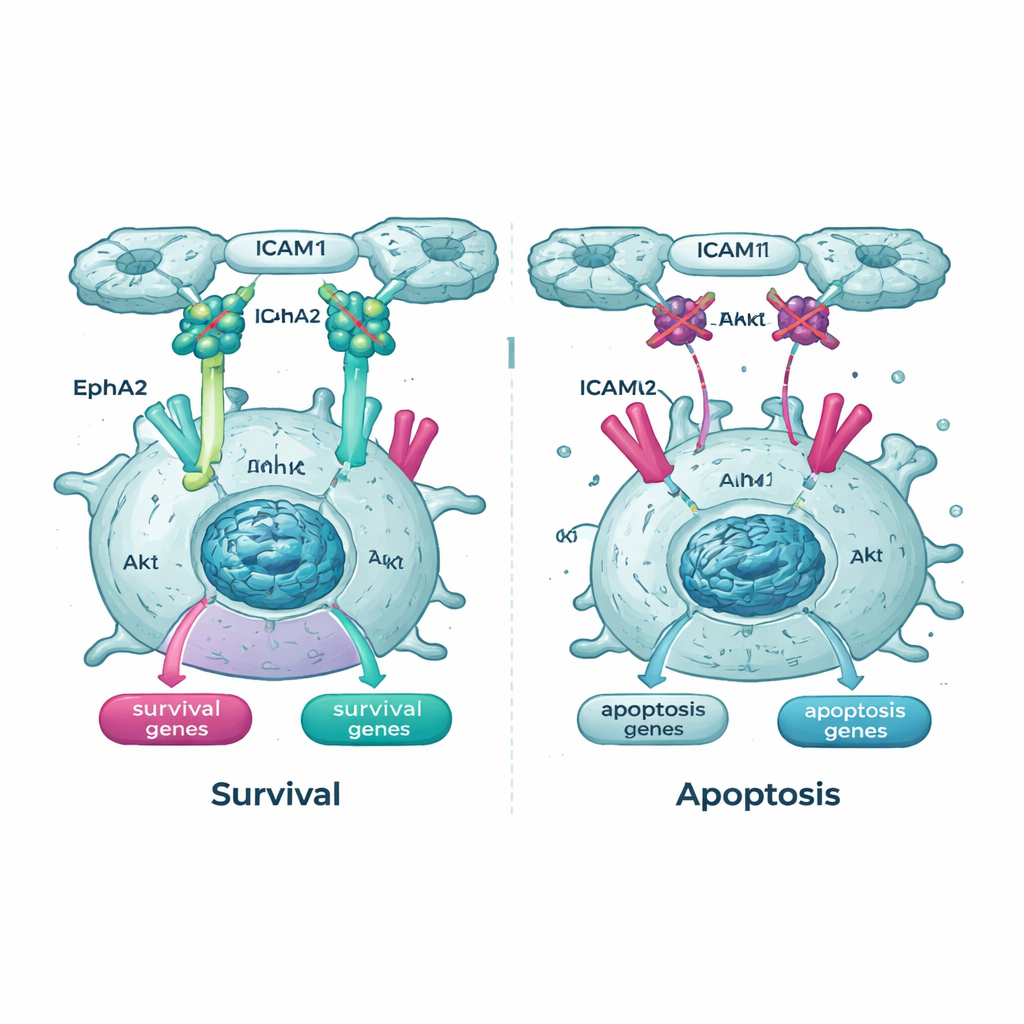
切断细胞内的关键生命线
基因学调查还强调了 Akt 通路及其一位伙伴——称为 EphA2 的受体,作为悬浮癌细胞的重要生命线。在表达 Tpm2.1 的细胞中,悬浮状态下活性化的、经磷酸化的 Akt 比对照细胞更低,EphA2 的水平和活性也有所下降。当团队用阻断 Akt 或 EphA2 的药物处理细胞时,无论是常规细胞还是表达 Tpm2.1 的癌细胞,在悬浮中都更容易死亡。值得注意的是,恢复刚性感知的细胞随时间对这些药物尤为敏感,这意味着一旦它们的机械安全检查部分重启,就更依赖剩余的存活信号。
将一种“被激活”的状态变成致命弱点
对非专业读者来说,关键的信息是:修复癌细胞中一个损坏的安全开关——即它们感知并响应失去接触的能力——是必要的但不充分以使其自毁。存活下来的细胞通过结成群体并将内部线路改道到替代的生长与存活通路来求生。这项工作表明,通过 Tpm2.1 恢复刚性感知会把转移性乳腺癌细胞置于一种“被激活”的状态——它们更接近死亡但尚未注定一死。随后同时阻断 Akt–EphA2 通路并通过 ICAM1 干扰细胞–细胞粘附,研究人员就能将这些被激活的细胞推向死亡边缘,大幅增加脱落诱导的细胞死亡。从实用角度看,该研究勾画出一种未来组合疗法的策略,旨在在游离肿瘤细胞播种新转移前将其消灭。
引用: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
关键词: 乳腺癌转移, 细胞粘附, 失锚性凋亡, Akt 信号传导, 刚性感知