Clear Sky Science · zh
定义的 Oligo-MM12 微生物组对单核细胞增生性李斯特菌肠道定植与播散的影响
为什么肠道中的微生物很重要
许多人知道单核细胞增生性李斯特菌是一种危险的食源性病原体,常与被污染的即食食品及易感人群的严重疾病有关。更不明显的是,这种细菌是否能在体内站稳脚跟,不仅取决于我们的免疫系统,还取决于已居住在肠道中的繁忙微生物群落。本研究利用专门设计的小鼠模型和一个迷你“人工结肠”来回答一个简单但重要的问题:肠道微生物组的复杂性如何影响李斯特菌在肠道中的定植能力及其在体内的扩散?
两种微生物“社区”的故事
为了解答这一问题,研究人员比较了两类小鼠。一组称为 SPF 小鼠,携带一种丰富、自然的肠道细菌混合物,类似于许多实验动物中发现的群落。另一组 Oligo-MM12 小鼠则只拥有由 12 种经过良好表征的细菌菌株构成的极简群落。由于该群落的每个成员都是已知且在多代间稳定的,Oligo-MM12 小鼠成为解析哪些微生物有助于阻挡入侵者、哪些可能留下防御空档的强大工具。通过对比这两类小鼠,团队可以检验一个密集、多样的肠道生态系统与一个精简、极简生态系统在应对感染挑战时有何不同。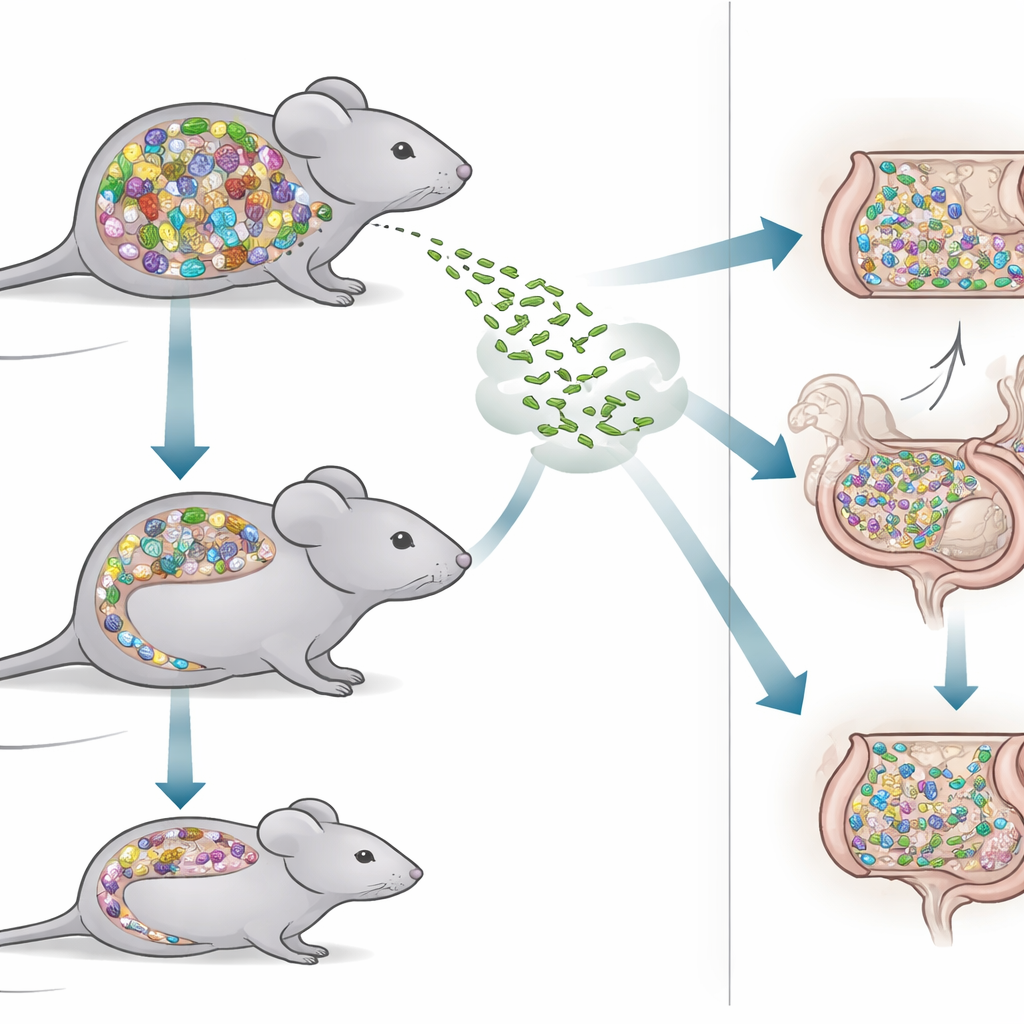
追踪李斯特菌在肠道内外的行踪
科学家对两类小鼠给予相同剂量的口服李斯特菌感染,并在三天内追踪粪便和内脏器官中出现的细菌数量。有趣的是,更简单的 Oligo-MM12 群落在最初似乎更能抑制李斯特菌:感染后第一天,这些小鼠在粪便中脱落的李斯特菌细胞比 SPF 小鼠少。然而,这种早期优势并未持久。到第三天,Oligo-MM12 小鼠排泄的李斯特菌更多,而 SPF 小鼠则稳步将其水平压低。尽管肠道内存在明显差异,但肝脏、脾脏和淋巴结等内脏器官中的李斯特菌数量在两种小鼠模型之间相当,这表明一旦李斯特菌进入深部组织,微生物组的复杂性所起的作用较小。
在受控“盒子”中模拟结肠
为了将宿主组织与免疫的影响与微生物自身行为区分开来,研究团队还使用名为 micro-Matrix 生物反应器的装置进行了体外(ex vivo)实验。他们用每种小鼠类型的粪便制成悬浊液,加入富营养培养基于密封、无氧的小孔中,并在部分微型培养中引入李斯特菌,同时将其他培养作为对照。在五天内,他们测量李斯特菌数量并测序细菌 DNA 以追踪群落如何演化。在这个人工结肠中,不论面临的是复杂的 SPF 微生物组还是更为简单的 Oligo-MM12 群落,李斯特菌均达到相似水平,其存在仅引起整体群落组成的温和变化。这一点与活体动物的结果形成对比,强调了免疫系统、肠道黏膜以及胆汁和黏液流动在真实肠道感染中所起的强大作用。
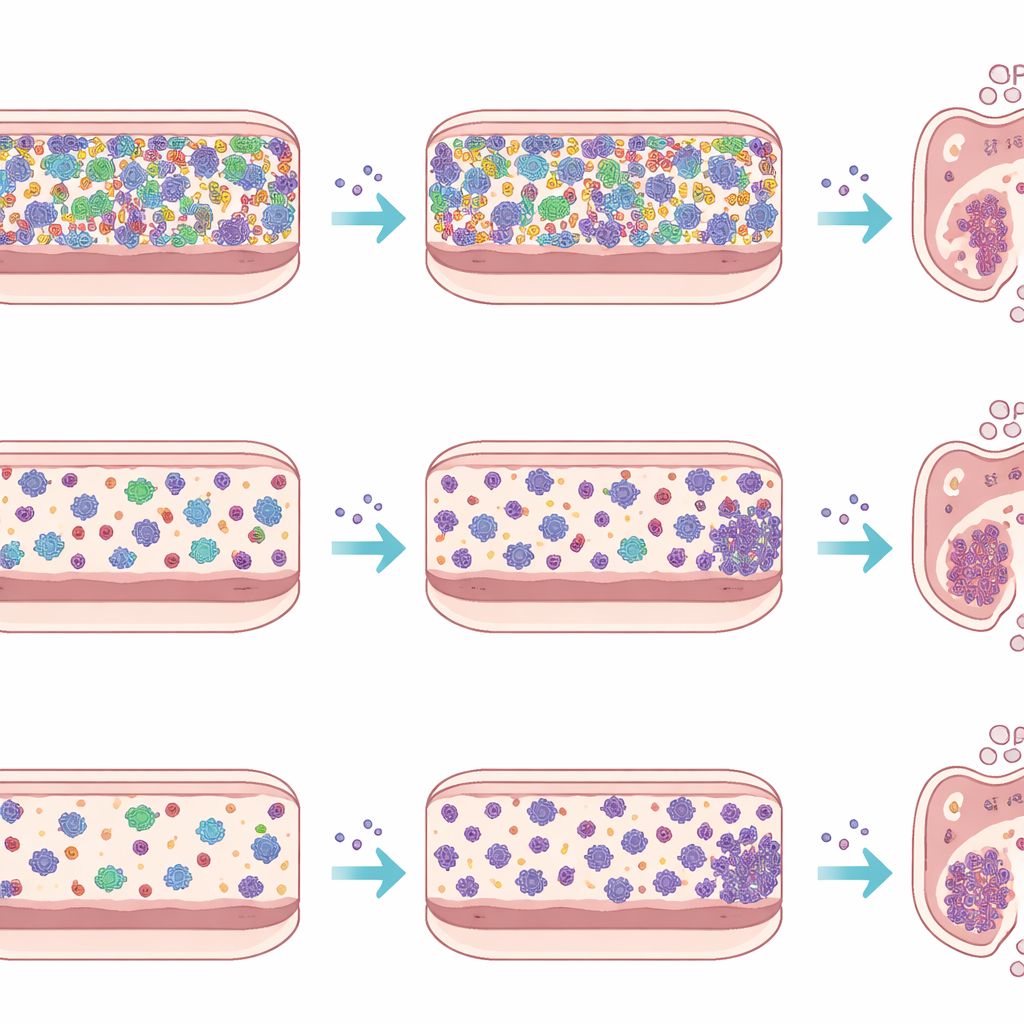
关键的微生物胜者、失败者与旁观者
通过观察在感染过程中哪些细菌群体增加或减少,研究锁定了可能影响李斯特菌成败的候选者。在 Oligo-MM12 小鼠中,与黏液相关且常与肠道健康相关的拟阿克曼氏菌(Akkermansia)在第二天下降,随后在第三天强劲反弹。在 SPF 小鼠中,若干已知产生有益代谢物或支持屏障完整性的属,如 Blautia 和 Bacteroides,在感染期间下降,而某些类 Prevotella 的细菌则显示出复杂的升降模式,这可能反映了它们被李斯特菌自身的抗菌物质直接影响。体外实验中,这些模式大多被削弱,进一步支持这样一种观点:许多观察到的群落变化并非仅由微生物间的直接竞争引起,而是病原体、定植微生物与宿主环境三者相互作用的结果。
这对保护人类意味着什么
对非专业读者而言,核心信息是:并非所有看起来健康的微生物组在防御感染方面都以相同方式发挥作用,“更多多样性”并不总是在任何时刻都是更好的选择。简化的 Oligo-MM12 群落在肠道中对李斯特菌提供了强劲的早期抵抗,但随时间推移,结构更复杂的 SPF 微生物组在清除入侵者方面表现更佳。这项工作表明,经过精心设计的低复杂度微生物组模型,结合可控的体外系统,可以揭示哪些细菌群体和环境因素在阻止危险的食源性病原体方面至关重要。最终,这类见解可为有针对性的益生菌或基于微生物组的疗法提供指导,在正确的时间增强合适的微生物同盟,以预防高危患者发生严重的李斯特菌感染。
引用: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
关键词: 李斯特菌感染, 肠道微生物组, 定殖抵抗, 小鼠模型, 益生菌