Clear Sky Science · zh
用于多亚型肾脏肿瘤分类的对比增强CT深度学习集成框架
为何及早发现肾脏肿瘤至关重要
肾癌可以多年无声无息,直到已发生转移才出现明显症状。然而借助现代影像学,许多肾脏占位在为腰痛或其他问题做检查时被偶然发现。关键问题随之而来:该占位是需要手术的危险性癌症,还是可以随访的良性病变?本研究探讨了人工智能如何帮助医生更准确地解读CT影像,既减少不必要的手术,又能及时发现具侵袭性的肿瘤。
五类肾脏肿块,一个艰难抉择
肾脏肿瘤并不相同。某些如血管成分脂肪瘤(AML)和肾上皮瘤(RO)是良性的,可能永远不会危及生命;而另一类被归为肾细胞癌(RCC)的则为恶性,能向其他器官转移。在恶性肿瘤中,透明细胞型RCC(ccRCC)最常见且最易发生转移;乳头状RCC(pRCC)和嗜铬性RCC(chRCC)通常侵袭性较低但仍然严重。然而在常规影像上,这些亚型外观常常相似,因此临床上往往依赖活检或手术以获得确诊。作者旨在检验一种复杂的计算机系统是否仅凭对比增强CT图像就能可靠地区分这五类肿瘤。
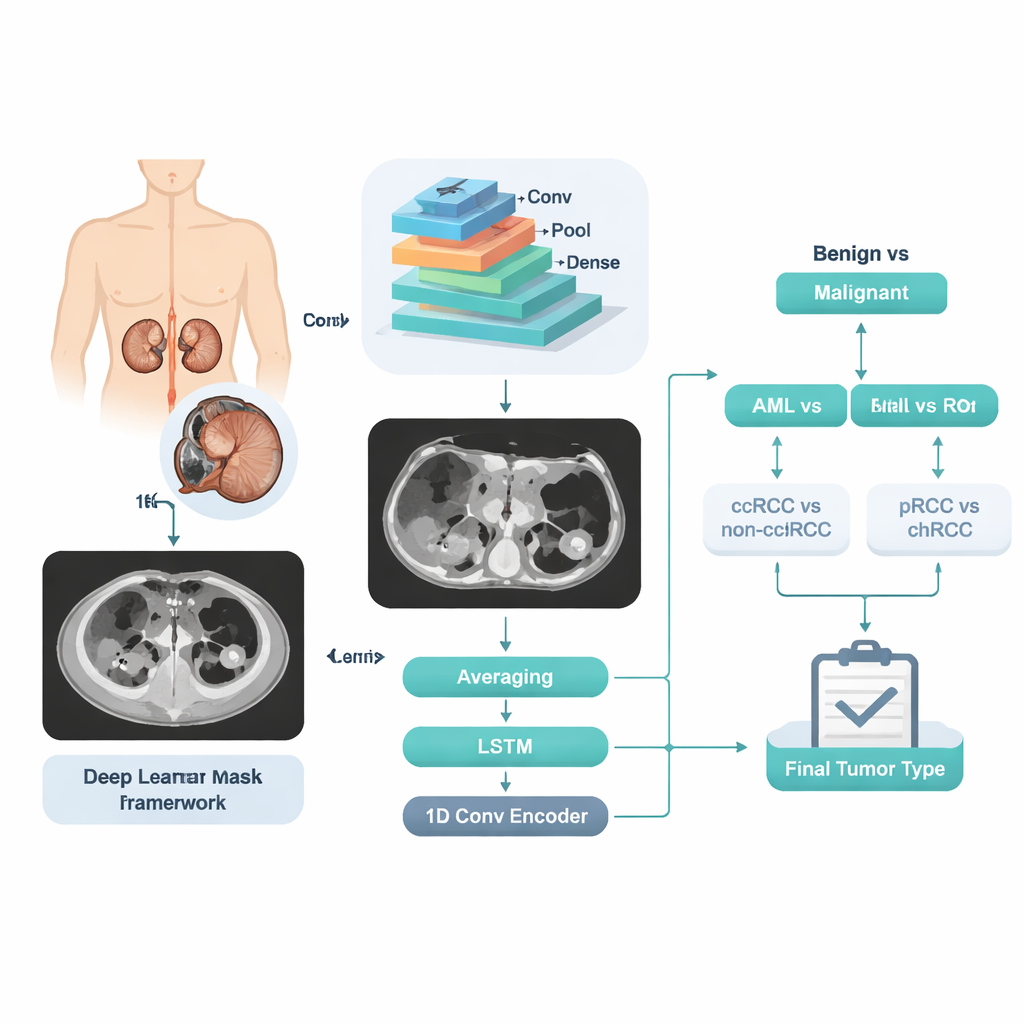
将CT扫描转化为可学习的模式
研究团队收集了280例经组织学确诊的肾脏肿瘤对比增强CT影像。资深放射科医师逐层手工勾画每个肿瘤,提供精确的“金标准”区域用于计算机学习。仅使用了一个CT分期——门静脉期,这一常用于常规检查的阶段,强调该方法应能兼容医院常见的影像协议。数据集最终包含五个明确标注的组别:84例ccRCC、36例pRCC、48例chRCC、72例AML和40例RO,覆盖广泛的年龄段和男女两性。随后作者按患者将病例划分为训练集、验证集和测试集,确保同一患者的图像不会出现在多个组中。
一步步的数字化第二意见
研究者没有让计算机直接从图像跳到五个标签之一,而是设计了一个分步决策流水线,模拟医生的判断过程。首先系统决定肿瘤是良性还是恶性。若为良性,第二步区分AML与RO;若为恶性,则先将ccRCC与其他RCC类型分开,随后再区分pRCC与chRCC。在每一步,一个强大的图像分析引擎——卷积神经网络会检查来自同一患者的多张切片。其内部的数值“特征”随后通过三种不同方式处理:对切片级预测进行简单平均、使用序列感知模型考察肿瘤在切片间的变化,以及用紧凑编码网络将整组切片压缩为单一特征签名。这三种意见被融合为该阶段的最终概率。
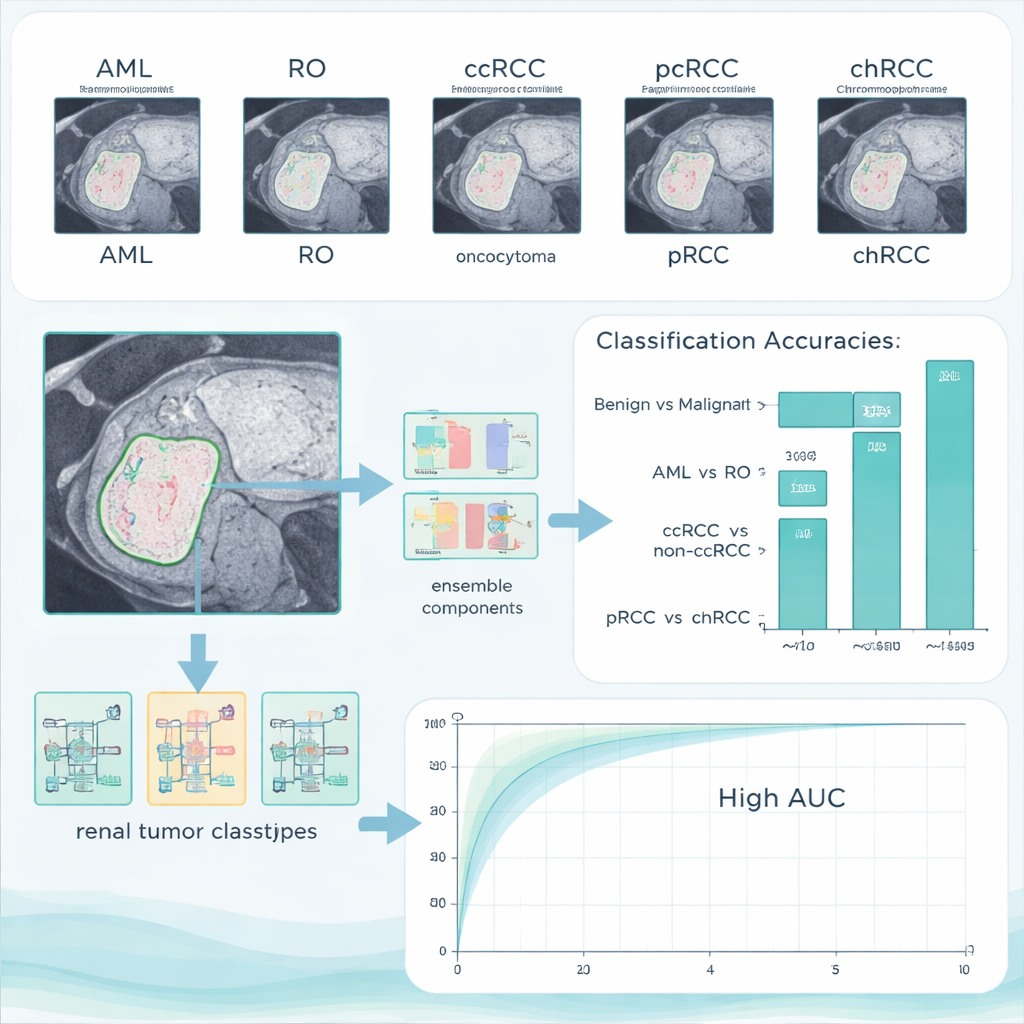
AI系统的表现如何
在主要测试集上,组合系统在区分良性与恶性肿瘤方面达到了96.4%的准确率,且没有良性病例被误标为癌症,仅有少量癌症被漏诊。在区分两类良性肿瘤时,系统实现了完美的100%准确率。更微妙的任务——将ccRCC与其他RCC类型区分开,以及将乳头状与嗜铬性癌区分开——更具挑战性,但系统仍保持在90%以上的准确率。重要的是,作者还将训练好的模型在另一个不同来源的公开数据集上进行了测试,性能仍然很高,表明该方法并非仅记忆某一医院的影像,而是能推广到新的患者和扫描设备。
这对患者可能意味着什么
简单来说,这项研究表明,AI“助手”能够以接近甚至在某些方面超越当前人工方法的方式解读肾脏CT影像,既能区分无害与危险的肿瘤,又能识别重要的癌症亚型。如能进一步验证,此类系统可帮助放射科医生避免对良性肿瘤进行不必要的活检和手术,同时在对侵袭性癌症的早期治疗决策中提供更大信心。对患者而言,这可能意味着更少的侵入性操作、更快的诊断结果,以及基于肿瘤具体性质的更个性化护理。
引用: Abdeltawab, H., Alksas, A., Ghazal, M. et al. A deep learning ensemble framework for multi-subtype renal tumor classification using contrast-enhanced CT. Sci Rep 16, 6657 (2026). https://doi.org/10.1038/s41598-026-37283-7
关键词: 肾癌, 肾脏肿瘤影像, 深度学习, CT扫描, 计算机辅助诊断