Clear Sky Science · zh
与多药耐药克雷伯氏肺炎菌抗菌耐药性逆转相关的全局调控因子与外排基因的综合分析
这些医院病菌为何如此难以消灭
在世界各地的医院中,某些克雷伯氏肺炎菌(Klebsiella pneumoniae)菌株已变得特别难以治疗。它们能抵御多种曾经有效的抗生素,使常见感染演变为危及生命的急症。本研究深入微生物层面,旨在理解这些细菌使用的一个重要伎俩:将抗生素泵出细胞外的微小“泵”,以及似乎能调节这些泵开启或关闭的遗传开关。
超级细菌及其分子逃生口
多药耐药的克雷伯氏肺炎菌现在在许多医院都能遇到,包括开展本研究的伊拉克医疗中心。这些细菌能同时存活于几大类抗生素之中,例如氟喹诺酮类、氨基糖苷类和三代头孢菌素。它们实现耐药的一个方式是在细胞包膜中装配强大的“外排泵”。其中最重要的系统之一称为 AcrAB‑TolC,它跨越细菌膜,像微型抽水机一样,将细胞内的抗生素分子抓住并排出细胞外,阻止药物造成严重损害。当这些泵高度活跃时,细菌内部的抗生素浓度永远达不到致死水平。
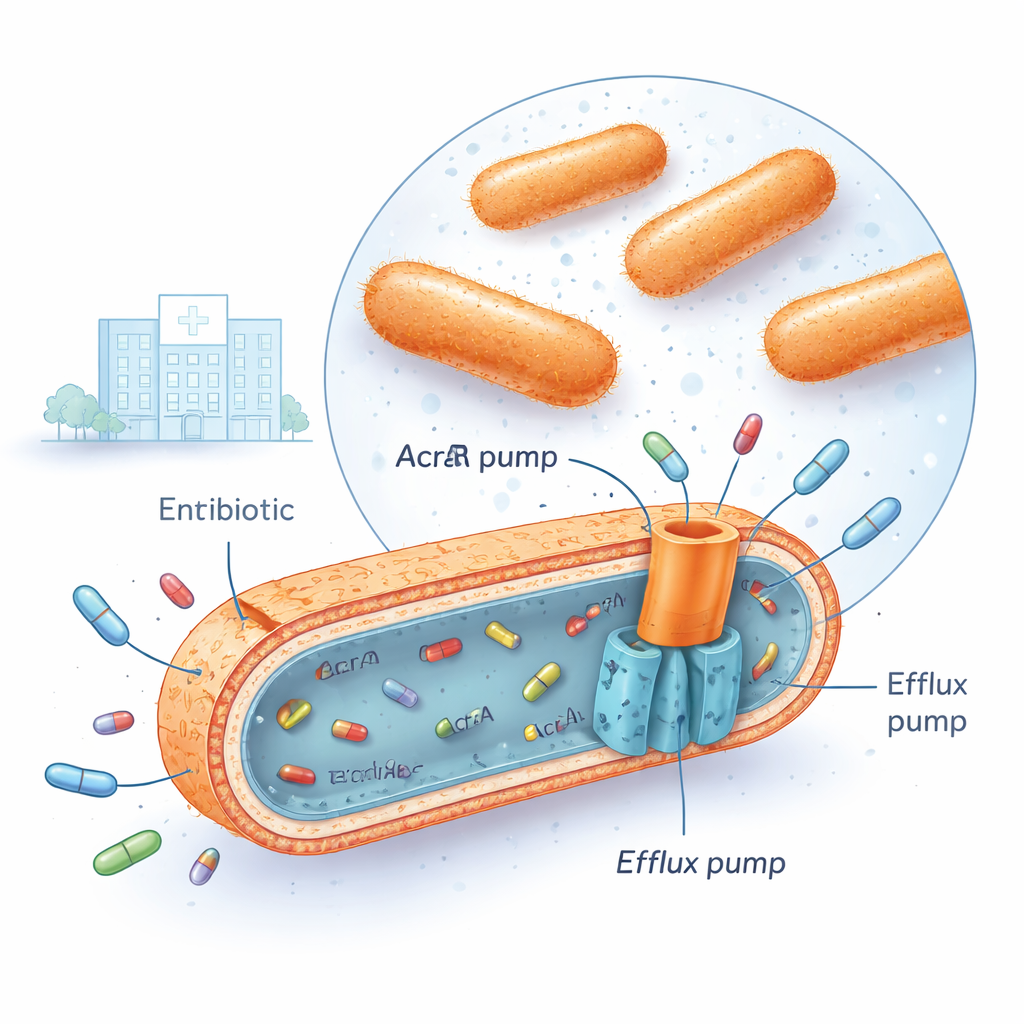
伴随泵过度驱动的基因开关
研究者收集了30株多药耐药临床分离株的克雷伯氏肺炎菌,并与10株对抗生素敏感的分离株以及一个标准参考菌株进行比较。利用定量实时 PCR(qRT‑PCR)技术,他们测量了若干基因的表达水平。他们关注三种“全局调控因子”——名为 marA、soxS 和 rob 的基因——以及 AcrAB‑TolC 泵的三个组成部分(acrA、acrB 和 tolC)。在耐药菌株中,两种调控因子 marA 和 soxS 通常升高约四到五倍,而作为核心泵组成的 acrB 几乎提高了八倍。统计分析显示,当 marA 和 soxS 水平较高时,acrB 水平通常也较高,这些菌株往往能耐受更高剂量的氟喹诺酮类抗生素(如环丙沙星)。第三种调控因子 rob 变化不大,且与泵的活性没有一致关系,提示在所测条件下其作用较小。
关闭外排泵以削弱耐药性
发现泵和调控基因共同活跃具有提示性,但不足以证明它们确实驱动了耐药性。为检验外排泵的功能重要性,研究团队使用了一种名为 PAβN 的化学工具。该化合物并不用于临床治疗,但在实验室中它可阻断类似 AcrAB‑TolC 的泵,阻止其将抗生素排出。研究者选择了十株 acrB 表达特别高的耐药分离株,测定在有无 PAβN 情况下阻止其生长所需的环丙沙星剂量。在这十株中,有八株在阻断外排泵后所需的环丙沙星剂量至少降低了四倍,有时甚至降低了十六倍。该下降表明,在许多这些超级细菌中,活跃的外排泵确实是它们能耐受高剂量抗生素的主要原因之一。
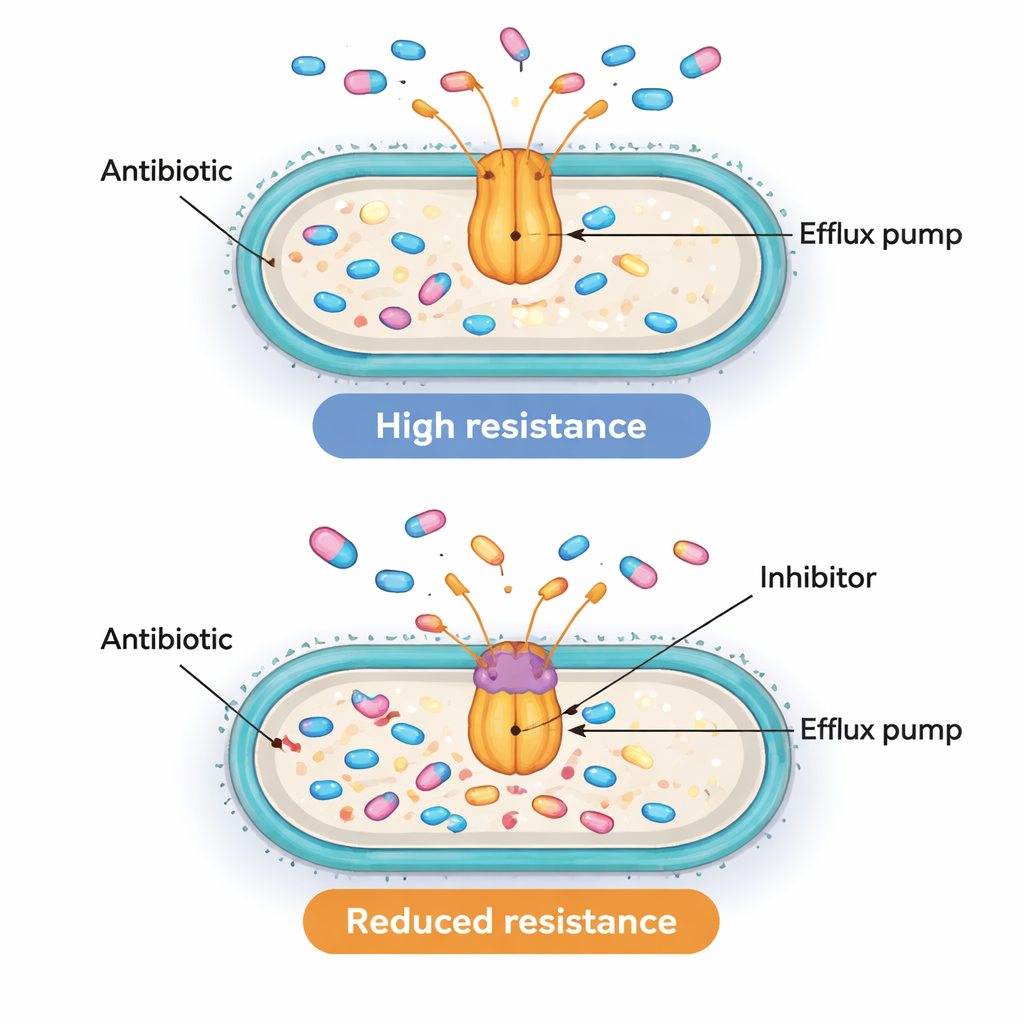
复杂的耐药拼图与有希望的靶点
并非所有菌株的表现都相同。一些高表达外排泵基因的细菌在阻断泵后仅部分恢复敏感性,这暗示还有其他耐药途径在发挥作用——例如抗生素靶位的改变、产生破解药物的酶或其他替代外排泵等。以氨基糖苷类抗生素庆大霉素为例,其敏感性在很大程度上并未随 marA/soxS 与 AcrAB‑TolC 基因模式的变化而改变,这强调了多药耐药通常是由若干重叠防御机制共同构成的,而非单一机制。
这对未来治疗的意义
对非专业读者而言,核心信息是某些医院细菌能通过主动将抗生素排出体外而生存,不仅仅是阻止药物进入或将其分解。该研究将两种基因“开关”MarA 和 SoxS 的高表达与更活跃的外排泵及对一种广泛使用抗生素类别的更强耐药性联系起来。当实验上堵塞这些泵时,许多菌株至少部分恢复了敏感性。尽管研究尚未确切证明这些开关如何控制泵的具体机制,但它强调了这些调控因子和外排泵作为有吸引力的干预靶点。长期来看,将传统抗生素与安全的泵抑制剂——或能下调这些全局调控因子的药物——联用,可能有助于恢复现有疗法对令人畏惧的多药耐药感染的疗效。
引用: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
关键词: 抗生素耐药性, 外排泵, 克雷伯氏肺炎菌, 氟喹诺酮, 耐药性逆转