Clear Sky Science · zh
使用带脂质‑PEG 锚定的荧光蛋白指示剂成像细胞间生物分子
实时观察细胞间的对话
我们的脑和身体依赖于细胞之间持续不断的化学交流。离子和神经递质在极小的间隙中传递信息,但这些快速且短暂的信号很难在不干扰它们的情况下被观察到。这项研究提出了一种简单方法,用能附着在细胞外表面的发光传感器“涂”活细胞,使科学家可以实时、细致地观察这些信息——尤其是钾离子和神经递质谷氨酸。 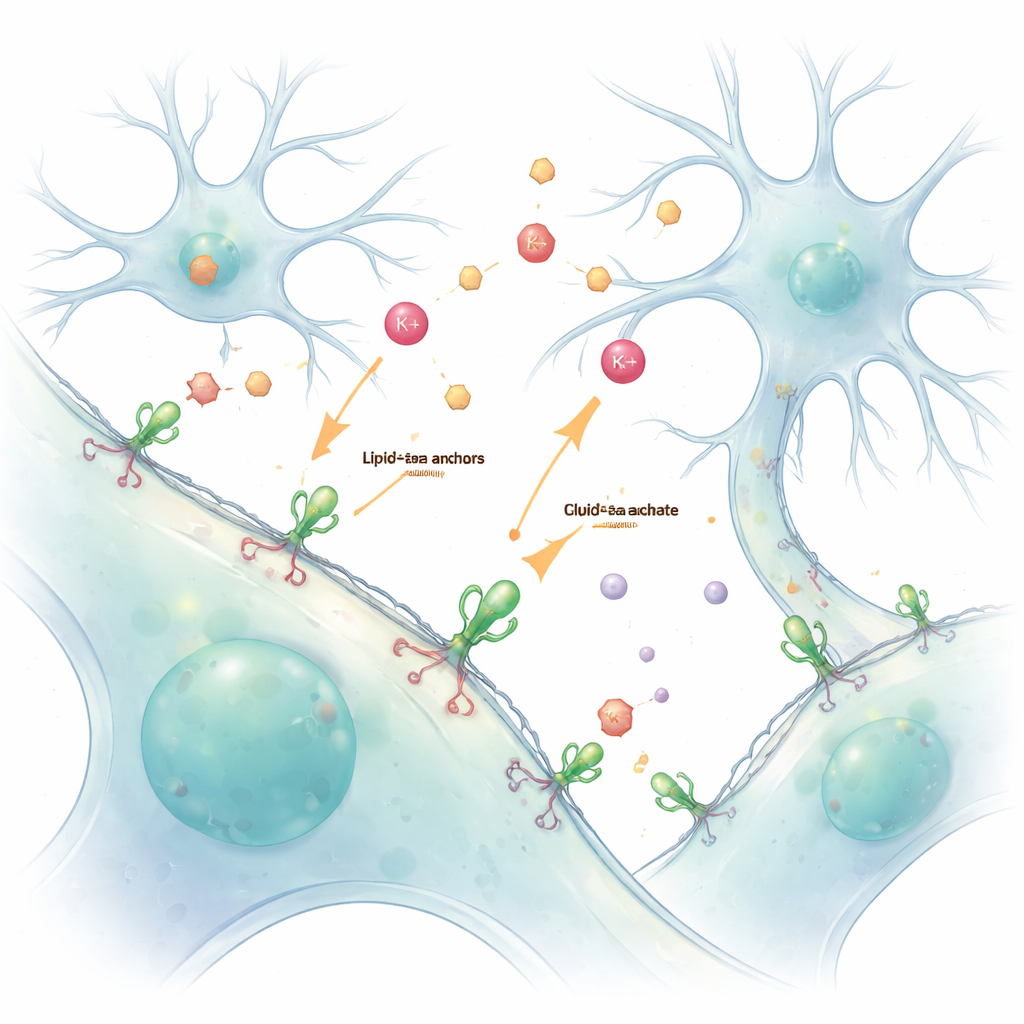
一种新的细胞表面标记方法
传统上,研究人员通过基因工程让细胞自身表达荧光蛋白传感器。虽然这种方法很强大,但常常会把传感器放在细胞内部,从而难以区分细胞内外发生的事情。作者通过使用一种称为脂质–PEG 锚的化学手柄解决了这一问题。该分子的一端嵌入外膜,而另一端通过化学键连接到荧光蛋白传感器。当这些制备好的传感器被直接加入活细胞时,它们会自发地覆盖细胞外表面,形成稳定的发光层,报告周围液体中的变化。
将钾和谷氨酸变成可视化信号
研究团队改造了两种现有的荧光指示剂:响应钾离子的 GINKO2 和响应谷氨酸的 R‑iGluSnFR1。他们从细菌中提纯这些蛋白,然后将脂质–PEG 锚连接到它们。在培养的人类细胞中,锚定的钾传感器在细胞表面形成了平滑的轮廓,当细胞外钾增加时变亮,钾水平下降时又变暗。重要的是,其发光特性和灵敏度在试管实验中与原始未改造的传感器非常接近,表明锚定并未削弱其性能。谷氨酸传感器也表现类似,锚定后仍能响应,并清晰地标出细胞外的谷氨酸分布。
在培养与切片中监听神经元
随后,研究人员将方法应用于小鼠海马的神经细胞——该脑区在学习和记忆中至关重要。他们用脂质–PEG 锚定的谷氨酸传感器包覆这些神经元,并在同一细胞内装载了另一种报告电活动的钙染料。利用全内反射显微镜,他们能够同时看到位于细胞表面的谷氨酸红色闪光和细胞内部表示放电的绿色信号。这种双色视图表明,锚定的传感器可以在不对神经元进行任何基因改造的情况下,追踪自发的神经递质释放。
在脑组织中绘制化学波传播图
接着,团队在保持海马自然连线的急性脑切片中测试了该方法。他们将锚定的钾传感器应用于切片,并对神经纤维进行电刺激。锚定传感器在每次刺激后产生清晰且可重复的荧光增加,而未锚定的传感器则迅速扩散并产生微弱、不稳定的信号。通过在已知钾浓度的溶液中浸泡切片并校正组织本身的微弱荧光,作者建立了标定曲线并估算了实际的细胞外钾浓度。基线水平约为2.5毫摩尔,适度刺激后升至约3.4毫摩尔,与传统电极测量一致。针对钾和谷氨酸的锚定传感器显示这些信号的扩散方式不同:谷氨酸的变化局限于活跃突触附近,而钾的增加则扩展到数百微米,暗示其对网络兴奋性的更广泛影响。 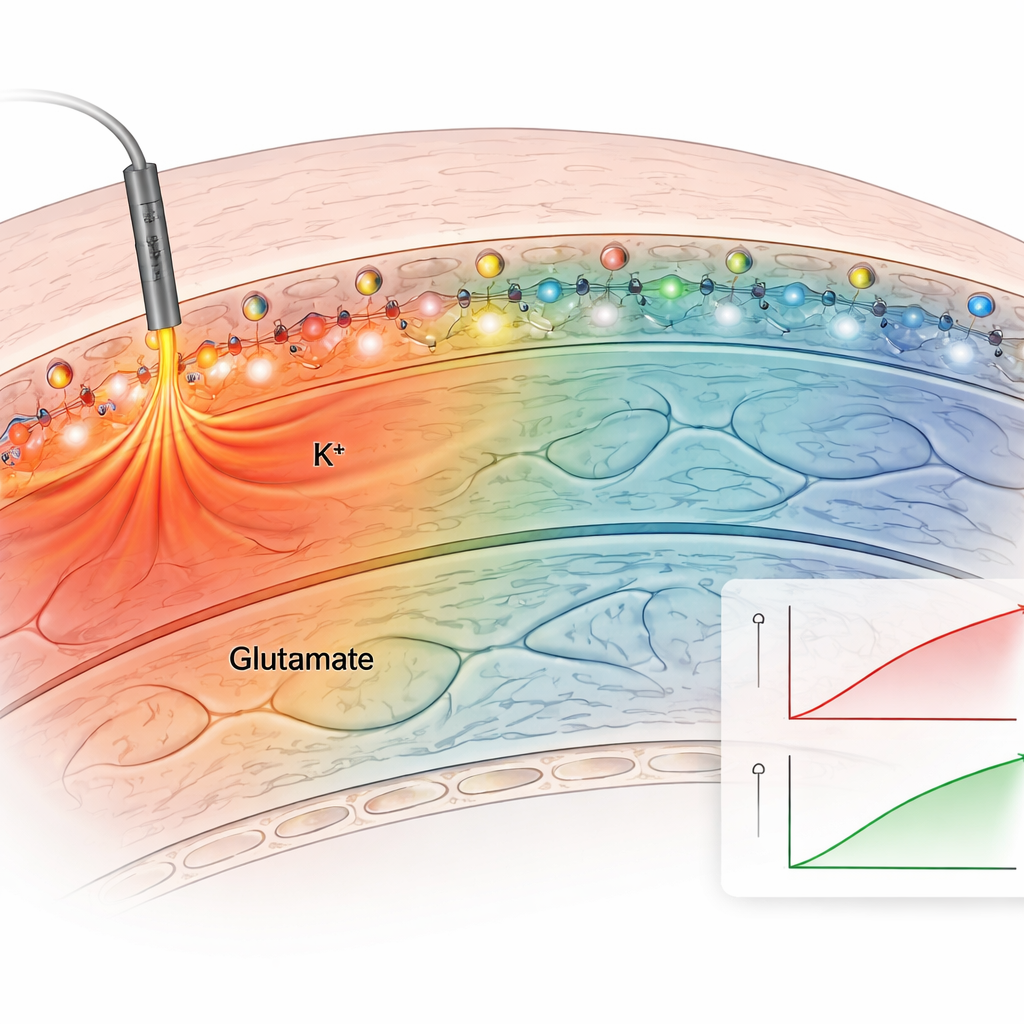
探查大脑如何清除与产生信号
由于传感器被固定在细胞表面,作者得以剖析哪些过程塑造这些细胞外波动。阻断通常清除谷氨酸的转运体,会使锚定的谷氨酸传感器显示更大且持续时间更长的信号,证实局部再摄取限制了谷氨酸的扩散。阻断 AMPA 型谷氨酸受体会减少电响应和钾信号,表明大部分钾升高来自受突触输入激活的突触后神经元。用四氟甲烷毒素(TTX)阻断钠通道几乎消除了钾的变化,将其直接关联到动作电位。总体上,这些实验说明锚定传感器能把复杂的、分布式的化学过程转化为直观的影片和地图。
这对未来脑研究的意义
对于非专业读者,关键结论是:这项工作提供了一种快速的、非基因学的方法,可以用高灵敏度的分子报告器涂覆活细胞和组织。研究人员无需对每种细胞类型做基因改造,而是可以从外部添加预制的传感器蛋白,立即可视化细胞表面离子和神经递质的实时变化。这种方法提高了可控性、可重复性和空间精度,同时避免了基因传递带来的挑战,尤其是在像急性脑切片这样敏感的准备中。随着更多针对不同化学物质的荧光指示剂被开发,脂质–PEG 锚定策略有望成为观察全身细胞化学语言的广泛工具包。
引用: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
关键词: 细胞外信号传递, 荧光生物传感器, 谷氨酸成像, 钾离子动态, 海马神经元