Clear Sky Science · zh
人类酪氨酸蛋白硫酸转移酶2(TPST2)中金属结合的结构表征
为何微小的金属离子对细胞信号至关重要
在细胞内部,无数分子机器默默调节组织生长、激素作用和免疫细胞间的通信。其中一种机器——名为TPST2的酶,会在蛋白质经过细胞的“运输中心”高尔基体时,给特定蛋白加上一个微小的硫酸基标签。本研究揭示了像钠和锰这样简单的金属离子如何通过微妙地使酶结构的部分区域变得更为僵固来提升TPST2的活性——这一发现可能将细胞内的矿物质平衡与癌症及激素相关疾病联系起来。 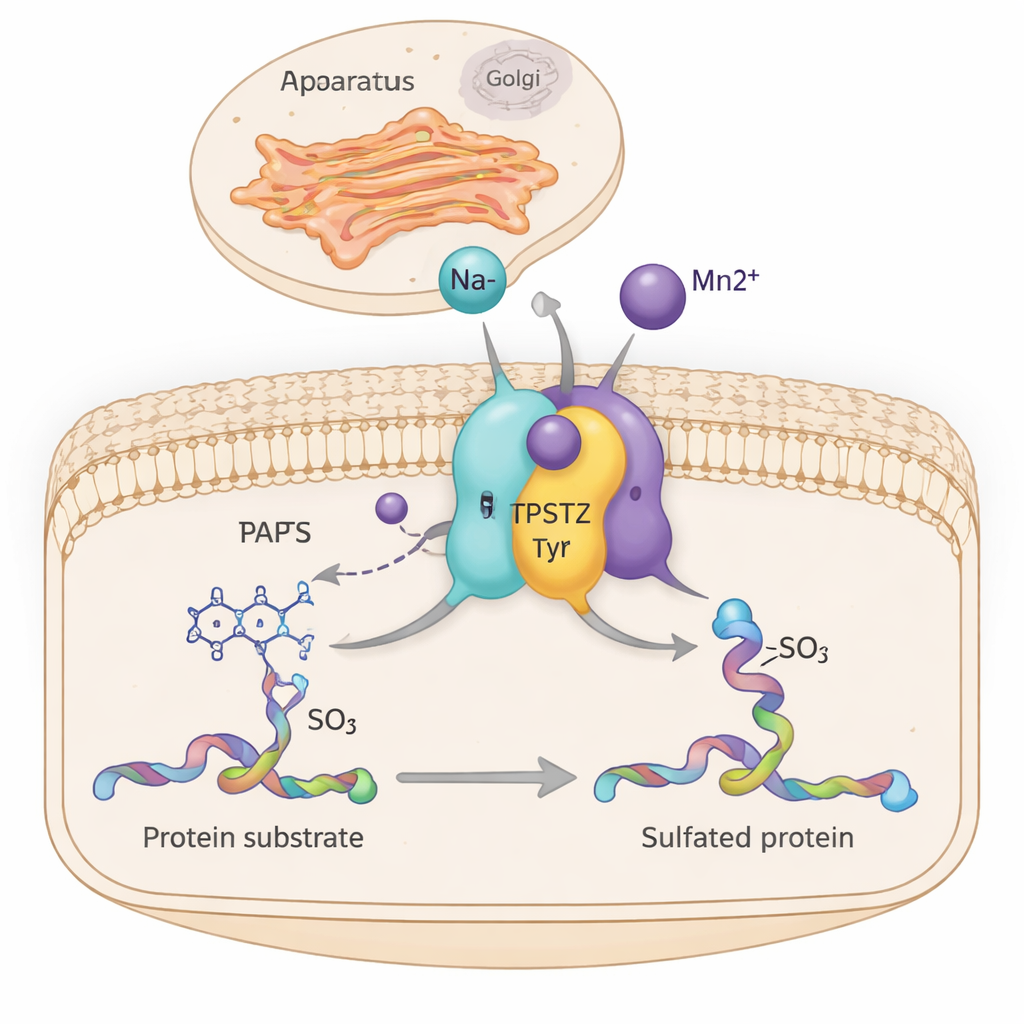
为其他蛋白“装饰”的一种酶
TPST2属于一类进行“酪氨酸硫酸化”的酶,这是一种被添加到蛋白质特定酪氨酸残基上的化学修饰。被硫酸化的蛋白在细胞外发挥关键作用,影响血液凝固、白细胞迁移、激素与受体的结合,甚或病毒进入细胞的方式。人体中主要有两种硫酸化酶——TPST1和TPST2,它们位于高尔基体膜上,在蛋白质准备被分泌时对其进行修饰。小鼠研究表明,失去TPST2会扰乱甲状腺激素的产生、抑制生长并导致雄性不育,突显了其对正常生理的重要性。
与癌症与免疫逃逸的关联
近期研究已将TPST2与疾病直接联系起来。在黑色素瘤中,TPST2修饰干扰素受体的一个组分,从而削弱免疫信号;阻断TPST2可增强针对PD-1的免疫检查点疗法的效果。在胰腺癌中,依赖于TPST2的通路帮助稳定一种促进肿瘤生长与转移的蛋白(整合素β4)。在这些模型中抑制TPST2可减缓癌细胞的增殖与侵袭。由于TPST2作用于细胞表面的蛋白,它有效地重绘了细胞感知与响应周围环境的方式,因此成为有吸引力的潜在治疗靶点。
发现金属的“开启开关”
生物化学家早已知道当存在二价金属如锰(Mn²⁺)时,TPST2的活性会大幅提升,但其结构学上的原因尚不清楚。在这项研究中,作者制备了人TPST2的催化核心并与反应副产物以及钠(Na⁺)或锰共同结晶。通过高分辨率 X 射线晶体学,他们发现酶内存在两个小的金属结合位点,每个位点周围原子的排列呈规整的六配位(八面体)结构。通过调节 X 射线波长以利用不同金属的特征吸收,他们确认Mn²⁺优先占据这些位点,而锌或铜等金属则要么在其他位置弱结合,要么根本不结合。
不是重塑整体,而是“加固”关键可动部分
出人意料的是,含钠的TPST2与含锰的TPST2在整体外观上几乎相同;并没有发生显著的张开或闭合。相反,金属主要影响的是通向活性位点入口处的两段柔性区域:一段称为α3的螺旋和一条邻近的α12–α13回圈。在无金属或结合松散的状态下,这些片段会摆动并部分无序。当Na⁺结合时,它们变得更有序;而Mn²⁺则进一步锁紧这些区域,X 射线数据中显示热运动降低,计算机的柔性分析也支持这一点。这种额外的僵固使酶的熔融温度略微升高,被认为会降低组织活性位点所需的“熵代价”——从而更容易、更快速地将底物引导到适合硫酸化的位置。 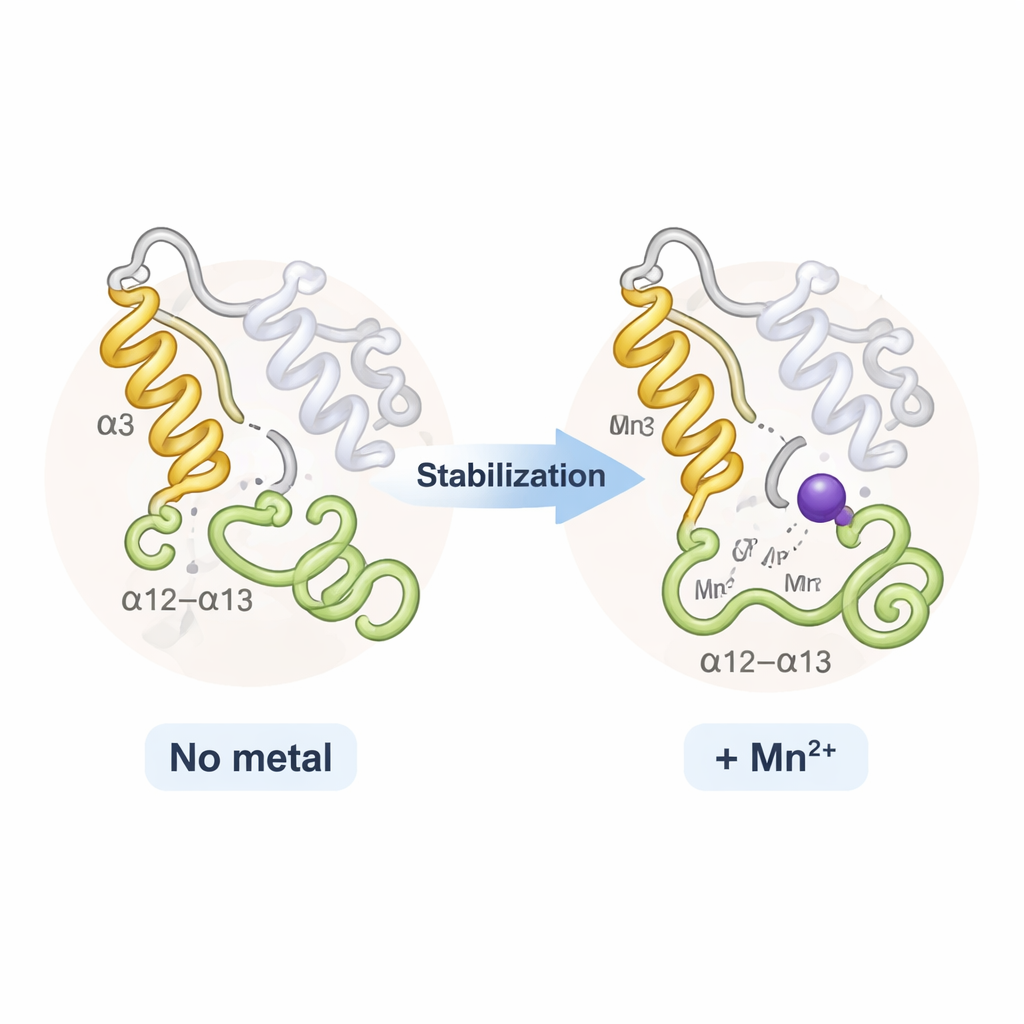
从细胞矿物质到信号控制
作者提出了一种“通过有序化激活”的模型。在无金属结合时,TPST2在其活性位点入口处较为松散且效率低下。细胞中丰富的钠可以结合这些位点,产生一种部分有序、活性适中的状态。而在高尔基体内以微摩尔量严格调控存在的锰,则结合得更牢固,将关键区域锁定到最佳排列状态,从而最大化催化效率。这提示高尔基体中锰含量的微小变化可能会调节TPST2对其底物的修饰强度。鉴于TPST2影响激素生成与癌症信号传导,此项工作强调了金属离子平衡、蛋白质“装饰”与疾病之间的潜在联系,并为通过模仿或破坏金属结合来调节TPST2活性的药物设计提供了结构学框架。
引用: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
关键词: 酪氨酸硫酸化, TPST2, 锰, 高尔基体, 蛋白质修饰