Clear Sky Science · zh
基于注意力融合与 EAOO-GA 优化的可解释混合集成用于肺癌检测
为何及早发现肺癌对所有人都至关重要
肺癌是致死率极高的癌症之一,主要原因在于常常在病情已晚、治疗选择受限且存活率骤降时才被发现。医生越来越依赖 CT 扫描和计算机程序,在症状出现之前识别肺部可疑病灶。本文提出了一种新的人工智能(AI)系统,旨在使计算机诊断不仅更准确,而且更可靠、更易为临床医生理解。
计算机如何解读肺部扫描
现代 AI 系统可以扫描 CT 图像并学习区分良性结节与危险肿瘤的模式。这些基于深度神经网络的系统已在狭窄任务上展现出可与甚至超越人类专家的能力。但在真实医院环境中它们面临三大难题:可能对单一数据集过拟合而在新患者上失效、在某些病种稀少时难以处理不平衡数据、以及常以不透明的“黑箱”形式运行让临床人员难以信任。作者针对一个常用的肺部 CT 数据集展开研究,该数据集包含三类病例:良性结节、恶性结节和正常扫描。
多位专家而非单一模型
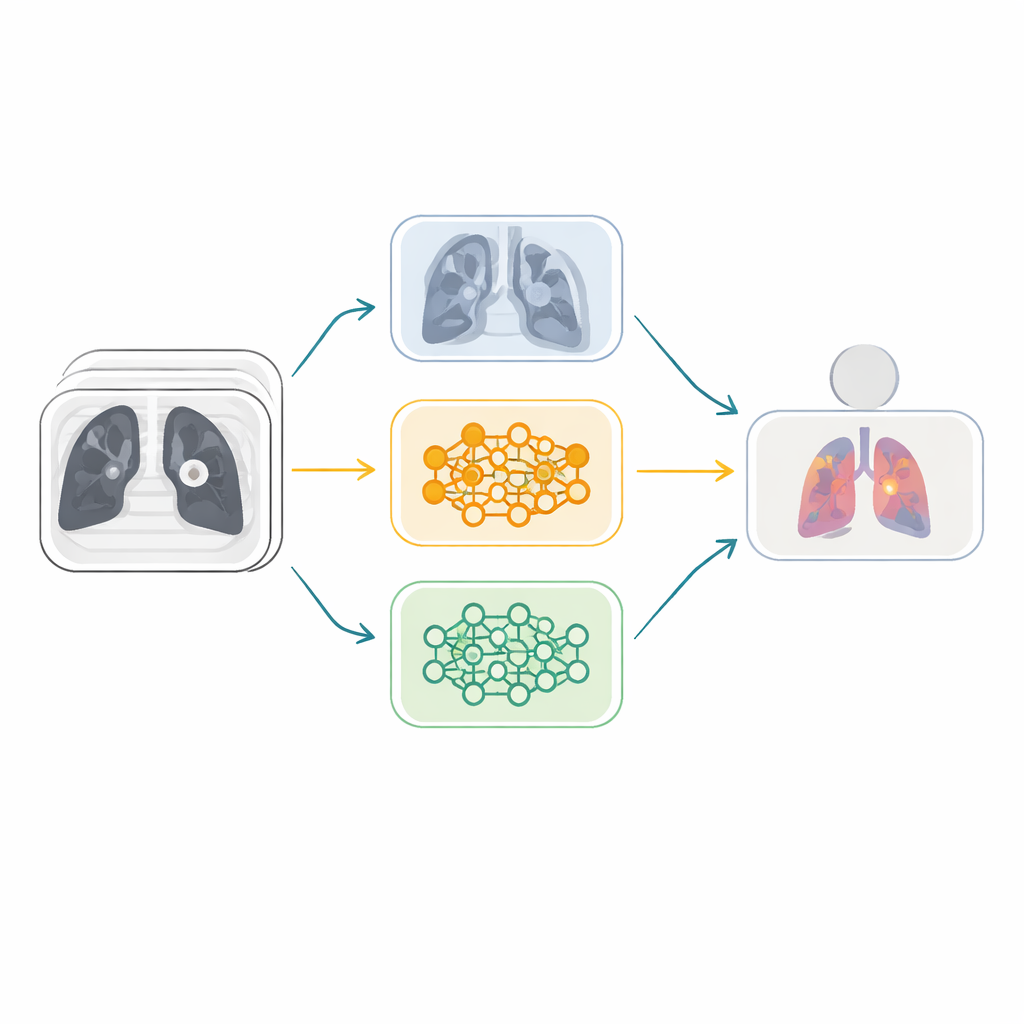
研究人员没有依赖单一神经网络,而是构建了一个集成——由多种 AI 模型组成的团队共同投票。研究从六种强大的图像识别架构出发,这些架构最初在数百万张日常照片上训练,然后被调整用于肺部 CT。随后将这些模型配对为三条“融合”分支,每条分支结合两种互补优势的网络。在每个分支内部,一种称为 Squeeze-and-Excitation 的注意力机制学习哪些内部特征通道携带最有用的视觉线索(例如细微纹理或结节形状),并增强这些通道同时弱化信息量较小的模式。这有助于系统聚焦于医学上有意义的细节,而非噪声。
用自然启发的搜索来优化团队配比
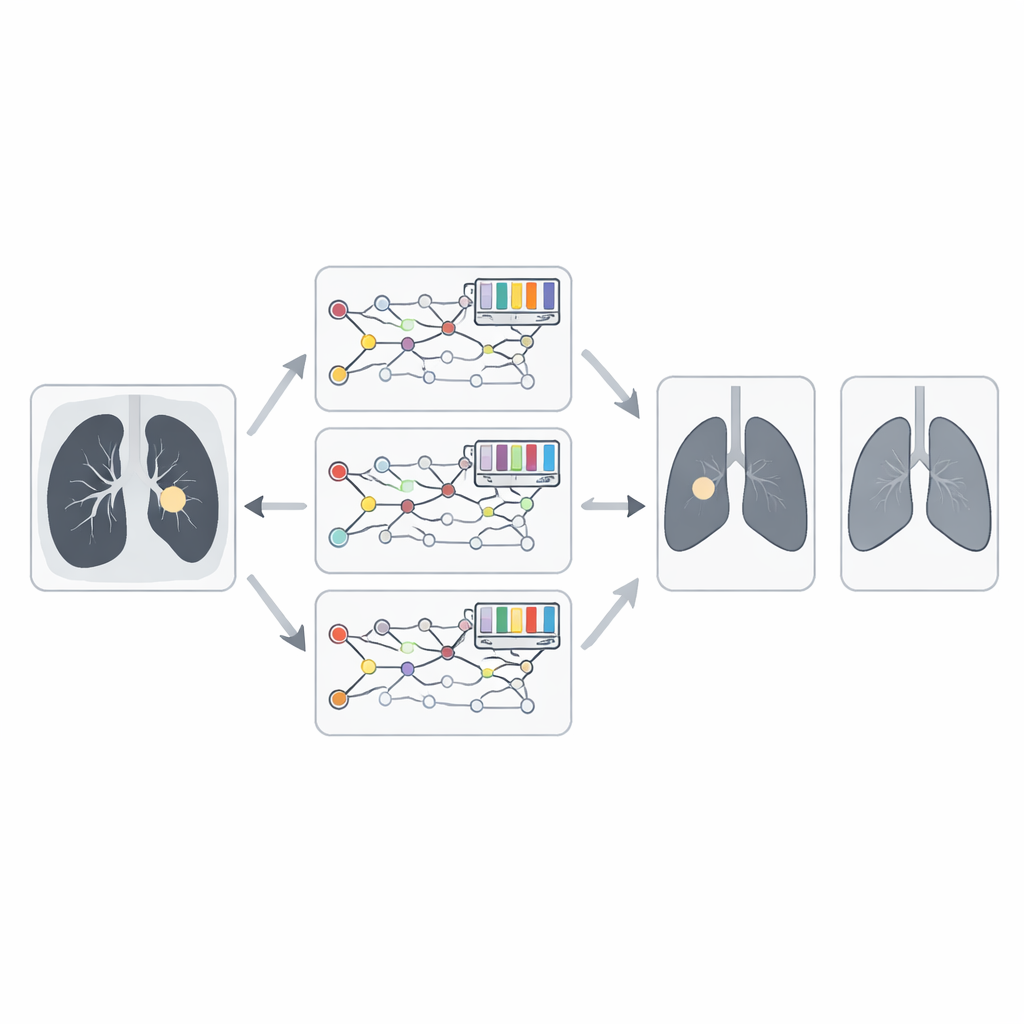
简单平均三条强分支的意见仍有改进空间。本工作的关键思想是让一种受自然启发的优化器决定每条分支应给予多少权重。团队引入了增强版的 Animated Oat Optimization 算法,并加入了类似遗传操作的交叉与变异。通俗地说,该算法将候选权重组合作为一个种群,反复“演化”它们,保留那些能带来更准确信息的个体并重排其余者。经过多次迭代,它会发现一种有效的平衡,使得更可靠的融合模型在最终诊断中占更大比重。
平衡少见病例并打开黑箱
真实的医学数据中恶性样本往往远多于良性或正常样本,这会使 AI 系统偏向过度判定癌症。为应对这一点,作者使用名为 SMOTE 的技术为不足类别生成额外的合成样本,从而平衡训练分布。他们还加入了一个解释层,使用 Grad-CAM 生成热图,显示对每个决策影响最大的图像区域。对于恶性病例,凸显区域通常与不规则、放射状的结节相吻合;对于良性或正常扫描,关注点则转向更平滑的组织。这有助于放射科医生核验模型是否关注正确的结构而非无关伪影。
系统在真实世界数据上的表现如何
在 IQ-OTH/NCCD 肺癌数据集上的测试表明,该集成达到约 99.4% 的惊人准确率,同时具有同样较高的精确度、召回率和 F1 分数。它持续超越所有单一网络、更简单的融合方案以及多种其他优化方法。关键是,作者还在一个常用的外部 CT 集合 LIDC-IDRI 上验证了模型,那里它仍维持接近 98% 的准确度。该外部测试表明系统超越了最初训练图像的泛化能力,这对于旨在跨不同医院和扫描设置辅助临床工作的工具至关重要。
这对患者和临床医生意味着什么
对外行人而言,最重要的结论是:将数个 AI“专家”结合起来、细致调整它们的协作方式并使其推理更透明,能够显著提升基于 CT 扫描的早期肺癌检测。本文提出的框架将原始图像转化为放射科医师的高准确度且相对可解释的第二意见。如果在临床试验中得到进一步验证并适配到日常医院流程,此类系统有望更早发现危险肿瘤、减少不必要的随访检查,并最终改善肺癌高危人群的生存率与生活质量。
引用: Al Duhayyim, M., Aldawsari, M.A., Ismail, A. et al. Interpretable hybrid ensemble with attention-based fusion and EAOO-GA optimization for lung cancer detection. Sci Rep 16, 8159 (2026). https://doi.org/10.1038/s41598-026-37187-6
关键词: 肺癌检测, CT 扫描分析, 深度学习集成, 医学图像人工智能, 可解释诊断