Clear Sky Science · zh
利用光物理学与计算方法探究五价磷-科罗尔与血红蛋白的结合机制
在血液中搭载的光激活药物
许多新一代癌症疗法依赖于只有在特定光照下才会发光或变得有毒的特殊染料。其中一类被称为科罗尔的染料,有望在杀伤肿瘤细胞时减少副作用。但在将此类试剂安全用于人体之前,科学家必须弄清它如何在体内运输,尤其是它如何与我们血液中主要的载氧蛋白——血红蛋白相互作用。本研究正是探讨一种新的基于磷的科罗尔如何与人血红蛋白结合,以及这对将血液蛋白作为天然药物载体意味着什么。 
血液载氧蛋白的新伙伴
血红蛋白被包装在红细胞内,将氧气从肺输送到各个器官,并将二氧化碳带回排出体外。由于它含量丰富且具有许多小分子可以嵌入的口袋和表面,血红蛋白也能结合药物并影响它们在体内的循环时间。科罗尔是与血红蛋白内的血红素相关的环状色素分子,但可以通过化学修饰来实现成像、抗感染或利用光破坏癌细胞等医疗功能。研究者集中研究了一种专门设计的五价磷科罗尔,称为1P,因其稳定性、强吸光性以及产生光动力疗法所需活性氧的能力而被选中。
用光观察分子对话
为验证1P是否真的与血红蛋白结合,团队首先采用了光学技术。通过对含有不同浓度1P的血红蛋白溶液照射紫外和可见光,他们追踪了蛋白特征吸收峰的细微位移。这些变化表明1P与血红蛋白在基态形成了稳定复合物,而不仅仅是短暂碰撞。荧光实验(测量血红蛋白中特定氨基酸的天然发光)显示,这种发光以一种最能由1P在这些发光残基附近形成紧密复合物来解释的方式被淬灭。根据不同温度下的淬灭程度,科学家们计算出相当大的结合强度和负的吉布斯自由能,说明在类似生理条件下该相互作用自发且在能量上是有利的。
结合如何推动蛋白构象变化
由于药物结合会轻微重塑蛋白,研究者接着用圆二色谱法检查了血红蛋白的结构,该方法能够读取蛋白螺旋和卷曲结构对旋光的吸收。加入更多1P会略微降低与血红蛋白螺旋含量相关的信号,表明局部结构有所松动但并未完全崩溃。当他们加热有无1P的血红蛋白时,含1P的复合物在稍低温度下开始展开,亦指向轻微的去稳定化。这些结果表明,1P嵌入在关键结构区域附近——足以调节蛋白的稳定性及血红素周围环境,但不足以破坏血红蛋白的整体架构或功能。 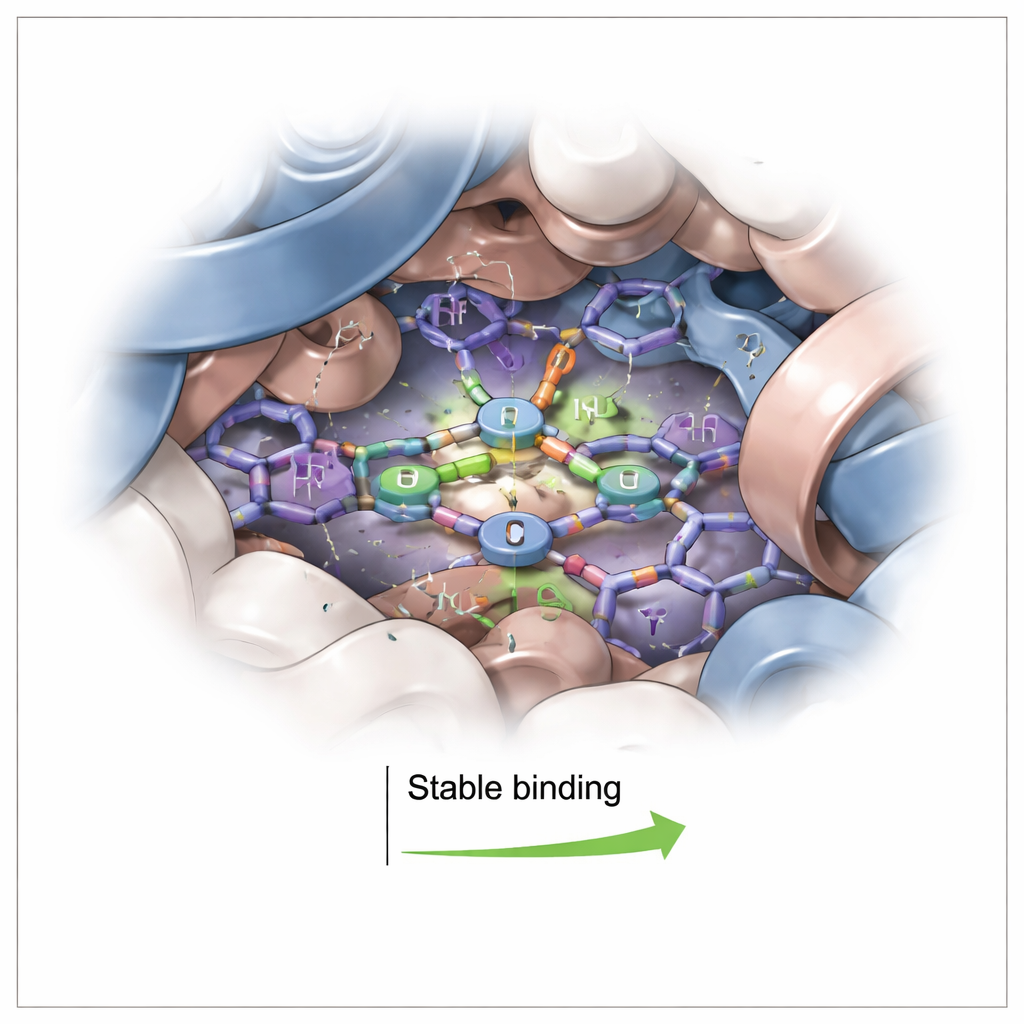
计算模拟揭示“就座”位置
为可视化1P的确切位置,团队转向计算建模。他们将1P对接到一份高分辨率的人类血红蛋白结构上,然后在水环境中对该复合物进行了100纳秒的模拟。模拟显示1P落入一个芳香性口袋,距离血红素约十亿分之一米,但并未直接与铁中心结合。相反,科罗尔扁平的环状表面与附近芳香族氨基酸发生堆积,间或由氢键加以稳固。在整个模拟过程中,血红蛋白的整体构象和1P的位置都保持得相当稳定。能量计算证实了结合是高度有利的,其驱动力主要来自紧密堆积与疏水接触,而非仅靠强烈的静电吸引。
对未来光驱动药物的意义
综合这些实验和模拟结果表明,五价磷科罗尔1P能紧密且特异地与人血红蛋白结合,形成一个仅对蛋白结构有温和影响的稳定复合物。通俗地说,1P在血红蛋白上找到一个舒适的位置,而不会挤掉其重要的血红素组分。这使得血红蛋白成为通过血流输送科罗尔类药物的有前景的天然搬运工具,可能改善它们在体内的循环时间及到达病灶的效率。通过澄清1P的结合位置与方式,这项工作为设计更安全的光激活药物奠定了基础,能够利用我们的血液蛋白作为内建载体。
引用: Kritika, Kubba, R., Kumar, L. et al. Probing into the binding mechanism of phosphorus(V)-corrole with hemoglobin using photophysical and computational approach. Sci Rep 16, 6097 (2026). https://doi.org/10.1038/s41598-026-37177-8
关键词: 血红蛋白 药物运输, 光动力疗法, 科罗尔 光敏剂, 蛋白配体 结合, 分子对接