Clear Sky Science · zh
多模态影像评估糖尿病中缺氧骨髓微环境与H型血管损伤
为何糖尿病中的骨骼健康至关重要
人们通常把1型糖尿病与血糖和胰岛素联系在一起,但该病也在悄然重塑骨骼。许多患者会出现骨强度下降,骨折风险增加,即便骨密度检测结果看上去几乎正常。本研究利用先进的医学影像技术在糖尿病模型兔的骨髓深处观察微小血管和氧含量的变化,旨在揭示这些隐匿损伤的发生过程。理解这些变化有助于实现更早的诊断并开发保护糖尿病患者骨强度的新疗法。
骨内隐秘的血液通道
在胫骨等长骨内部,存在一片丰富的血管网络,这些血管不仅为骨组织供养,还引导其生长与修复。其中一类特殊血管被称为“H型”血管,聚集在骨端邻近的区域,那儿有生长板和活跃的骨重塑过程。这类血管携带较高的氧含量,并与新骨形成密切相关。然而在1型糖尿病中,长期高血糖产生的化学副产物与氧化应激可能扰乱这一精细调控系统。研究者旨在在活体动物中可视化这些变化如何在骨的不同区域展开。
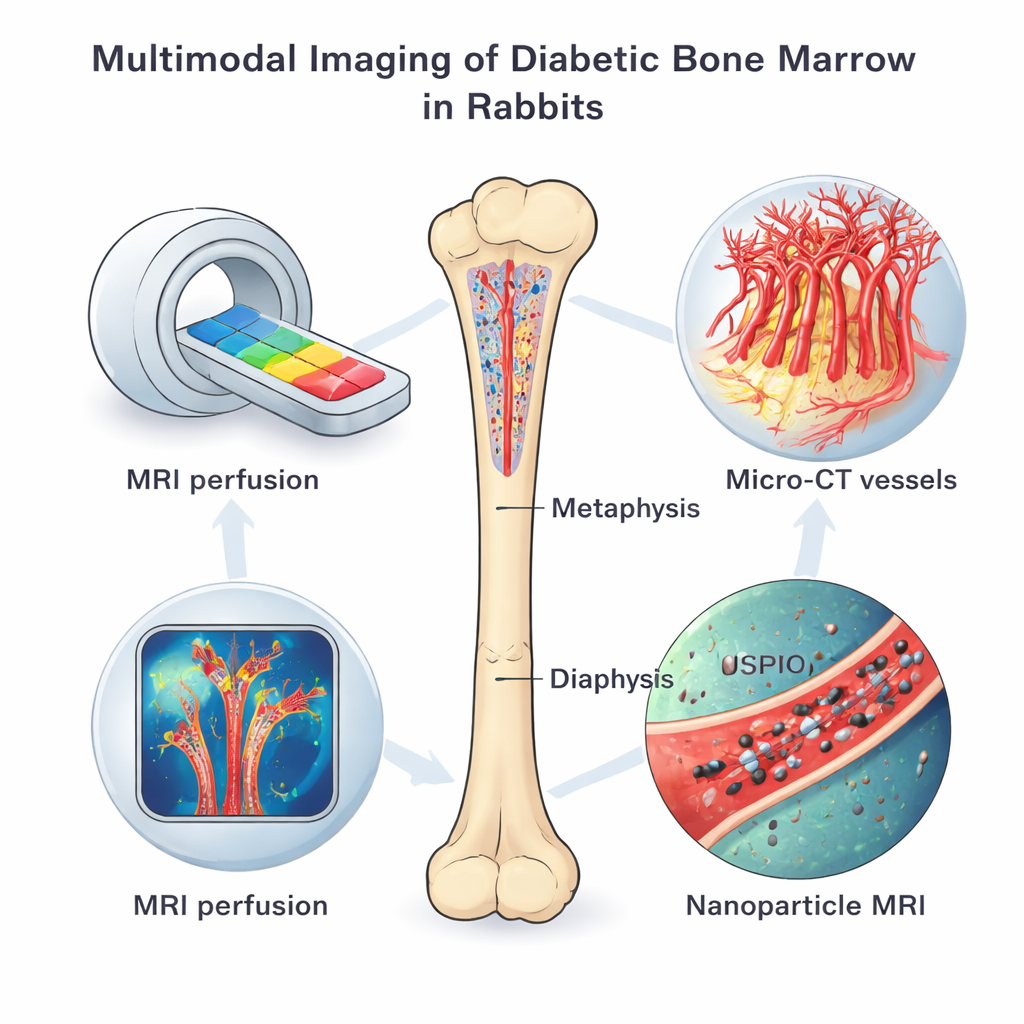
从多角度扫描活体骨组织
研究团队对化学诱导产生1型糖尿病的兔子和健康对照组进行了多种影像学检查,所有动物均在确立糖尿病四个月后成像。动态对比增强磁共振成像(DCE‑MRI)跟踪了造影剂在骨髓中的进出速率,揭示微小血管的灌注情况及通透性。另一种借助铁基纳米颗粒的MRI技术显示了血管内皮细胞对颗粒的摄取活性,这是代谢和血管行为改变的标志。动物安乐死后,采用高分辨率微型CT绘制了微血管的三维网络,而荧光染色、基因检测与电子显微镜则在细微层面检查了血管类型、氧感应蛋白和细胞损伤。
糖尿病在骨内最严重打击的部位
在所有影像手段中,糖尿病兔的骨髓血管均表现出比健康动物更高的通透性和异常性。造影剂流动更快且停留时间更长,铁纳米颗粒的摄取更为显著,尤其集中在富含H型血管的骨端(干骺端)。微型CT显示,糖尿病骨骼的小血管数量明显减少,总血管体积下降,以至于骨端通常优于骨干的优势消失。流式细胞术与荧光标记证实,H型血管的比例在糖尿病中显著降低,沿生长板的新生血管也变得稀少。简言之,通常支持强健骨形成的血管小环境被选择性地变薄和损伤。
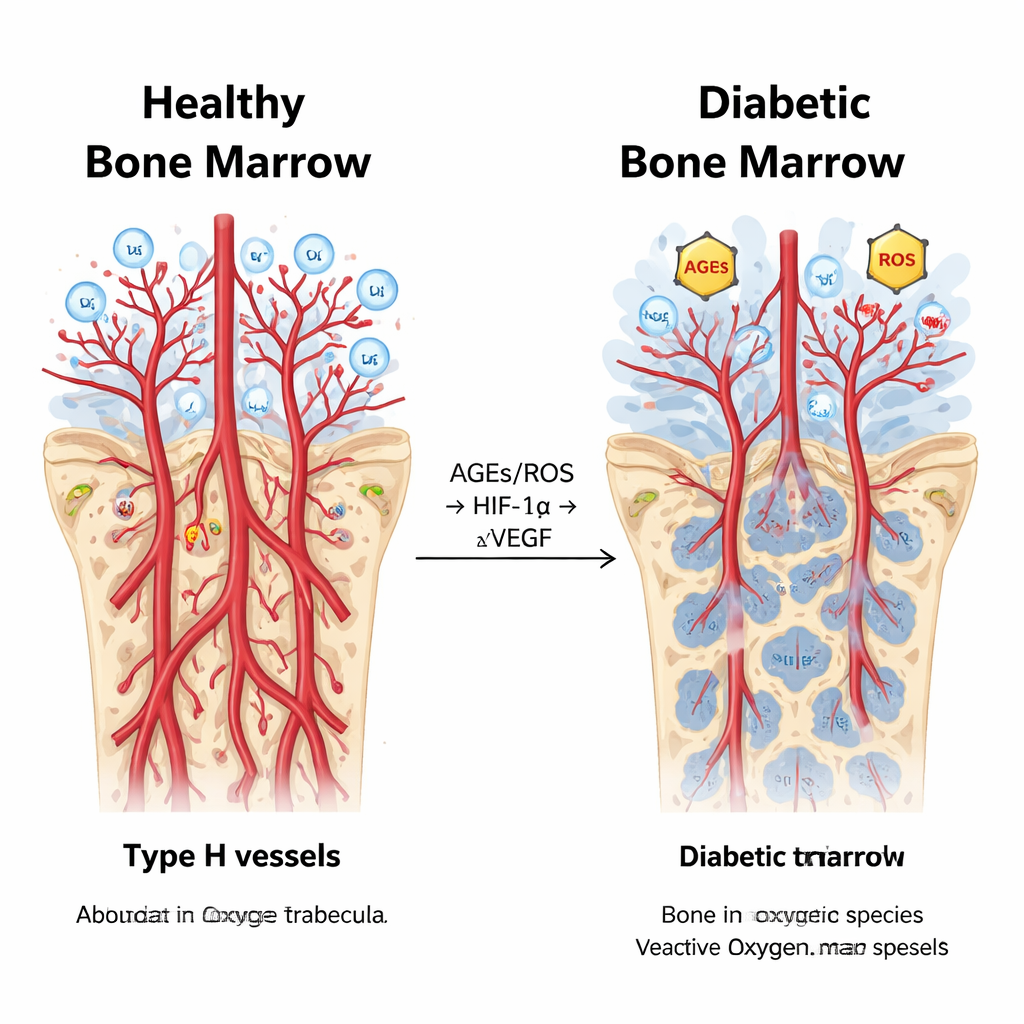
糖尿病骨髓内的复杂化学级联反应
进一步分析中,科学家测量了与缺氧(氧气不足)及高血糖驱动的氧化应激相关的分子。糖尿病兔表现出更高的晚期糖基化终产物(AGEs)和活性氧(ROS)水平,以及氧感应蛋白HIF‑1α及其受体配对分子AGER在干骺端的增强活性。令人意外的是,尽管HIF‑1α通常促进血管生成,但关键的促血管生长因子VEGF在糖尿病骨髓中反而受到抑制,血管萌芽减少。统计分析将这些线索联系起来:氧化应激标志物与异常灌注指标的变化与HIF‑1α同步上升,而VEGF及血管密度指标则呈相反趋势。这一模式表明,在慢性糖尿病中,正常的“缺氧报警”系统被异化,驱动炎症和血管渗漏,而非健康的新血管与新骨形成。
这对糖尿病患者意味着什么
简而言之,本研究表明糖尿病并非以均匀方式削弱骨骼;它在本应最坚固和最具再生能力的部位制造斑块状的血管损伤和低氧“热点”。通过将多种影像方法结合,研究者既观察到了功能上的血管渗漏,也看到了H型血管的结构性丧失,并将这些改变与包含AGEs、ROS、HIF‑1α和VEGF的特定化学通路关联起来。对于患者而言,这项工作提示未来的影像检查可能在骨折发生前检测到早期骨损伤,并且旨在恢复健康氧信号和保护H型血管的治疗策略,可能成为预防糖尿病相关骨病的新方向。
引用: Lei, H., Wang, K., Li, L. et al. Multimodal imaging evaluation of hypoxic bone marrow microenvironment and type H vascular injury in diabetes. Sci Rep 16, 7206 (2026). https://doi.org/10.1038/s41598-026-37164-z
关键词: 1型糖尿病, 骨髓, 微血管损伤, 缺氧, 骨脆弱性