Clear Sky Science · zh
全基因组筛选鉴定细胞表面朊蛋白表达的核心调控因子
这对大脑健康为何重要
朊病毒病,如人类的库鲁茨费尔德—雅各布病和牛的“疯牛病”,虽罕见但总是致命的脑部疾病。核心罪魁祸首是一个正常的脑蛋白,称为朊蛋白,它能够错误折叠并在细胞之间传播损伤。神经细胞表面这种蛋白越多,疾病越容易发生。本研究旨在绘制一张全基因组图谱,找出哪些基因控制神经样细胞表面朊蛋白的量。这张图谱可帮助科学家设计新策略以降低该蛋白,从而可能延缓多种神经退行性疾病的进程。
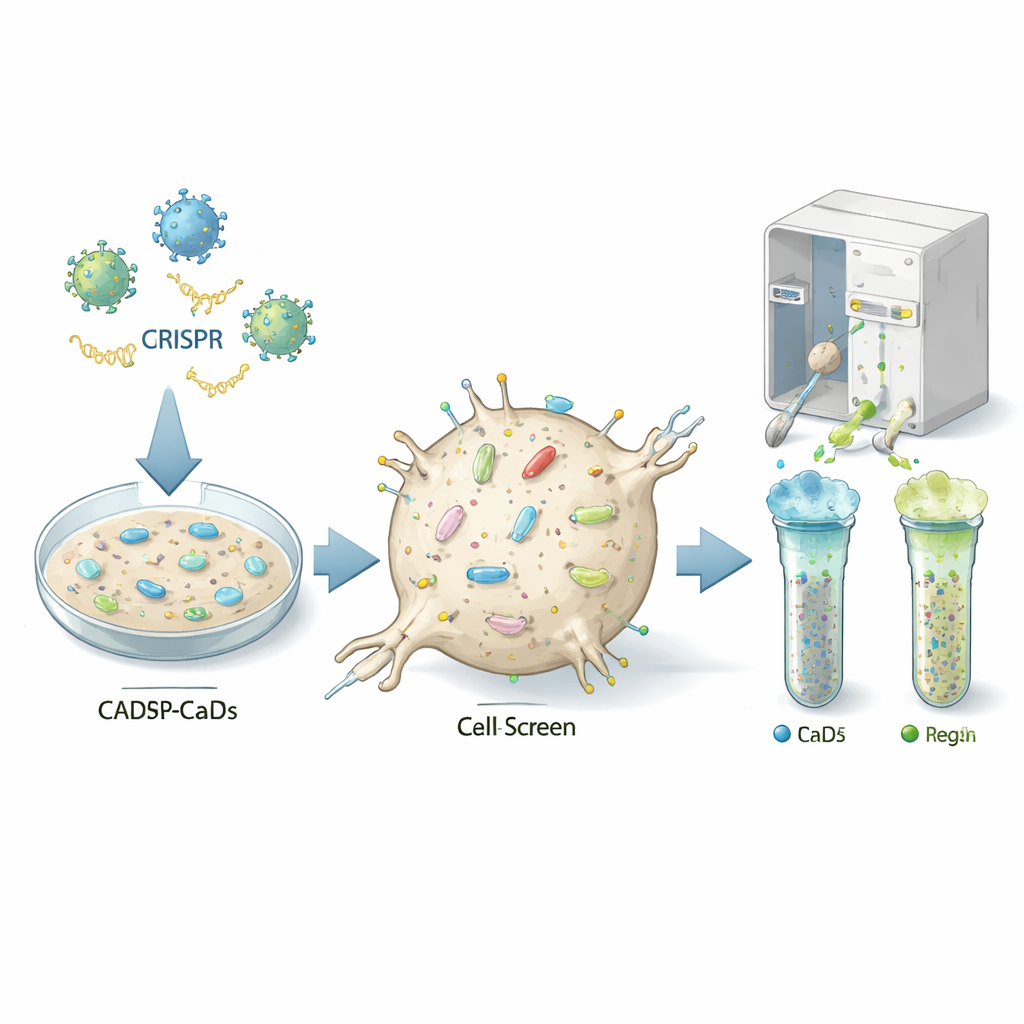
找出细胞的“控制旋钮”
作者使用了一种强大的基因编辑方法——CRISPR——逐一关闭几乎所有基因,作用于一种可以被朊病毒感染的小鼠神经样细胞系(称为 CAD5 细胞)。每个细胞接受不同的基因“打击”,因此所得细胞群体包含数百万种变体,每种缺失特定基因。研究团队随后用识别细胞表面正常朊蛋白的荧光抗体对细胞进行染色,并用细胞分选仪将表面该蛋白异常低或异常高的细胞分离开来。通过测序低组或高组中富集的引导 RNA,便可推断出被敲除的基因在正常情况下是作为表面朊蛋白的开启还是关闭开关。
两种细胞状态,重叠的答案
神经元在其生命周期中并非全都长相或行为相同,因此研究者探究相同基因是否在不同细胞状态下控制朊蛋白。CAD5 细胞可以维持在一种快速生长、较少分化的状态,或通过从培养基中去除血清促使其采取更成熟、更像神经元的形态。研究团队在这两种条件下运行了相同的全基因组 CRISPR 筛选。在未分化(较不成熟)细胞中,他们验证了 46 个可使表面朊蛋白增加的基因和 21 个可使其减少的基因。在分化(更神经样)细胞中,他们确认了 41 个正向调控子和 13 个负向调控子。有 23 个基因在两种细胞状态中均被鉴定出来——大多与将脂质“锚”附着到蛋白上的过程相关——凸显出一套在成熟度无关的情况下运行的核心调控机制。
最重要的关键装配线
进一步分析显示,许多新鉴定的基因属于已知的细胞“装配线”,这些装配线在蛋白质运往细胞表面过程中对其进行修饰。一条主要通路构建 GPI 锚,这是一个富含脂质的小结构,将朊蛋白系留在细胞膜外侧。破坏该通路中的几乎任一步骤都会减少朊蛋白到达表面的数量,在未成熟和成熟细胞中均是如此。第二条通路涉及 N-连接糖基化,在蛋白通过细胞内膜系统时会向其添加复杂的糖链。糖基化途径中的基因主要在较不成熟的细胞中显现出重要性。当研究者用小分子抑制特定糖基化步骤时,表面朊蛋白水平在不杀死细胞的情况下下降了大约三分之一,从而证实了基因学发现。
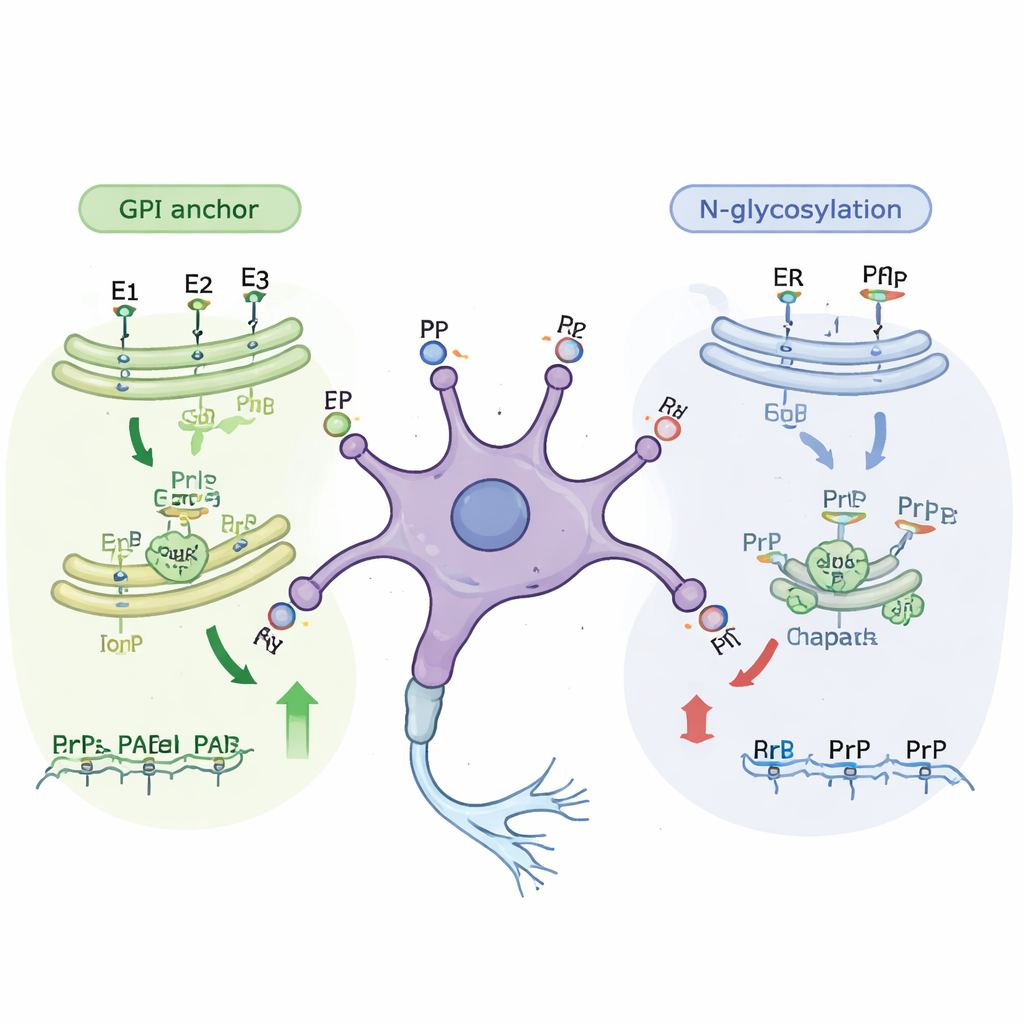
帮手蛋白与应激反应
筛选还突出了分子伴侣——帮助其他蛋白正确折叠的蛋白——作为重要的朊蛋白调控因子。特别是 Hspa5(也称为 BiP),细胞蛋白折叠区室中的核心伴侣,在更神经样的细胞中表现为正向调控子。当研究者用药物抑制 Hspa5 时,两个细胞状态的表面朊蛋白水平均下降,且未见明显的细胞损伤。其他命中基因包括参与蛋白质运输、控制基因表达开关以及若干与突触功能和其他大脑疾病(如阿尔茨海默病和 ALS)相关的蛋白。总体而言,这些结果表明,细胞表面的朊蛋白水平由一张横跨蛋白生成、修饰、运输和质量控制的通路网络共同塑造。
对未来治疗的意义
这项工作提供了首份关于控制易受朊病毒感染的神经样细胞表面朊蛋白量的基因全谱清单。其中一些基因,尤其是 GPI 锚与 N-糖基化通路以及 Hspa5 伴侣系统,成为药物发现的有前景起点:降低它们的活性应能减少可供错误折叠的朊蛋白数目,而既往研究显示即便部分减少也能显著延缓动物模型中的疾病进程。同时,未成熟与成熟细胞之间的明显差异强调了在选择靶点时需考虑脑细胞的状态。尽管还需更多工作来检验操纵这些基因对活体大脑中实际朊病毒感染和其他神经退行性疾病的影响,但本研究为研究者提供了一张可探索的细胞“杠杆”路线图,旨在减缓或预防这些毁灭性疾病。
引用: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
关键词: 朊蛋白, CRISPR 筛选, 神经退行性疾病, 蛋白质糖基化, GPI 锚定