Clear Sky Science · zh
鉴定RBX1为LIPT1转录的调控因子及其在GBM细胞铜诱导细胞死亡中的作用
为什么铜与脑肿瘤很重要
多形性胶质母细胞瘤是最致命的脑癌类型之一,尽管接受了积极的手术、放疗和化疗,大多数患者在确诊后存活时间仍然很短。本研究探讨了一种对抗这些肿瘤的意外盟友:金属铜。研究人员检验了一种新近识别的由铜触发的细胞死亡形式,并鉴定出一条分子通路,可能帮助临床利用这一过程削弱肿瘤并有望增强免疫系统对癌细胞的攻击。
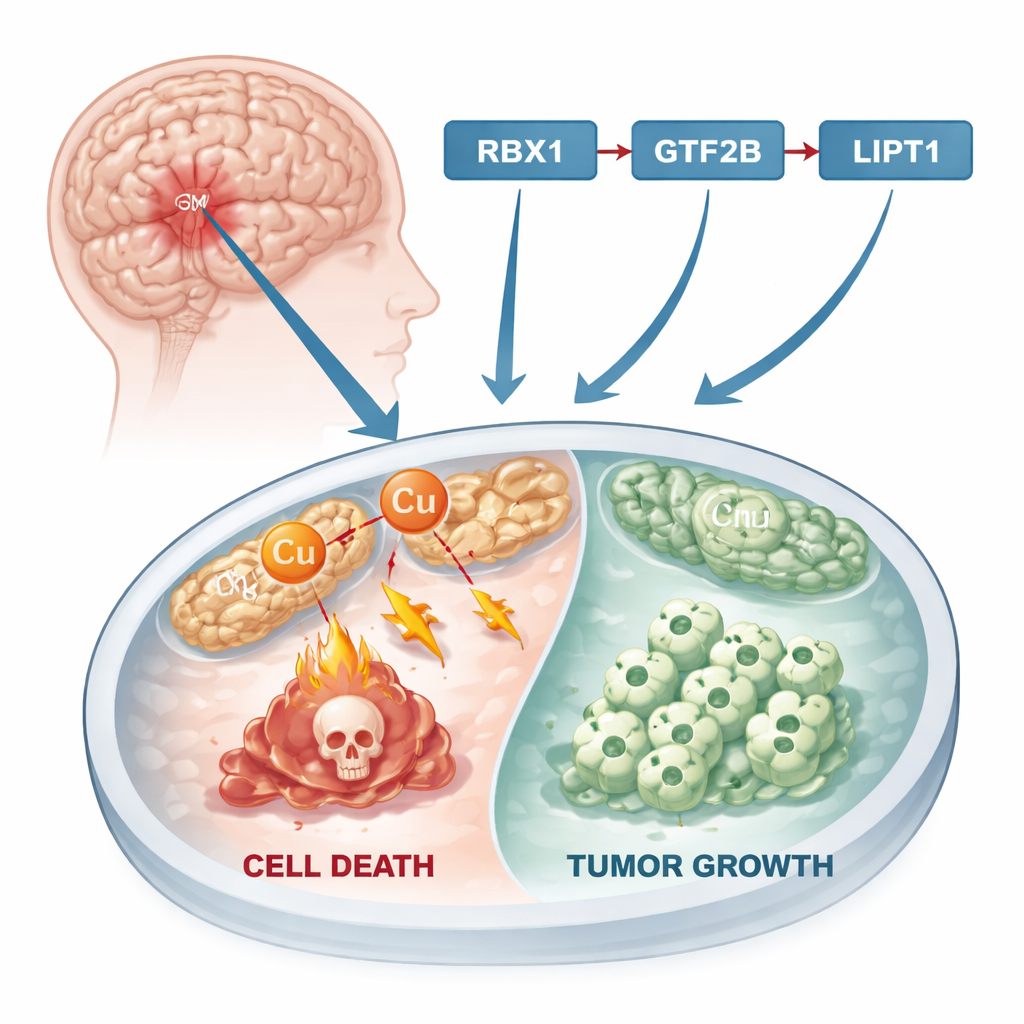
细胞死亡的新途径
几十年来,癌症研究主要关注熟悉的细胞死亡形式,例如程序性细胞死亡(凋亡),在这种过程中受损细胞会静默地关闭自身。最近,科学家们发现了一条不同的路径,称为铜诱导的细胞死亡,或“铜毒死”(cuproptosis)。在这一过程中,过量铜在细胞的能量工厂——线粒体中积累,干扰关键蛋白质,导致有毒蛋白团块形成并最终杀死细胞。由于许多肿瘤具有改变的金属代谢并且铜含量高于正常组织,铜毒死提供了一个潜在的突破口:如果研究者能促使肿瘤细胞走向这种由铜驱动的死亡,可能会减缓或阻止癌症的生长。
聚焦胶质母细胞瘤中的关键基因
作者首先对一组已知参与铜毒死的基因进行了筛查,并比较了它们在胶质母细胞瘤样本与正常脑组织中的表现。特别有一个基因,LIPT1,脱颖而出。它在胶质母细胞瘤组织和若干胶质母细胞瘤细胞系中的活性高于正常脑细胞。重要的是,肿瘤中LIPT1活性较高的患者在治疗后无复发生存期往往更长。高水平的LIPT1还与更多CD8 T细胞的存在相关——这些细胞是免疫系统对抗癌症的前线杀手——这提示该基因可能有助于使肿瘤微环境更易受到免疫攻击。
当铜死亡开关被调低时会发生什么
为检验LIPT1是否真正影响铜驱动的细胞死亡,研究团队将胶质母细胞瘤细胞暴露于一种可靠引发铜毒死的载铜药物组合,然后使用遗传学工具降低LIPT1水平。当抑制LIPT1时,肿瘤细胞对铜诱导的杀伤表现出更强的抵抗性,存活率更高,并显示出更强的迁移和侵袭能力——这些行为与更具侵袭性的癌症相关。在肿瘤细胞与人CD8 T细胞的混合培养中,降低LIPT1还减少了免疫信号分子的释放,使T细胞更难杀死癌细胞。总体而言,这些实验表明LIPT1提高了对铜诱导细胞死亡的敏感性,并支持抗肿瘤免疫活性。
沿着指挥链追溯到RBX1
下一步挑战是弄清为何LIPT1在胶质母细胞瘤中被上调。通过整合若干大型基因与蛋白质数据库,研究人员鉴定出一个转录因子——一种控制基因活性的主开关,名为GTF2B——它与LIPT1基因附近结合,可能增强其表达。他们进一步探究控制GTF2B的上游因子,第二个蛋白RBX1成为有力候选。RBX1是细胞标记与降解系统的一部分,负责为其他蛋白打上被降解的标签。在胶质母细胞瘤细胞中,RBX1水平均低于正常脑细胞,而GTF2B和LIPT1则升高。体外测定显示,RBX1可向GTF2B附加小的“销毁我”标记,导致其被降解;当RBX1增加时,GTF2B水平与LIPT1活性下降,而阻断细胞的降解机制可逆转该效应。
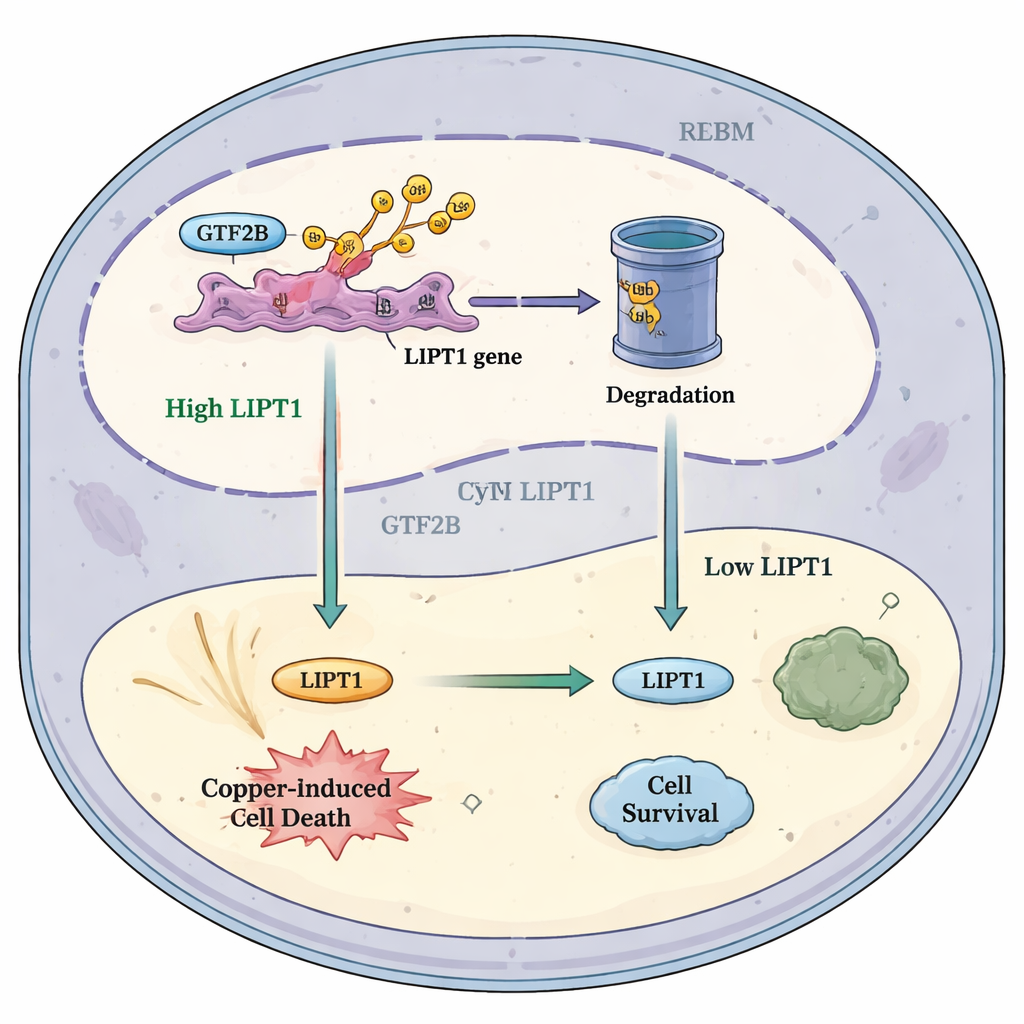
该通路如何助力未来治疗
将这些发现综合起来,作者提出了一个简明模型:在健康状态下,RBX1抑制GTF2B的水平,限制其对LIPT1基因的激活强度。在胶质母细胞瘤中,RBX1减少意味着GTF2B被降解的程度降低。额外的GTF2B进而增强LIPT1,使肿瘤细胞对铜诱导的死亡更敏感并吸引更多抗癌免疫细胞进入。这一模型暗示,通过精确调控RBX1–GTF2B–LIPT1通路,可能配合靶向铜的药物和免疫疗法,将肿瘤内部环境倾向于自我毁灭。尽管在将这一想法应用于患者之前仍需大量工作,这项研究突出了金属生物学、基因调控与肿瘤免疫学的有希望交叉点,可能为这一顽固癌症开辟新的治疗途径。
引用: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
关键词: 胶质母细胞瘤, 铜诱导的细胞死亡, LIPT1, 肿瘤免疫学, RBX1通路