Clear Sky Science · zh
将机器学习与基于物理的建模相结合以预测吉西他滨负载纳米复合材料的设计
通过设计打造更聪明的癌症药物
像吉西他滨这样的抗癌药物能够挽救生命,但它们常常更像是粗糙的工具而非精密仪器:在体内容易被迅速分解、难以准确到达目标,并且会引起严重的副作用。本研究探讨了计算机如何帮助科学家在屏幕上“预先测试”新的微小药物载体,而不只是依赖实验室,从而使吉西他滨治疗更有效、持续时间更长,并有可能对患者更安全。
微小载体为何重要
传统化疗在体内扩散大量药物分子,这些分子遍布全身,而不仅仅集中在肿瘤部位。纳米复合材料——由工程化的颗粒构成,其尺寸比一粒沙子小数千倍——提供了一种封装吉西他滨的方式,使其在血液中得到保护并更直接地递送到癌细胞。两个数值在很大程度上决定了设计是否有用。载药量(loading efficiency)告诉我们每个粒子内最终含有多少药物,而封装效率(encapsulation efficiency)则衡量起始药物中有多少比例被成功捕获而未被浪费。两者都高意味着注射次数更少、所需载体材料更少,并且更有可能猛烈打击肿瘤而不压垮机体其他部位。
从试错到数据驱动的设计
手工设计这些纳米载体就像试图调节数百个旋钮的收音机——粒子尺寸、表面电荷、材料、涂层和制备方法都以复杂的方式相互影响。直到现在,研究者主要一次只改变一两个参数并测量结果,这一过程既缓慢又昂贵,只能揭示整体图景的一小部分。在这项工作中,作者从文献中收集了59个经过仔细检验的吉西他滨纳米载体配方,并用计算机生成的基于物理的示例来丰富数据集。该组合数据集使他们能够测试若干机器学习方法——即从数据中学习模式的计算程序——以仅凭设计选择来预测载药量和封装效率。
让物理引导算法
大多数机器学习系统是强大的曲线拟合工具:它们可以发现模式,但并不知道何时答案会违背自然法则。为避免产生不现实的预测,研究者构建了一种混合方法,将数据与关于药物分子如何运动、结合以及在封闭体系中如何达到平衡的基本物理规则结合起来。在他们的框架中,任何会暗示例如“产生比最初加入更多的药物”或“忽视分子如何在材料中扩散”的预测,都将在训练中受到温和惩罚。这种“物理知情”方法会将模型引导向在化学和物理上合理的答案,特别是在真实测量数据稀缺的设计空间区域。
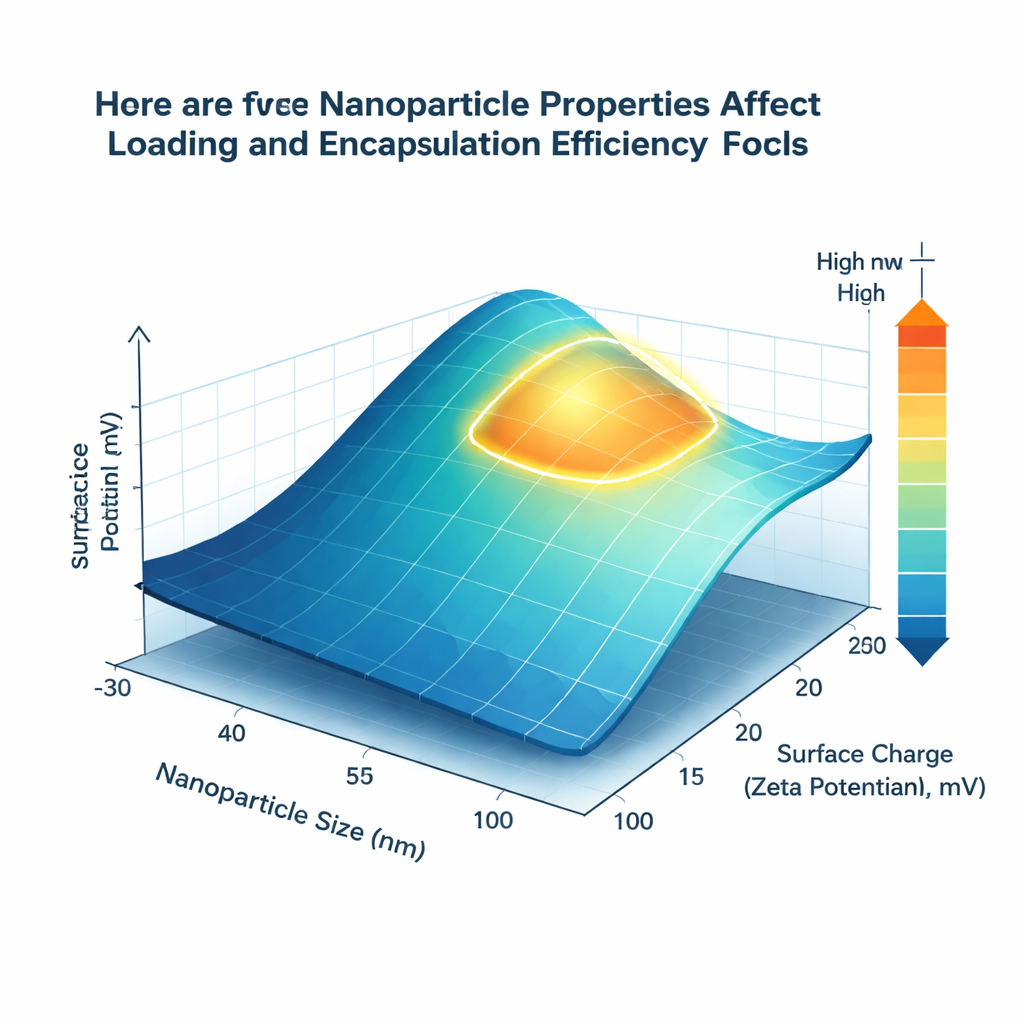
模型发现了什么
在测试的技术中,一种名为XGBoost的先进集成算法给出了最精确的预测,与报道的实验结果在两项关键效率上都高度吻合。但除了准确性,团队还希望得到可理解的设计规则。通过一种称为SHAP的方法——可对每个因素推动预测上升或下降的强度进行排序——他们发现粒子尺寸和表面电荷始终主导性能。直径约在80到150纳米之间的纳米载体在表面积与内部体积之间提供了最佳平衡,从而提升了载药量和封装效率。轻微正电的表面电荷(约+15到+25毫伏)被发现与更好的吉西他滨捕获相关,这很可能是因为带正电的载体表面与药物的带负电基团发生有利相互作用。
面向未来癌症治疗的数字化地图
最终结果并非一种现成的药物,而是一个强大的规划工具。这项研究提供了一种“设计地图”,指引研究者朝着那些更有可能很好地容纳并保护吉西他滨的纳米载体配方前进,同时避免数百万种不太可能成功的组合。作者强调,他们的预测仍需在新的实验室和动物研究中得到验证,并且他们的数据集——尽管经过精心汇编——规模有限。即便如此,这一物理感知的机器学习框架展示了计算机如何帮助缩小寻找更好癌症药物载体的范围,降低成本并加速从想法到更精确、更利于患者的治疗方案的进程。
引用: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
关键词: 纳米医学, 吉西他滨, 药物递送, 机器学习, 纳米颗粒