Clear Sky Science · zh
基于网络药理学与多组学分析的celastrol靶向CTNNB1/STAT3抑制葡萄膜黑色素瘤的分子机制研究
古方遇到眼部癌症
葡萄膜黑色素瘤是一种罕见但致命的眼内肿瘤。一旦发生转移,现有治疗对预后几乎无能为力。本研究探讨了从传统中药提取的分子celastrol是否可被重新利用来对抗该癌症。研究者结合大数据生物学、计算模拟与实验室验证,揭示了celastrol可能如何关闭帮助葡萄膜黑色素瘤生长和扩散的关键分子开关。
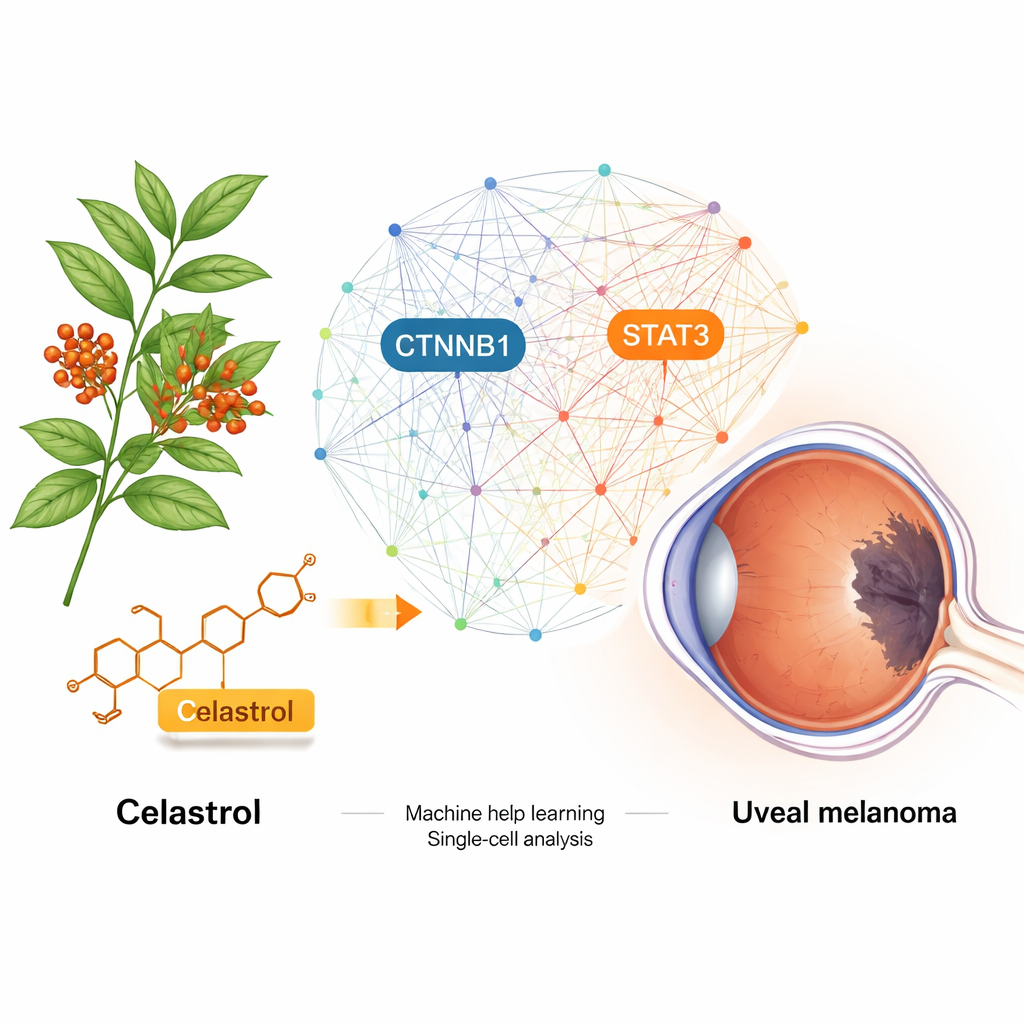
是什么让这种眼肿瘤如此危险
葡萄膜黑色素瘤是成人最常见的原发性眼部恶性肿瘤,约半数患者最终出现转移,通常首发于肝脏。到那一阶段,生存期常以月计。外科、放疗及局部治疗可控制眼内原发灶,但全身用药疗效有限且常伴严重副作用。因此,科学家们在寻找既能抑制肿瘤生长又更易耐受的药物——天然产物如celastrol正因此受到高度关注。
显微镜下的天然化合物
Celastrol来源于雷公藤(Tripterygium wilfordii),该植物在传统中医中有长期应用。既往研究表明其能延缓若干肿瘤的生长,但在葡萄膜黑色素瘤中的作用机理尚不明确。团队首先挖掘多个生物医学数据库,预测celastrol可能结合的人体蛋白以及与葡萄膜黑色素瘤高度相关的蛋白质。比较这些名单后,他们找到了46个重叠候选分子。利用描绘蛋白相互作用的计算工具,他们将目标缩小到位于肿瘤细胞主要生长与生存通路控制点的若干“枢纽”分子。
锁定两个主控开关
为确定最关键的因子,研究者将癌症基因组图谱(TCGA)的患者肿瘤基因数据与三种不同的机器学习方法相结合。三种方法一致指向两个基因:CTNNB1——Wnt信号通路的核心成分,驱动细胞增生;以及STAT3——炎症、细胞存活与免疫逃逸的重要调控因子。对整体肿瘤样本和单细胞RNA测序的进一步分析显示,这两基因在葡萄膜黑色素瘤细胞中高度活跃,特别是在更具侵袭性的细胞亚群中,并与周围免疫细胞的变化相关。简言之,CTNNB1和STAT3像是帮助肿瘤生存并抑制免疫反应的主控开关。
从计算模型到活细胞验证
随后,团队使用分子对接与长时分子动力学模拟测试celastrol是否能在物理上结合CTNNB1和STAT3。虚拟实验表明结合强且稳定,通过多个氢键及药物周围的紧密包裹得到支持。接着他们开展细胞实验,用celastrol处理人源葡萄膜黑色素瘤细胞系与一种相关的鼠源黑色素瘤细胞系。两种细胞中,celastrol显著降低细胞存活和克隆形成能力,在伤口愈合迁移实验中减缓迁移,并诱导程序性细胞死亡。它还导致细胞在细胞周期的特定阶段停滞,阻止细胞分裂。当研究者测量基因表达和蛋白水平时,发现celastrol显著下调CTNNB1和STAT3,证实其在活细胞内命中了预测的靶点。
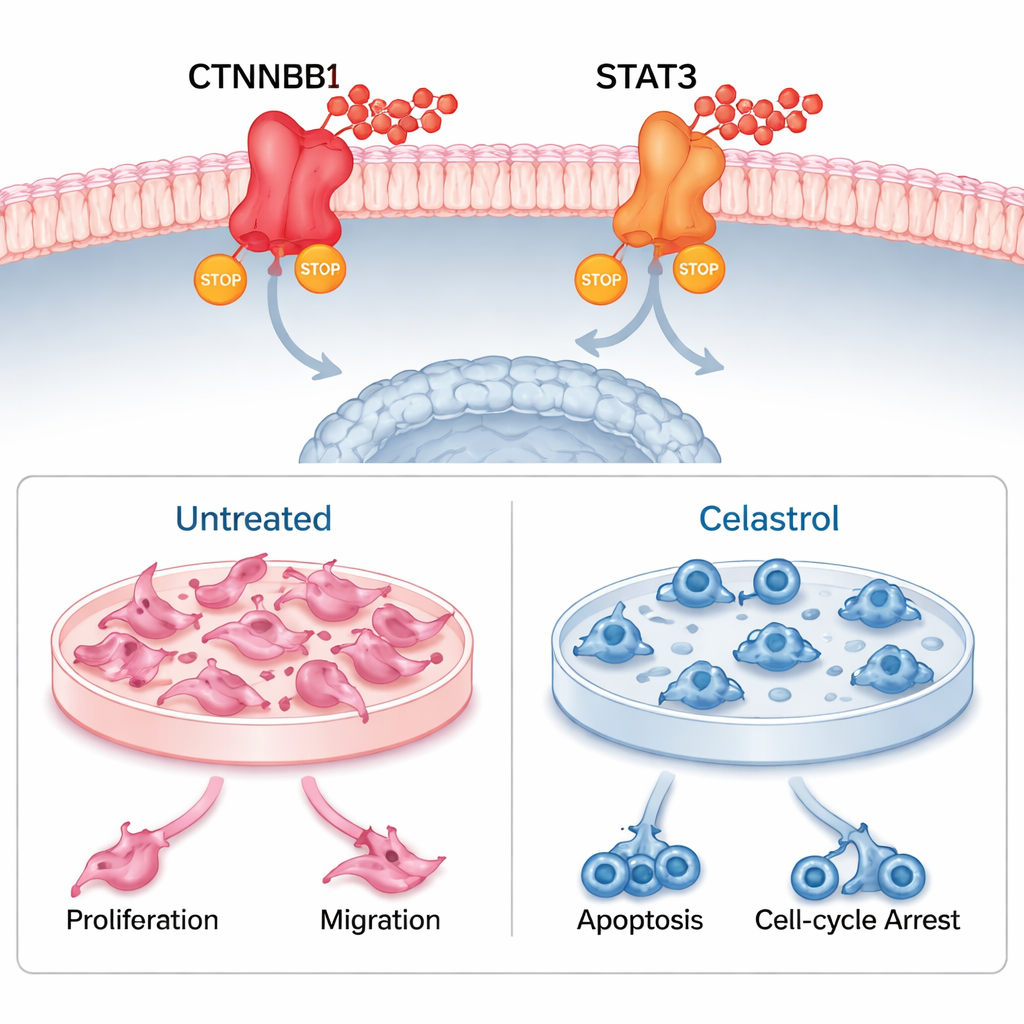
这对未来治疗意味着什么
综合来看,结果表明celastrol可能通过同时关闭CTNNB1和STAT3来对抗葡萄膜黑色素瘤。这种双重作用不仅减缓肿瘤生长和转移,还可能以有利于抗肿瘤反应的方式重塑肿瘤的免疫环境。尽管这些工作基于细胞与计算模型—尚未在患者或动物模型中验证—但为进一步测试奠定了坚实基础。对普通读者来说,关键信息是:一种根植于传统医学的化合物已成为一种科学上合理的新型眼癌治疗候选者,能够同时作用于肿瘤及其周围的细胞生态系统。
引用: Li, Z., Xi, R., Han, X. et al. Research on the molecular mechanism of celastrol targeting CTNNB1/STAT3 to inhibit uveal melanoma based on network pharmacology and multi-omics analysis. Sci Rep 16, 6140 (2026). https://doi.org/10.1038/s41598-026-37061-5
关键词: 葡萄膜黑色素瘤, 雷公藤内酯(celastrol), 眼部癌症, 癌症信号通路, 肿瘤微环境