Clear Sky Science · zh
神经内分泌肿瘤特定系统治疗对神经内分泌肿瘤细胞中CXCR4表达与功能的影响
这对未来癌症护理的重要性
当某些罕见的肠道和胰腺癌变得更具侵袭性时,常常会不再对标准的靶向治疗产生反应。临床医生和研究者迫切需要新的方法来识别并攻击这些更难处理的肿瘤。本研究提出了一个具有重大意义的实用问题:患者已接受的化疗和靶向药物是否会改变一个关键的肿瘤标志物CXCR4?该标志物正被开发为诊断“灯塔”与治疗靶点。
在侵袭性肿瘤细胞上变化的靶点
神经内分泌肿瘤是起源于分泌激素细胞的罕见癌症,最常见于肠道和胰腺。在早期、较为有序的状态下,这些肿瘤通常在细胞表面表达称为生长抑素受体2(sst2)的分子,医生可以借此用专门的放射性药物进行成像和治疗。随着疾病变得更具侵袭性,这些肿瘤常丧失该标志,使其更难检测和靶向。与此同时,许多肿瘤会激活另一种表面分子——称为CXCR4的受体,这与更快的生长、向远处器官转移及生存率降低有关。因为CXCR4可用PET示踪剂成像,且有可能用放射性或抗体类药物攻击,故其已成为常规治疗失败时有前景的“备选”靶点。
在肿瘤细胞模型中测试真实世界的药物
研究者想弄清楚那些已用于治疗高分化或高恶性度神经内分泌肿瘤的药物,会如何影响CXCR4本身。如果这些药物无意间降低了CXCR4,可能会削弱未来基于CXCR4的成像或治疗——但它们也可能帮助抑制肿瘤的侵袭性。团队使用了三种代表侵袭性形式的人类肿瘤细胞系,其中一条是接近模拟难治性肿瘤的混合系。研究者将这些细胞暴露于六种常用药物:化疗药顺铂、依托泊苷、链脲佐菌素、5‑氟尿嘧啶,口服药替莫唑胺,以及靶向mTOR的抑制剂依维莫司。处理后,他们在基因和蛋白水平测定CXCR4,并测试细胞摄取针对CXCR4的PET示踪剂的能力。
部分药物降低了CXCR4信号
结果显示,并非所有抗癌药对该受体的影响相同。顺铂在三条细胞系中的两条中明显降低了CXCR4的基因活性,并在两条中显著减少了示踪剂的摄取,表明可供示踪剂结合的功能性受体减少。替莫唑胺和依维莫司也在若干细胞系中降低了CXCR4的基因和蛋白水平,尽管这并不总是转化为示踪剂摄取的统计学显著下降。相比之下,依托泊苷和链脲佐菌素对CXCR4影响甚微,而5‑氟尿嘧啶仅引起温和变化,未显著改变示踪剂结合。总体模式表明,顺铂、替莫唑胺和依维莫司均可在这些侵袭性肿瘤细胞中抑制CXCR4,而其他药物主要保持其不变。
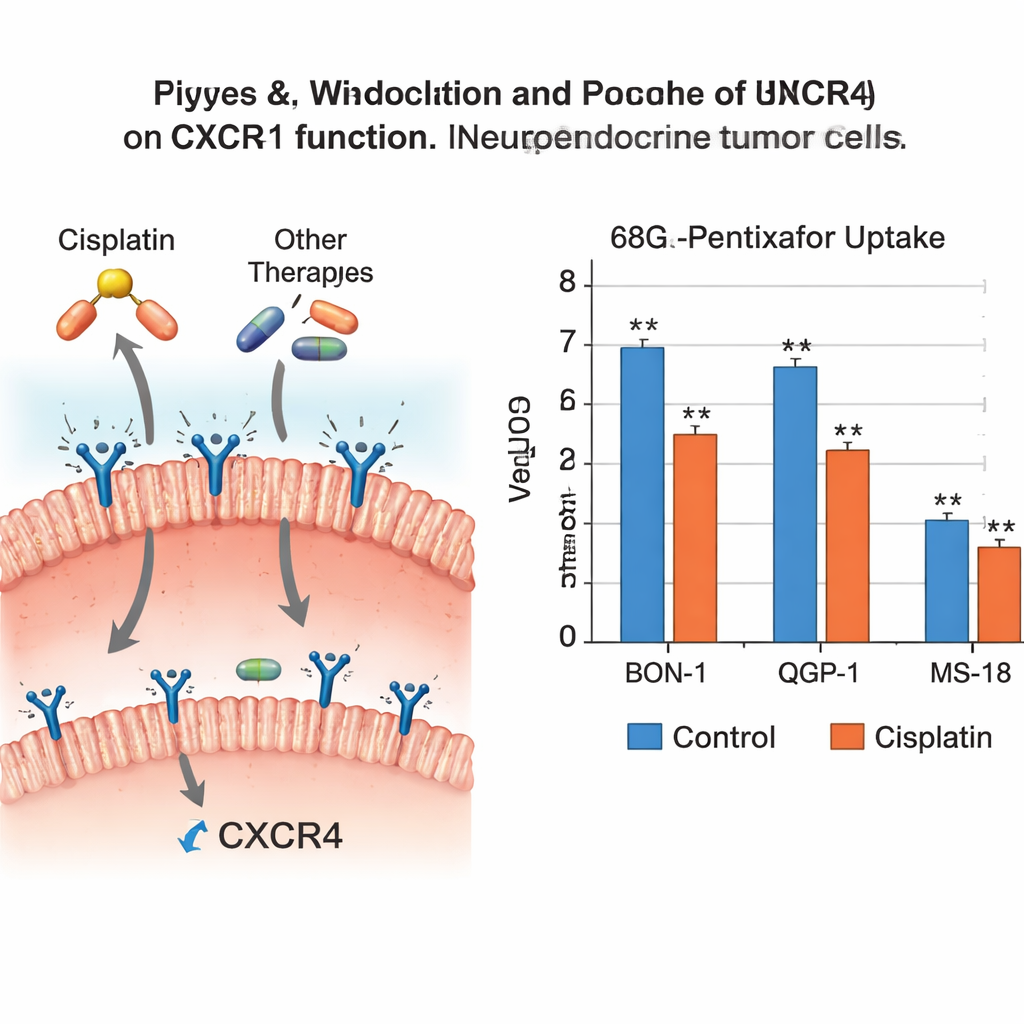
这对扫描与治疗时机的含义
这些发现对未来的病人护理传达了双重信息。一方面,降低CXCR4可能是顺铂、替莫唑胺和依维莫司等药物遏制肿瘤扩散的一部分机制,因为高表达的CXCR4与侵袭性和转移相关。另一方面,如果肿瘤在持续治疗下被抑制了CXCR4,基于CXCR4的PET扫描可能会低估病灶规模,基于CXCR4的放射性治疗也可能因结合位点减少而效果受限。该研究提示,将CXCR4靶向治疗与这些系统药物直接联合使用不太可能增强CXCR4聚焦疗法的效果,反而可能削弱它们。
为个体化治疗补上的新一块拼图
对非专业读者而言,关键结论是:单一肿瘤标志物可以同时扮演双重角色——既是侵袭性疾病的警示信号,也是成像与靶向治疗的有用切入点。本研究表明,一些既有的抗癌药物可以悄然地上调或下调该标志物。在临床实践中,这可能影响何时安排基于CXCR4的扫描与治疗——理想情况下在受体最丰富时进行——并有助于解释为何某些治疗对快速生长的神经内分泌肿瘤有效。尽管这些结果来自细胞模型,仍需在患者中得到验证,但它们为更智能地安排这些棘手肿瘤的治疗顺序迈出了重要一步。
引用: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
关键词: 神经内分泌肿瘤, CXCR4, 顺铂, 依维莫司, 靶向成像