Clear Sky Science · zh
无标记荧光寿命成像可在自发性发生的犬口腔肿瘤中区分癌变与健康组织
以新光谱看见癌症
人类和宠物的口腔癌都以难以完全切除著称。外科医生必须在肿瘤周围切取较宽的“安全”边缘以避免留下隐藏的癌细胞,但在口腔中这可能意味着损失重要的骨骼、牙齿和影响进食与发声的软组织。本研究探索了一种用于宠物犬手术中的光学成像方法,可能帮助外科医生在手术中实时区分癌变与健康组织——在确保控制肿瘤的同时尽量保留正常组织。
为何肿瘤边界如此难以辨认
在现有的头颈部癌症手术中,医生常依赖冰冻切片的快速病理分析来判断切除边缘是否无癌。但该过程耗时、仅取样小范围且可能漏诊。类似的问题也困扰着犬只口腔肿瘤的治疗,局部复发仍相当常见。由于在手术中无法可靠“看见”显微级的癌变,外科医生通常会切除较大的边缘,这会影响咀嚼、吞咽和外观。作者希望测试一种非侵入性的成像方法,能在手术室内直接划清癌组织与正常组织的界线。
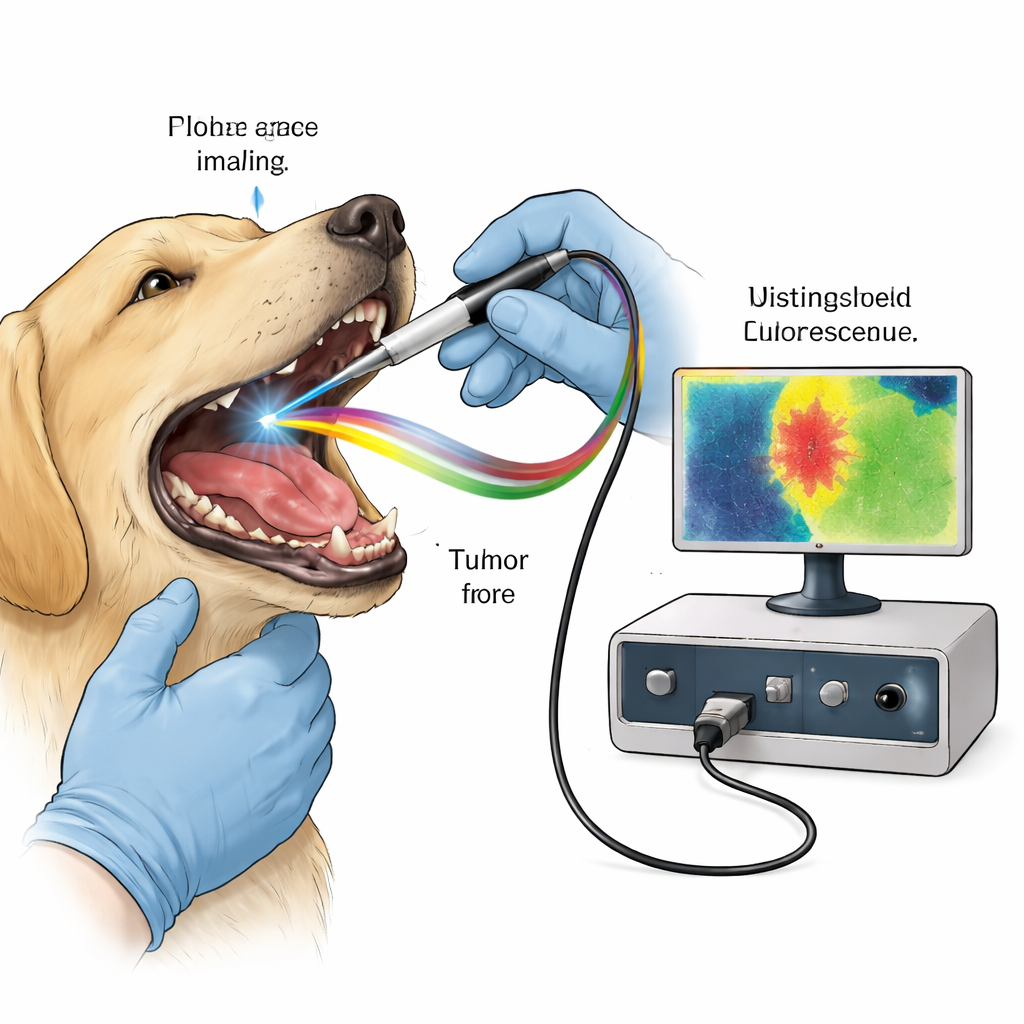
以天然荧光作为手术向导
组织中许多分子在受短脉冲激光激发后会自然发出微弱荧光。结缔组织中的胶原以及与细胞代谢相关的分子(如NADH和FAD),在发光的颜色与衰减时间上各有特征。癌症会扰乱组织结构和能量代谢,细微改变这种荧光指纹。荧光寿命成像(FLIm)不仅测量组织发光的强度,还测量这种发光持续的时间(以十亿分之一秒计),这一特性较不受观察条件影响。研究团队使用定制的手持探头,对麻醉犬的肿瘤区域发射快速紫外脉冲,并在三个光谱通道中记录返回的荧光,分别针对胶原、代谢分子和一种发红光的化合物原卟啉 IX(PpIX)。
加入趋癌染料:帮助还是炒作?
通过口服前体药物5-氨基乙酰丙酸(5-ALA),PpIX可在许多肿瘤中积累。在蓝光下,富含PpIX的区域常显鲜艳的粉红色,外科医生据此定位癌变。研究者先在犬口腔癌细胞系中确认5-ALA可诱导强烈的PpIX荧光,并证明参与产生和摄取5-ALA的基因在癌细胞中更为活跃。随后他们招募了15只自然发生口腔肿瘤的宠物犬,在手术前数小时给予5-ALA。在手术室内,大多数肿瘤在肉眼下有可见荧光,但一些非癌性的炎性或病毒性病变也会发光,提示单凭肉眼颜色可能无法可靠标记肿瘤边界。
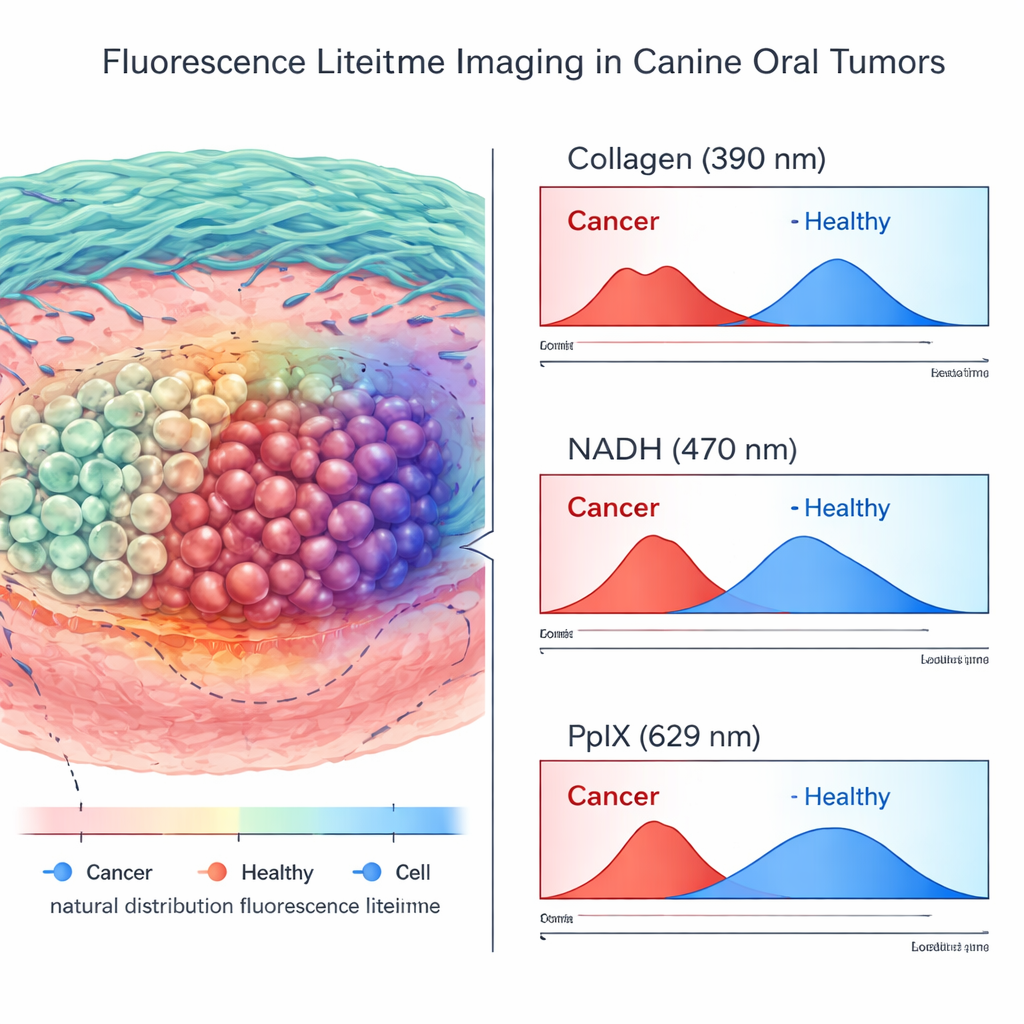
寿命图像揭示了什么
在来自肿瘤及邻近正常组织的20多万个高质量测量点中,团队将FLIm信号与详细病理图谱进行了比较。他们发现许多寿命和强度特征在癌变与健康组织之间有显著差异。然而,最强且最一致的区分来自无标记通道:在对胶原敏感的波段中寿命变短,以及在对NADH敏感波段中出现特征性位移,这些都与癌变紧密相关。相比之下,受5-ALA增强的PpIX通道在活体组织中提供的信息较不可靠,其信号在正常区域波动很大,可能是因为发炎的牙龈和黏膜要么积累了5-ALA,要么含有天然荧光的卟啉类物质,模仿了肿瘤信号。
从手术台到实验台再回到手术室
当研究者在切除后的标本上进行成像时,结果略有变化。体外时,一些基于PpIX的特征在区分癌变与健康组织方面变得更有用,提示其在“床旁”切缘检查中可能有用。但当应用复杂的统计模型和机器学习时,术中和术后数据的最佳分类器都更依赖于天然自发荧光信号,而非外加染料。无标记FLIm本身在区分癌变与正常组织上达到了可观的准确度,加入PpIX增益甚微,有时反而带来混淆。
这对未来手术意味着什么
对宠物主人以及最终的人类患者来说,关键的信息是外科医生或许有一天可以使用一种基于光的工具,在不依赖额外药物或染料的情况下看到癌症的边界。此项在犬只进行的研究——作为接近人类口腔癌的大型动物模型——显示机体自身的荧光特征足以在手术中指导决策。在此背景下加入5-ALA和PpIX并未显著提升准确性以抵消额外的成本、复杂性和潜在副作用。作者得出结论,未来的工作应着重完善无标记荧光寿命成像本身——可能针对特定解剖部位定制分析方法——而不是一味追求更多对比剂。若成功,这类技术可减少二次手术,保留更多正常组织,同时仍能控制癌症。
引用: Goldschmidt, S., Marcu, L., Ehrlich, K. et al. Label-free fluorescence lifetime imaging can distinguish cancer from healthy tissue in spontaneously occurring canine oral tumors. Sci Rep 16, 6077 (2026). https://doi.org/10.1038/s41598-026-37001-3
关键词: 口腔癌成像, 犬口腔肿瘤, 荧光寿命, 手术切缘, 5-ALA PpIX