Clear Sky Science · zh
使用Oxford Nanopore技术的扩增子测序作为绵羊小反刍动物逆转录病毒的诊断替代方法
日常绵羊身上的隐匿感染
全世界的绵羊常常携带一些能削弱健康、缩短寿命并给农场带来损失的病毒——这些病毒在多年间往往没有明显症状。该研究探讨了使用便携式DNA测序技术发现这些隐匿感染的新方法,可能在保护动物福祉、农场收入乃至粮食安全方面带来重大改进。
缓慢且代价高、难以察觉的疾病
研究聚焦于小反刍动物逆转录病毒(SRLV),这是一类感染绵羊和山羊的病毒。在绵羊中,它们引发马埃迪-维斯纳病(Maedi-Visna),为长期慢性感染,可能导致呼吸问题、关节炎、脑部疾病和慢性乳房炎。许多被感染的动物从不表现明显症状,但病毒仍会降低产奶量、增加羔羊死亡率并导致提前淘汰。在一些欧洲的乳用羊群(包括西班牙和希腊),约有一半的动物可能被感染,这使得该病成为强度化养殖中最重要的绵羊疾病之一。
为何现有检测漏掉许多感染个体
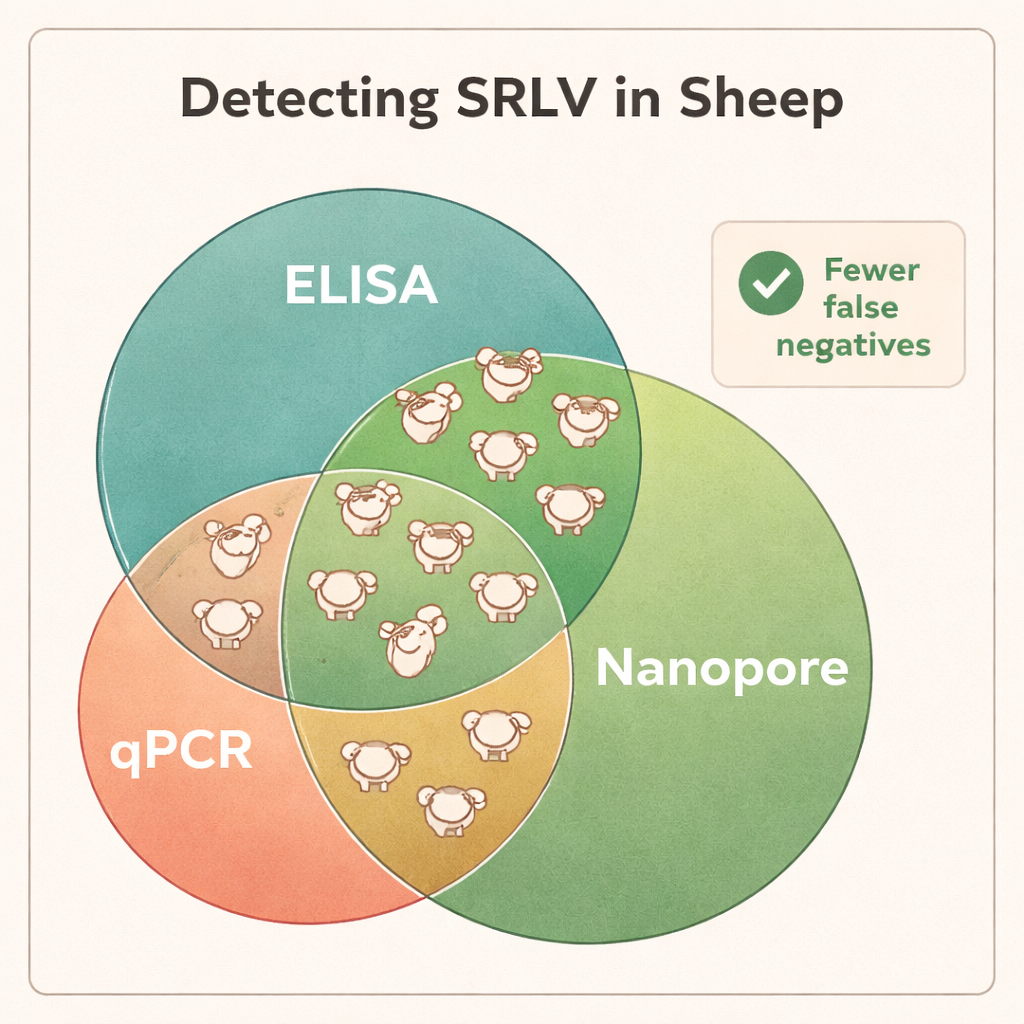
目前,农场主要依赖检测血液中抗体的血清学检测(ELISA)或标准的DNA检测(qPCR)来判断哪些动物感染并应从羊群中移除。但SRLV变异和重组速度快,形成许多略有不同的病毒变体。一些变体难以被抗体检测识别,部分感染的绵羊甚至不会产生强烈的抗体反应。qPCR针对的是短而非常特异的病毒DNA片段,如果这些目标区域发生变化,qPCR也会失效。因此,许多真正感染的动物检测呈阴性并留在羊群中,悄悄传播病毒。
用实时读取DNA来发现病毒
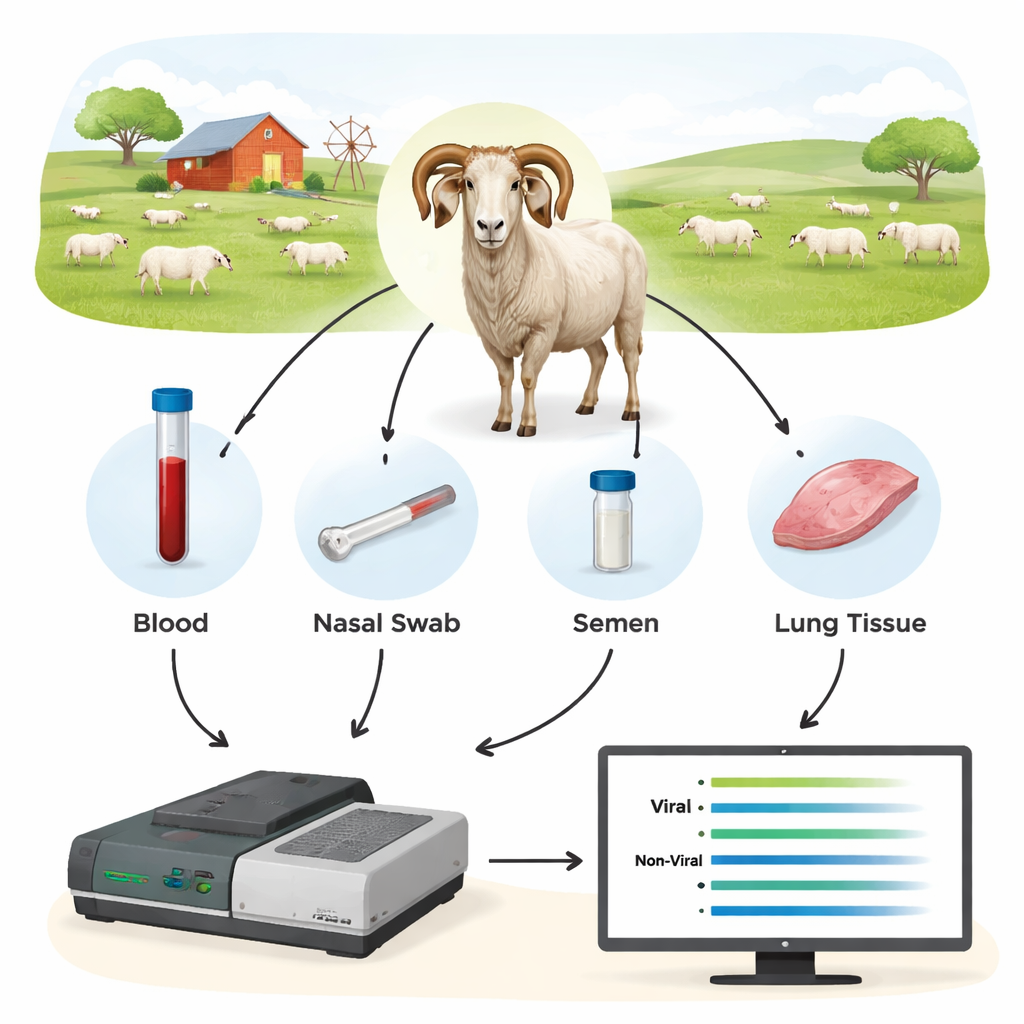
研究者测试了一种称为Oxford Nanopore测序的第三代DNA方法,作为一种新型诊断工具。他们不是去寻找单一很小的病毒DNA片段,而是先从动物样本中扩增更长的关键病毒基因片段,然后在Nanopore设备上实时测序这些片段。他们从44只公羊及其他绵羊采集了血液、鼻拭子、精液和来自血液与肺部的细胞,其中许多动物已用常规方法检测过。通过关注那些相对保守但足够长以揭示确切菌株的病毒区域,团队既能检测感染,又能识别存在的病毒类型。
血液效果最佳——并发现其他检测遗漏的感染
测序结果表明,全血DNA是发现SRLV最可靠的样本类型,尽管病毒主要存在于一小部分白细胞中。来自高度感染动物的肺组织含有极高量的病毒DNA,但此类样本仅在宰杀后可获得。相比之下,鼻拭子、精液和纯化的白细胞提供的病毒量太少,难以稳定诊断。将Nanopore结果与标准ELISA和qPCR比较时,差异明显:Nanopore测序确认了所有ELISA阳性的公羊也确实感染,但同时揭示许多ELISA阴性的动物实际上也被感染。在不同羊群中,约40–45%被ELISA判定为“阴性”的动物被发现携带病毒,而qPCR漏检的比例更高。测序数据还在部分公羊中揭示了不同SRLV类型的混合感染,这类信息传统检测难以提供。
从单纯的“有/无”到更深入的见解
由于Nanopore能够读取实际的病毒序列,它能超越简单的是非诊断。团队利用这些数据比较病毒菌株,构建流行于羊群中的病毒家族树,并研究病毒蛋白的细微差别,这些差别可能解释为何某些动物逃避免疫学ELISA试剂盒的检测。他们表明,被商业抗体检测所针对的关键病毒蛋白的某些版本,在抗体阳性和抗体阴性动物之间存在显著差异。随着时间推移,这类信息可用于改进血清学测试和育种计划,旨在选择自然更具抗性的动物。
对农户和动物健康的意义
对非专业读者而言,核心信息很直接:通过直接读取更长的病毒DNA片段,Nanopore测序比当前常规检测能更早、更准确地发现更多被感染的绵羊。它还可以告诉我们羊群中有哪些确切的病毒菌株。尽管该方法目前比一次性血液检测更复杂且成本更高,但技术正变得更快、更便宜、更便携。如果将其纳入控制计划,可能大幅减少“隐匿”携带者的数量,改善疫苗和检测的设计,并支持培育更具抗性的羊群——使养羊业更可持续、更人道。
引用: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
关键词: 绵羊健康, 逆转录病毒, 纳米孔测序, 兽医诊断, 马埃迪-维斯纳(Maedi-Visna)