Clear Sky Science · zh
评估 HIST1H4C 在乳腺癌中的预后意义:对新辅助治疗的启示
这项研究为何重要
对于许多乳腺癌患者,手术前给予的化疗——称为新辅助治疗——可以缩小肿瘤,使手术更安全、更成功。但并非人人受益,且该治疗可能带来严重副作用。本研究探讨在肿瘤样本中测量的单一基因 HIST1H4C,是否能够帮助医生预测谁更可能对这种术前治疗有良好反应,谁则可能面临更高的复发风险。
隐藏在肿瘤“包装”中的基因
HIST1H4C 属于一类帮助在细胞内包装 DNA 的基因,有点像线轴绕线的卷轴。这些“包装”蛋白——组蛋白,不仅仅用来组织 DNA;它们影响基因的开启与关闭,因此能影响癌症的侵袭性以及对药物的反应。早期使用单细胞测序的研究提示,HIST1H4C 在高分级乳腺肿瘤中特别活跃——这些肿瘤在显微镜下看起来更异常,通常行为更具侵袭性。这提出了一个关键问题:HIST1H4C 是否可以作为一个将肿瘤侵袭性、化疗反应和长期预后联系起来的标志?
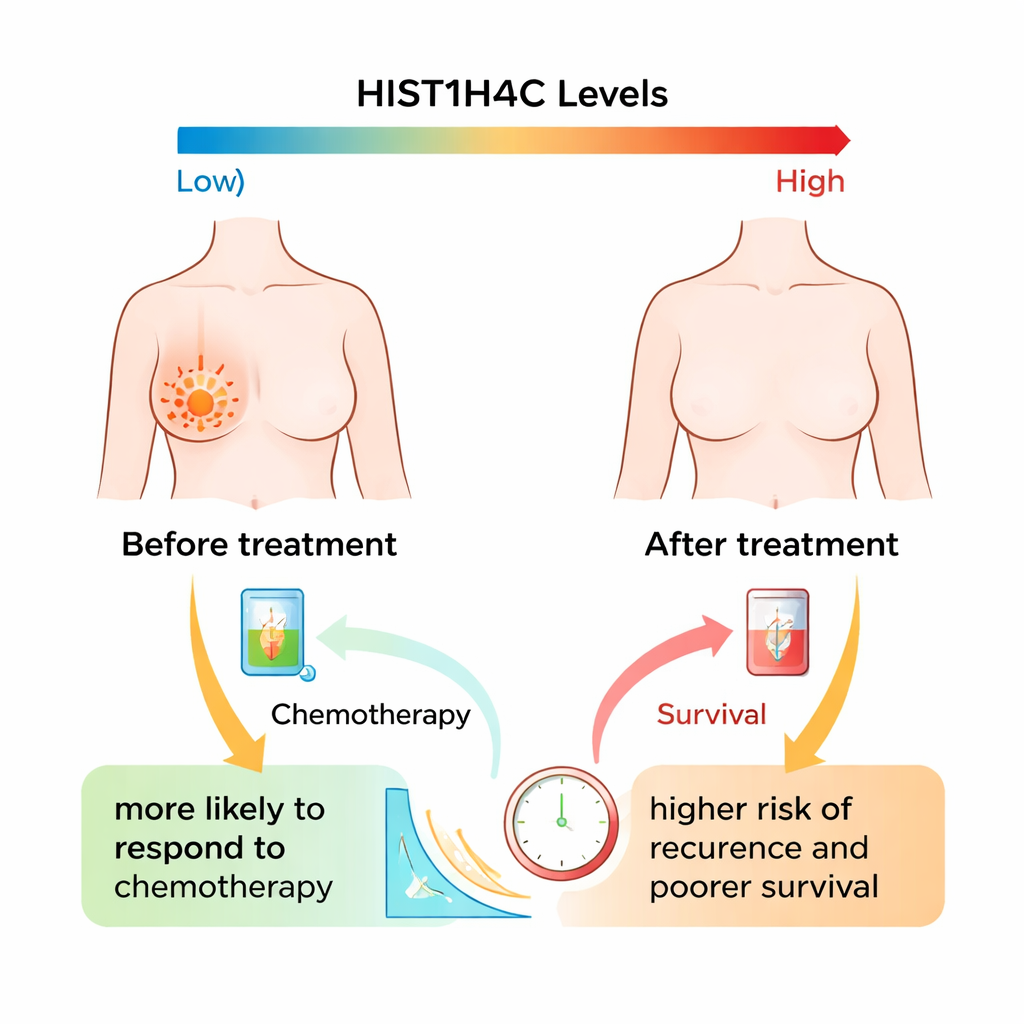
在治疗前后检测肿瘤
研究人员随访了 2019 至 2022 年间在中国广州一所医疗中心接受治疗的 100 多名 II 期及以上乳腺癌女性患者。所有患者均接受标准新辅助化疗,包括蒽环类和紫杉类药物,部分 HER2 阳性患者还接受了靶向治疗。在治疗前和手术后分别采集了肿瘤样本。团队测量了每个样本中 HIST1H4C mRNA 的含量——这是基因表达强度的一个指标——并将这些水平与肿瘤的治疗反应(完全或部分缩小)以及患者无病生存时间进行了比较。
一个意外的双面信号
结果显示出一个有趣的模式。在治疗前,反应良好的患者——肿瘤完全或部分缩小者——实际具有比反应差的患者更高的 HIST1H4C 水平。换句话说,较高的起始基因水平与更强的化疗敏感性相关,尽管这些肿瘤常伴随其他高危特征,如激素受体阴性、更多淋巴结受累和三阴性状态。然而在治疗后,情况发生了逆转:手术后仍显示高 HIST1H4C 水平的患者往往残余肿瘤较大且无进展生存更差。在整个队列中,HIST1H4C 水平通常在治疗后下降,但这种下降在反应良好者中比反应差者更显著。
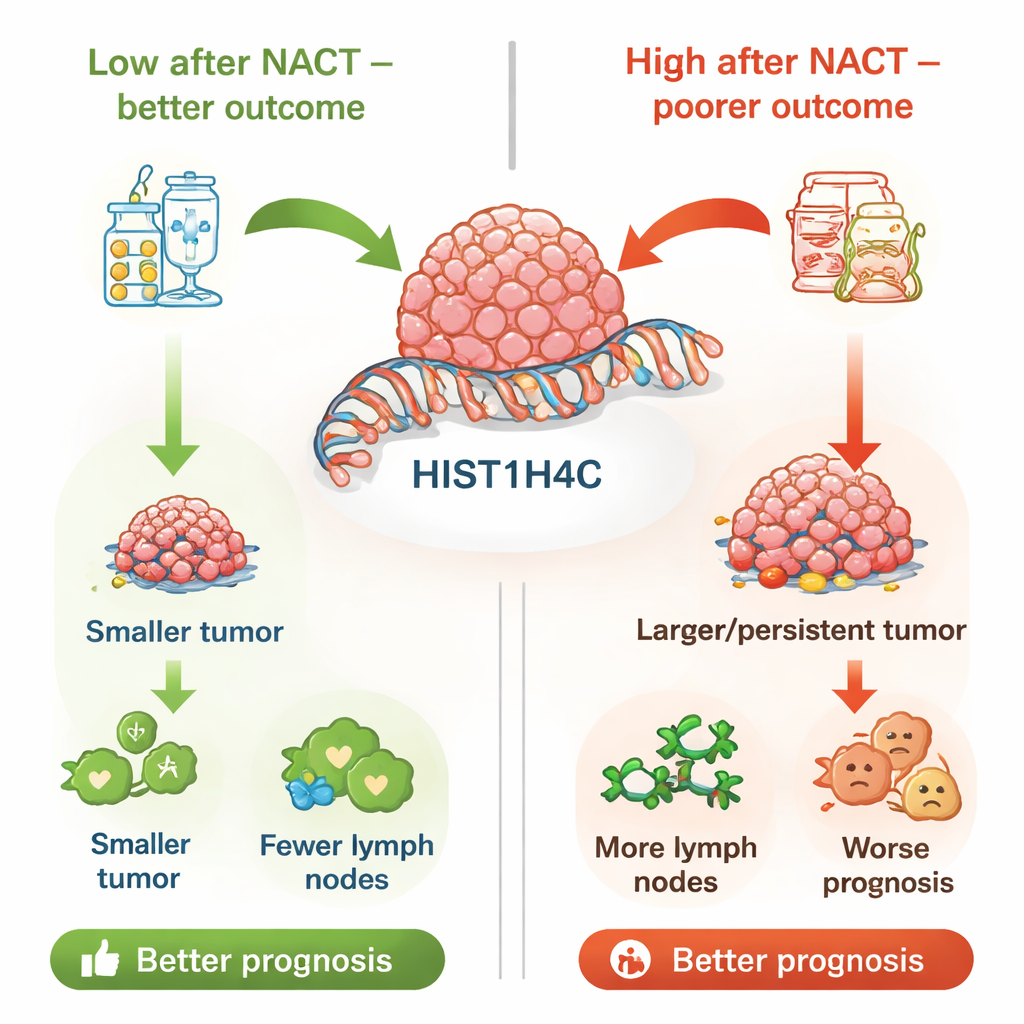
将基因水平与长期预后相连
为检验这些发现是否在更大范围内成立,作者分析了一个大型公开乳腺癌数据库(Curtis 数据库)。在该数据库中,高 HIST1H4C 表达同样与更高的肿瘤分级、更大的肿瘤、更多的淋巴结转移以及不良肿瘤类型(如三阴性和激素受体阴性)相关。最重要的是,在这个外部数据集中,HIST1H4C 水平较高的患者生存期更短。综合医院队列与大数据分析,两者都指向 HIST1H4C 作为更具侵袭性疾病和较差预后的标志,尤其是在治疗后其水平仍然偏高时。
走向更个性化的治疗决策
对外行人而言,关键信息是对肿瘤组织中 HIST1H4C 进行的简单实验室检测,有朝一日可能帮助医生更好地将新辅助治疗与个体患者匹配。治疗前高 HIST1H4C 可能提示肿瘤更具侵袭性但也更易对化疗缩小,而治疗后持续偏高的 HIST1H4C 则可能预示更高的复发风险,需要更密切的随访或额外治疗。因为该检测基于许多医院已常用的标准基因表达方法,作者认为它有望成为一种实用且具成本效益的工具,尤其在资源有限的环境中。尽管仍需进一步验证,但这项工作表明,解读肿瘤 DNA 的“包装”可以提供有力线索,帮助判断哪些乳腺癌会对术前治疗产生反应以及患者长期可能的结局。
引用: Qian, L., Ge, R., Haihu, Z. et al. Evaluating the prognostic significance of HIST1H4C in breast cancer: implications for neoadjuvant therapy. Sci Rep 16, 6792 (2026). https://doi.org/10.1038/s41598-026-36983-4
关键词: 乳腺癌, 新辅助化疗, 生物标志物, HIST1H4C, 治疗反应