Clear Sky Science · zh
元动力学揭示黄酮浣铃素通过构象稳定性对抗对阿伐普替尼耐药的PDGFRα D842V/G680R GIST
这对癌症治疗为何重要
靶向抗癌药物在很多情况下效果显著——直到肿瘤进化出逃避它们的方式。本文探讨了一种常见植物化合物浣铃素(luteolin)如何可能帮助恢复一种用于某些胃肠道间质瘤(GIST)的重要药物的疗效。这类肿瘤是消化道的癌症。研究者通过先进的计算模拟展示了浣铃素如何稳固癌细胞中一个变形的蛋白,使现有药物能够再次结合,提示了一种在不从零开始重新设计治疗方案的情况下对抗药物耐受性的新思路。 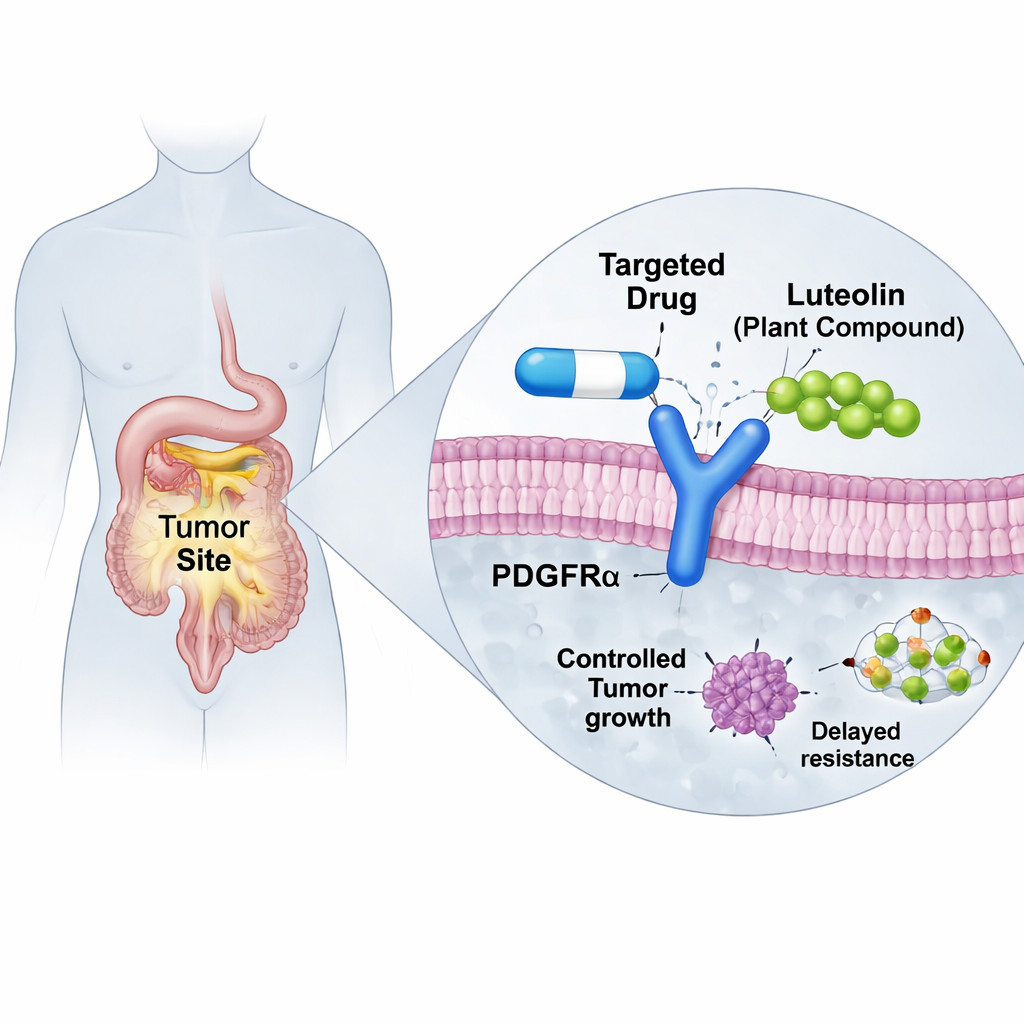
肿瘤学会躲避药物的问题
GIST通常由于细胞表面蛋白KIT或PDGFRα的“开启开关”出错而生长,这些开关驱动持续的生长信号。设计用来关闭这些开关的现代小分子——酪氨酸激酶抑制剂——已经改变了许多患者的预后。但PDGFRα中的一个常见突变D842V使得较早的药物伊马替尼大多失效。新一代药物阿伐普替尼(avapritinib)正是为抑制这一顽固突变而设计,并在临床试验中取得了显著成功。不幸的是,肿瘤仍能继续适应。有些患者在PDGFRα上出现额外改变,例如继发性的G680R突变,这一改变在空间上阻挡了阿伐普替尼舒适地嵌入其结合口袋,导致药物脱落并诱发耐药。
一种形状有趣的植物分子
天然产物是药物创意的丰富来源,类黄酮——存在于许多水果、蔬菜和药用植物中的色素化合物——已知能与细胞内的生长调控蛋白相互作用。浣铃素是一种存在于地中海灌木Retama monosperma中的类黄酮,已被研究其抗癌和抗炎特性,并且在口服补充剂可达到的剂量下表现出可接受的安全性。基于早期筛选工作,作者怀疑浣铃素可能会黏附在PDGFRα的一个靠近但不重叠常规模药结合位点的位置。如果属实,浣铃素可能像一个微妙的支撑,推动蛋白进入一种再次欢迎阿伐普替尼的构象。
模拟分子间的协作
为在计算机中检验这一想法,团队构建了携带D842V和G680R双突变的耐药PDGFRα蛋白的详细三维模型。他们模拟了阿伐普替尼单独存在时的行为以及浣铃素在附近存在时的行为,追踪数百纳秒内的原子运动——在真实时间上相当于十亿分之一秒。当只有阿伐普替尼结合时,随着体积较大的G680R改变将其推出,药物逐渐从结合口袋中漂移出来,最终完全从蛋白上脱落。相比之下,当浣铃素也在一个独立的“变构”位点(靠近关键螺旋)结合时,阿伐普替尼在很大程度上保持在位。整体蛋白的弯曲较少,关键结构片段保持形状,药物与蛋白之间的重要接触持续时间显著延长。 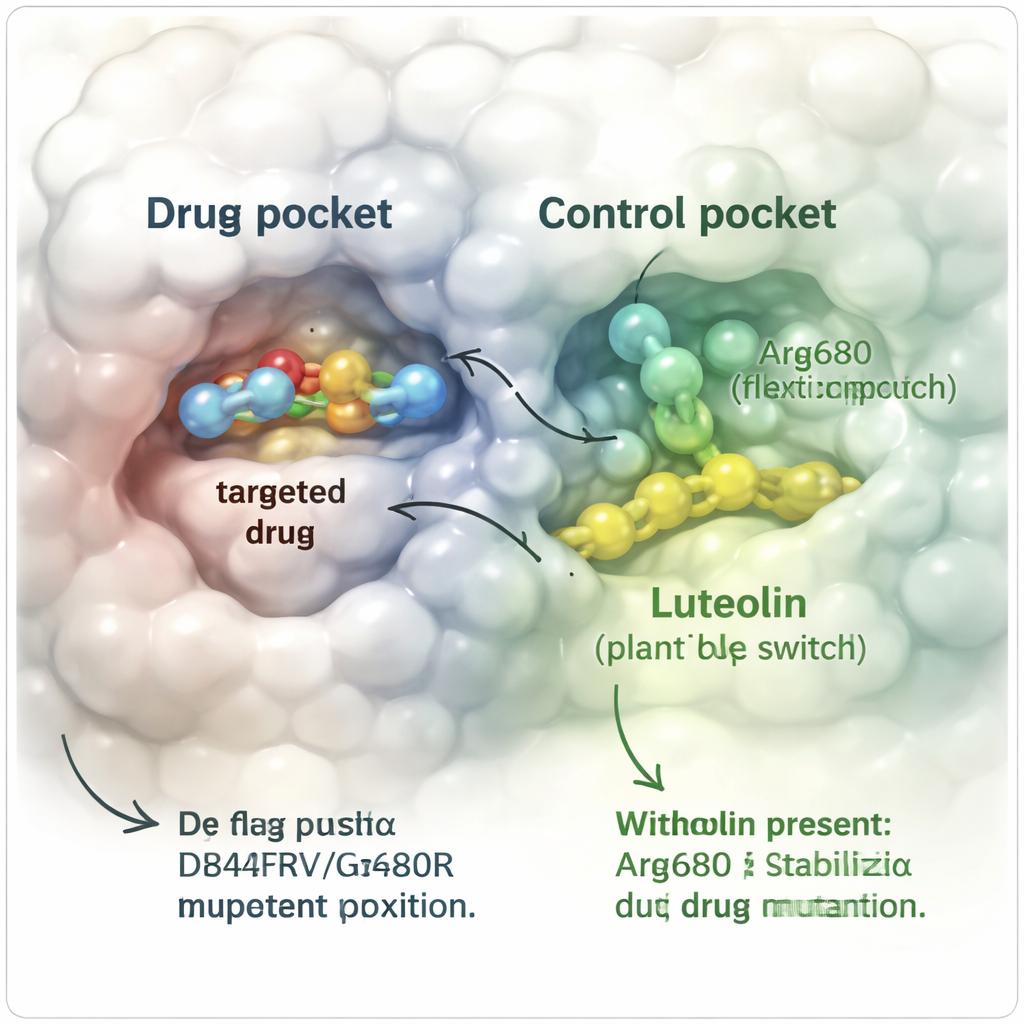
钉住一个任性的分子开关
常规模拟仍可能错过罕见但重要的构象变化,因此研究者采用了一种增强方法——元动力学(metadynamics)来更全面地探索蛋白可能的扭转与弯曲行为。他们聚焦于被改变的氨基酸Arg680的行为,该残基像一个位于药物口袋附近的小灵活臂。没有浣铃素时,这只“臂”取样许多位置,药物容易滑走,且逃逸的能量障碍相对较低。当浣铃素在位时,Arg680被固定在一种不再与药物冲突的特定取向。能量景观发生了变化:体系更偏好于阿伐普替尼保持结合的构象,药物要脱离所需越过的能量“坡”增加了数千卡路里(kilocalories)量级,使得解离的可能性大大降低。
这对患者可能意味着什么
简而言之,这项研究表明浣铃素可能像分子夹板一样,稳固一个变形的癌症蛋白,从而让已有的靶向药物再次抓住它。与其为每一种耐药突变设计全新的药物,不如将现有药物与经精心挑选的辅助化合物配对,可能恢复其疗效。这项工作基于强大的但纯粹的计算方法,因此仍需实验室和动物研究来确认浣铃素或经改造以具备更好药物性状的相关分子是否在生物体系中真正增强阿伐普替尼的作用。尽管如此,使用小分子变构助剂重新稳定耐药癌症靶点的概念,可能为延长当今精准疗法寿命开辟一条新路径。
引用: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
关键词: 药物耐药, 胃肠道间质瘤, 酪氨酸激酶抑制剂, 浣铃素, 变构调节