Clear Sky Science · zh
4-壬基酚通过 MEG3/PI3K/AKT 信号通路调控宫颈癌细胞增殖与凋亡
日常化学物质与女性癌症风险
我们周围充斥着来自塑料、洗涤剂和农药的化学物质,它们能够在体内表现出类激素作用。本研究探讨了其中一种化合物 4‑壬基酚(4‑NP)是否可能促进宫颈癌的发展,以及细胞内一种天然保护分子 MEG3 如何进行反制。理解二者关系有助于寻找降低环境污染风险的新方法,并为宫颈癌设计更明智的治疗策略提供线索。
显微镜下的常见污染物
4‑NP 广泛用于工业产品中,可能渗入水体、土壤,最终进入人体。它具有一定的雌激素样作用,与生殖系统问题有关。研究人员首先提出一个简单问题:宫颈癌患者体内是否含有更高水平的该化学物质?通过检测 35 名宫颈癌女性和 35 名健康女性的尿液中 4‑NP 水平,他们发现患者体内的 4‑NP 平均几乎高出六倍。这并不能证明该化学物质致癌,但表明患宫颈癌的女性通常暴露水平显著更高。
机体内建的制动器:MEG3
在细胞内,不编码蛋白质的长链 RNA 仍能控制细胞的生长与死亡。其中一种名为 MEG3 的长链非编码 RNA 通常充当抑制肿瘤生长的“刹车”。研究团队比较了 31 例患者的宫颈癌组织与邻近正常组织,发现肿瘤中 MEG3 水平显著降低。细胞实验也显示了同样的模式:宫颈癌细胞系(HeLa)中的 MEG3 少于正常宫颈细胞,且在暴露于 4‑NP 后,MEG3 随时间进一步下降。这提示肿瘤本身与环境中 4‑NP 暴露可能协同使这一天然肿瘤抑制信号沉默。
当制动器被恢复
接着,科学家们测试了如果强迫癌细胞产生更多 MEG3 会怎样。通过病毒载体在 HeLa 细胞中增强 MEG3 表达,他们观察到细胞增速放慢。癌细胞分裂减少,在培养皿中的迁移变得迟缓(表明侵袭能力降低),并更容易发生程序性细胞死亡(凋亡)。细胞周期检测显示 MEG3 使细胞在复制 DNA 之前停滞,作为限制增殖的另一种方式。在小鼠模型中,由增强 MEG3 的 HeLa 细胞形成的肿瘤比普通癌细胞形成的肿瘤明显更小、更轻,证实 MEG3 在体内也能抑制肿瘤生长。
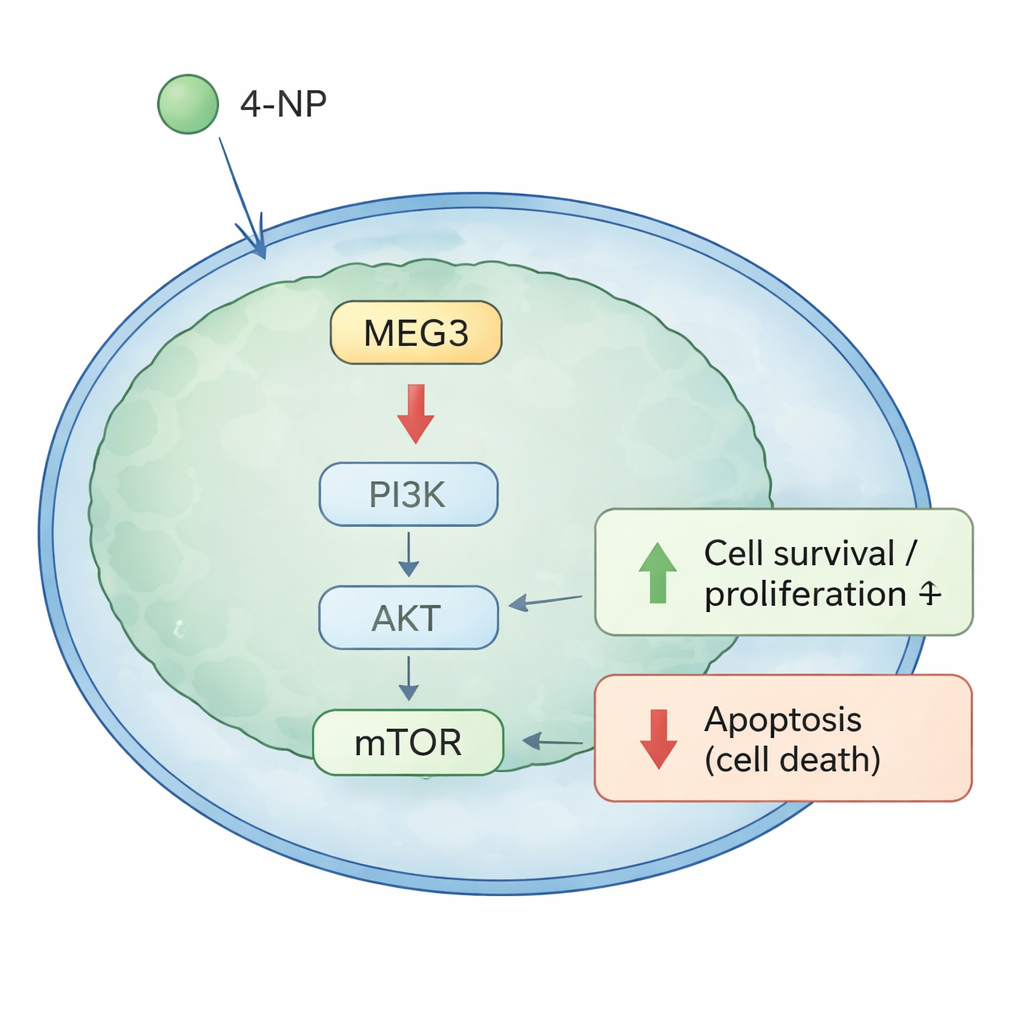
癌细胞内的生长开关
为弄清 MEG3 如何发挥作用,研究者们将注意力集中在细胞内一个广为人知的生长开关——PI3K/AKT 通路上。当该通路活跃时,细胞倾向于生长和存活;当其被抑制时,细胞更易走向死亡。在细胞培养与小鼠肿瘤中,增强 MEG3 降低了 PI3K、AKT 与 mTOR 的活性(磷酸化形式),并减少了保护细胞免于死亡的 BCL‑2 水平,同时有利于促死亡信号。相比之下,暴露于 4‑NP 则产生相反效果:促进生长和存活信号、减少细胞死亡。重要的是,当 MEG3 被恢复后,它在很大程度上逆转了 4‑NP 的促生长、抑凋亡效应,表明该 RNA 是环境暴露与癌细胞行为之间的关键介质。
这对患者与预防意味着什么
对非专业读者而言,结论是:一种常见的环境化学物质在宫颈癌患者体内呈现较高暴露水平,并且在实验室中能够推动癌细胞更快生长、减少死亡。细胞内的天然分子 MEG3 通过抑制一个强大的生长通路发挥保护作用。尽管该研究无法证明 4‑NP 必然引发宫颈癌,且样本量与模型存在局限,但它揭示了一条新的事件链:4‑NP 降低 MEG3,进而释放生长开关、助力肿瘤生长。未来同时监测 4‑NP 水平与 MEG3 活性可能有助于评估环境风险,恢复 MEG3 或阻断同一路径的治疗策略或为宫颈癌患者提供新的治疗选择。
引用: Wu, W., Ren, X., Chen, Y. et al. 4-Nonylphenol regulates cell proliferation and apoptosis in cervical carcinoma through the MEG3/PI3K/AKT signaling pathway. Sci Rep 16, 6067 (2026). https://doi.org/10.1038/s41598-026-36863-x
关键词: 宫颈癌, 环境污染物, 4-壬基酚, 长链非编码 RNA MEG3, PI3K AKT 通路