Clear Sky Science · zh
SARS-CoV-2 主蛋白酶抑制剂 VPC285785 在小鼠冠状病毒感染模型中的药代动力学、病理学与疗效
为什么我们仍然需要更好的 COVID 药丸
首批用于 COVID-19 的抗病毒口服药,如 Paxlovid,曾是抗疫的重要转折点。但它们并不完美:必须在极早期服用,每天需要多片药物,并且可能与其他药物发生危险的相互作用。本研究探讨了新型药物候选物,旨在通过多重作用阻断冠状病毒,可作为单片口服给药并降低药物-药物相互作用风险,研究采用小鼠冠状病毒感染模型进行评估。
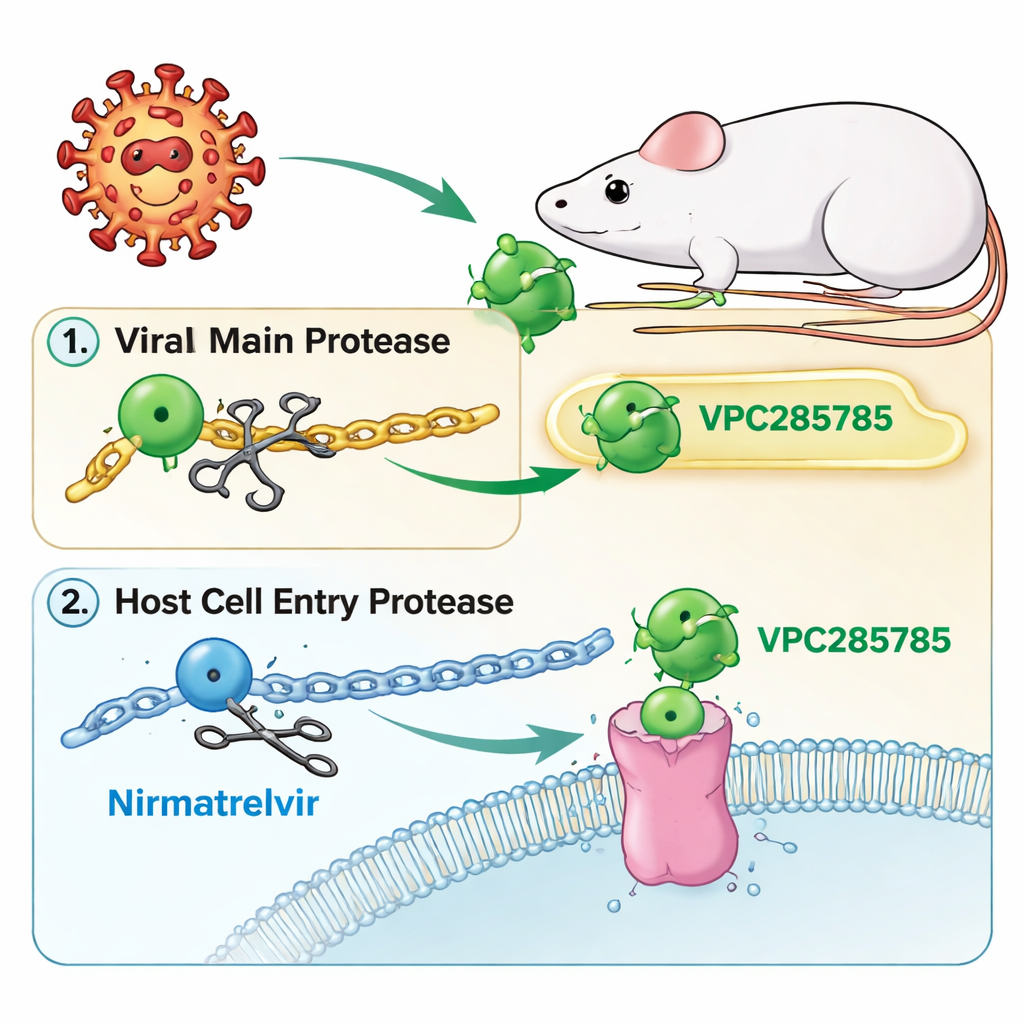
对 COVID-19 蛋白酶靶点的新思路
与 Paxlovid 类似,新化合物 VPC285785 与 VPC285786 以病毒的“主蛋白酶”为靶点,该酶像分子剪刀一样将长的病毒蛋白切割成能工作的片段。如果这把剪刀被卡住,病毒就无法完成组装并会停滞。研究者还将分子设计为同时作用于宿主细胞中的另一个蛋白——猫肽酶 L(cathepsin L),后者有助于某些冠状病毒进入细胞。通过同时瞄准病毒的剪刀和宿主的入侵辅助因子,团队希望开发出一种双重作用的口服药,使病毒更难产生耐药性,并且不需要助推药物。
为了持久性而设计,而非依赖助推药
Paxlovid 将 nirmatrelvir 与另一种药物 ritonavir 联合使用,ritonavir 的作用不是直接抗病毒,而是减缓 nirmatrelvir 在肝脏中的分解。然而 ritonavir 会干扰处理常见药物的多种酶,导致复杂且有时危险的药物相互作用。VPC285785 与 VPC285786 在化学上经过调节,使其自身更能抵抗代谢分解,采用了如氟原子引入和环状“加固”等特性,使其对肝脏酶的吸引力降低。在人体与小鼠的肝制剂体外试验中,两种新化合物的稳定性至少与 nirmatrelvir 相当,而 VPC285786 在某些方面甚至更为稳固,且未使用任何 ritonavir 的情况下仍表现出良好稳定性。
这些药物在小鼠体内的行为与分布
研究团队随后考察了这些化合物在小鼠体内的分布情况,测量它们在血液中消失的速度以及口服吸收率。注射给药后,VPC285785 与 VPC285786 在血液中的停留时间与 nirmatrelvir 相仿,并且总体暴露量更高。然而口服给药时,两者表现不同:VPC285785 达到中等但可接受的吸收率(约 15% 的吞服剂量进入循环),而 VPC285786 几乎未进入血液(约 3%)。由于口服药需通过肠壁进入血液才能作为实用治疗药物,仅有 VPC285785 被推进到感染实验中。
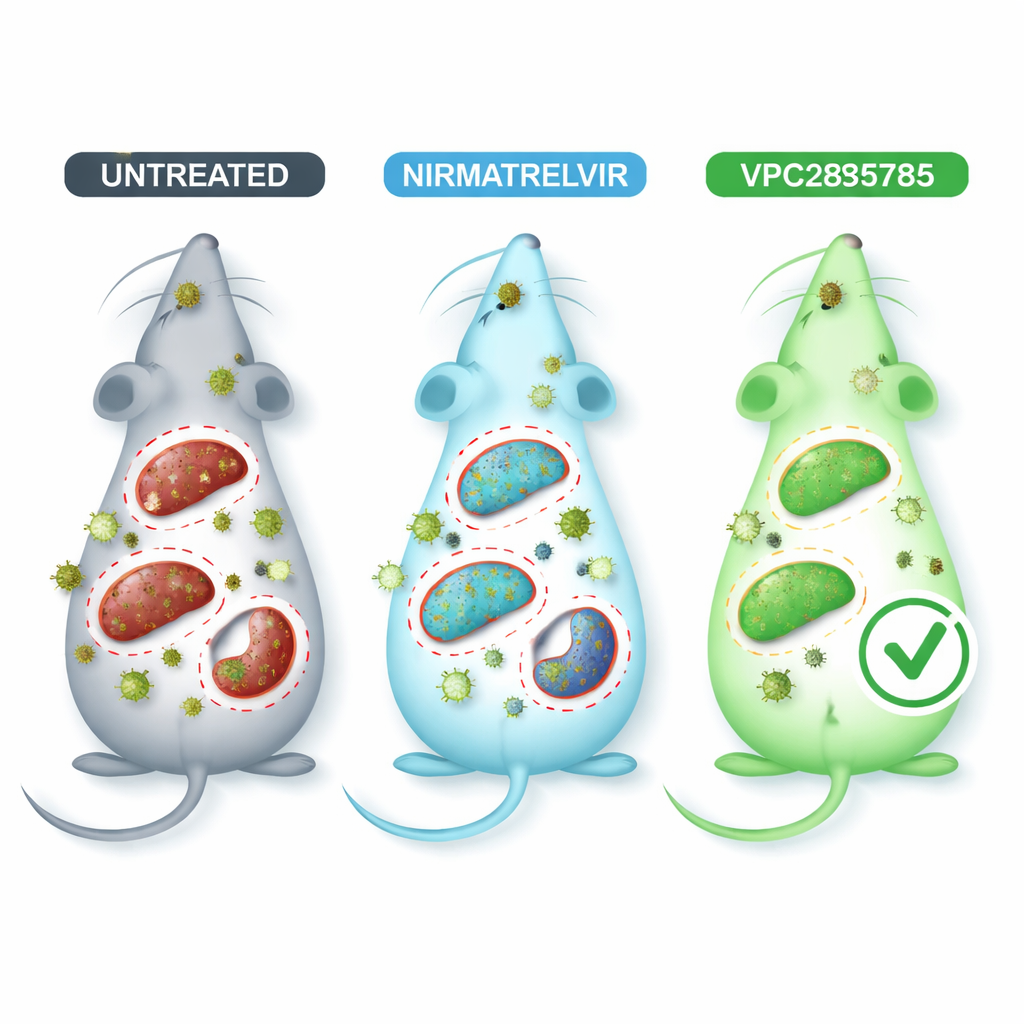
在感染小鼠中检验新药丸
为在更安全的条件下模拟冠状病毒疾病,研究者使用了一种名为 MHV-A59 的小鼠冠状病毒,该病毒侵袭多器官并在许多方面引起类似于人类感染的肺与肝损伤。受感染的小鼠通过口服给予 VPC285785,比较组给予 nirmatrelvir 或无活性载体。血液检查显示感染对肝肾造成压力,但接受 VPC285785 或 nirmatrelvir 处理的动物在肝酶与肾功能指标上通常优于未治疗的动物。最显著的是,VPC285785 显著降低了肝脏、脑和脾脏中的病毒遗传物质量,而 nirmatrelvir 仅在脑中产生了明显下降。在所测条件下,肺、心脏与肾脏中两种治疗均未显示出强烈效果。
这对未来 COVID 治疗意味着什么
尽管 VPC285785 在体外对病毒蛋白酶的抑制活性不如 nirmatrelvir,但其在活体动物中表现良好,显著降低多处重要器官的病毒含量并保护器官功能,且无需 ritonavir 助推。其姐妹化合物 VPC285786 表明可实现对病毒蛋白酶与猫肽酶 L 更强的双重靶向,但其较差的口服吸收仍需改进。总体来看,这些结果表明下一代 COVID 口服药有望被设计为单一、可口服的药物,同时作用于病毒与宿主目标,降低与其他药物发生危险相互作用的风险,并在关键组织中提供强有力的保护。
引用: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
关键词: SARS-CoV-2 抗病毒药物, 主蛋白酶抑制剂, Paxlovid 替代品, 小鼠冠状病毒模型, 口服 COVID 治疗