Clear Sky Science · zh
冷等离子体设备对DNCB诱导的特应性皮炎治疗效果的临床前研究
为老问题带来新光
特应性皮炎,常被称为湿疹,影响数以百万计的儿童和成人,引起皮肤干燥、发红和剧烈瘙痒。尽管药膏和免疫抑制药物能起到缓解作用,但它们可能带来副作用或随时间丧失疗效。本研究探讨一种不同寻常且无需注射的方法:用温和的“冷”等离子体——一种可在空气中产生的能量化气体——处理小鼠的类湿疹皮肤,观察它是否能抑制炎症并帮助恢复皮肤的天然屏障。
以柔光代替药丸
等离子体有时被称为物质的第四态,当气体被激发时,会产生带电粒子、反应性分子和微弱光。研究团队测试了三种在室温下产生冷大气等离子体的小型装置:氦气射流、氩气射流和一种基于空气的平面装置,称为浮动电极介质阻挡放电(FE-DBD)。这些工具不会切割或灼伤皮肤;它们只是短时间用反应性分子“洗浴”皮肤。研究者想知道,这些产生略有不同反应性粒子组合的不同设备,是否在类湿疹皮肤上显示出不同的愈合效果。
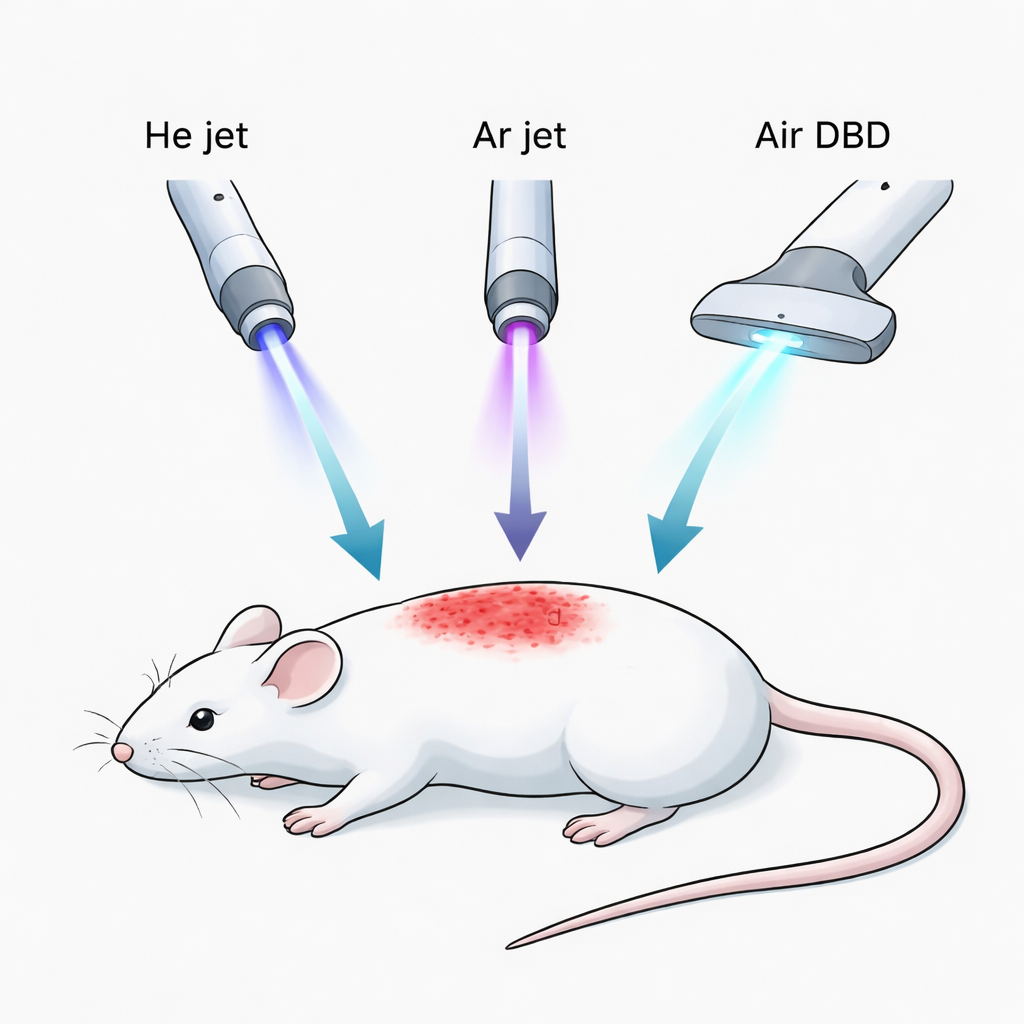
在小鼠身上建立类湿疹模型
为了模拟特应性皮炎,科学家在雌性小鼠背部剃毛皮肤上反复涂抹一种名为DNCB的化学物质,这是一种成熟的建模方法。这会诱发干燥、鳞屑、发红和受损的斑块,类似人类湿疹,同时伴随典型的内部变化,如皮肤层增厚、血管增生以及免疫细胞和与瘙痒及过敏相关信号的激增。疾病建立后,小鼠被分组,分别接受为期一周的每日氦等离子体、氩等离子体、空气等离子体、标准处方软膏(他克莫司)或不接受主动治疗。整个研究期间,研究人员仔细评分可见的皮肤损伤,并用显微镜和分子学检测检查组织样本。
皮肤对等离子体的反应
结果显示,并非所有等离子体的疗效都相同。接受氦和氩气射流处理的小鼠在可见改善方面最为显著:发红、脱屑和开放性溃疡减少,总体皮炎严重度评分低于未治疗动物。在显微镜下,这些组在表皮和真皮两层的损伤减少,在许多情况下与他克莫司软膏的效果相当甚至更好。相比之下,空气等离子体在这些结构学指标上仅表现出温和的改善。三种等离子体都使异常增厚的表皮变薄,但空气等离子体在缩小该厚度方面尤为有效,提示不同气体类型可能针对疾病的不同方面。
平息血管和免疫信号
除了表观变化,研究团队还探究了等离子体对皮肤生物学的影响。湿疹由过度活跃的免疫信号和微小血管的改变推动。在DNCB处理的小鼠中,用于标记血管增生的蛋白CD31升高,反映出与发红和肿胀相关的血管增多且渗漏。等离子体治疗将CD31水平降低,尤其是氦等离子体,其降幅与药物软膏相当。等离子体还提升了E-钙黏蛋白(E-cadherin),这是一种关键的黏附蛋白,有助于相邻皮肤细胞紧密连接以维持对刺激物和病原体的屏障。同时,基因检测显示,所有等离子体处理,尤其是氦和氩气射流,显著降低了与瘙痒、过敏和慢性炎症相关的炎症信使分子IL-13、IL-31和IL-12的表达。氩气和空气等离子体还减少了肥大细胞的数量——这些免疫细胞会驱动瘙痒和发作——而氦对该细胞类型的影响较小。
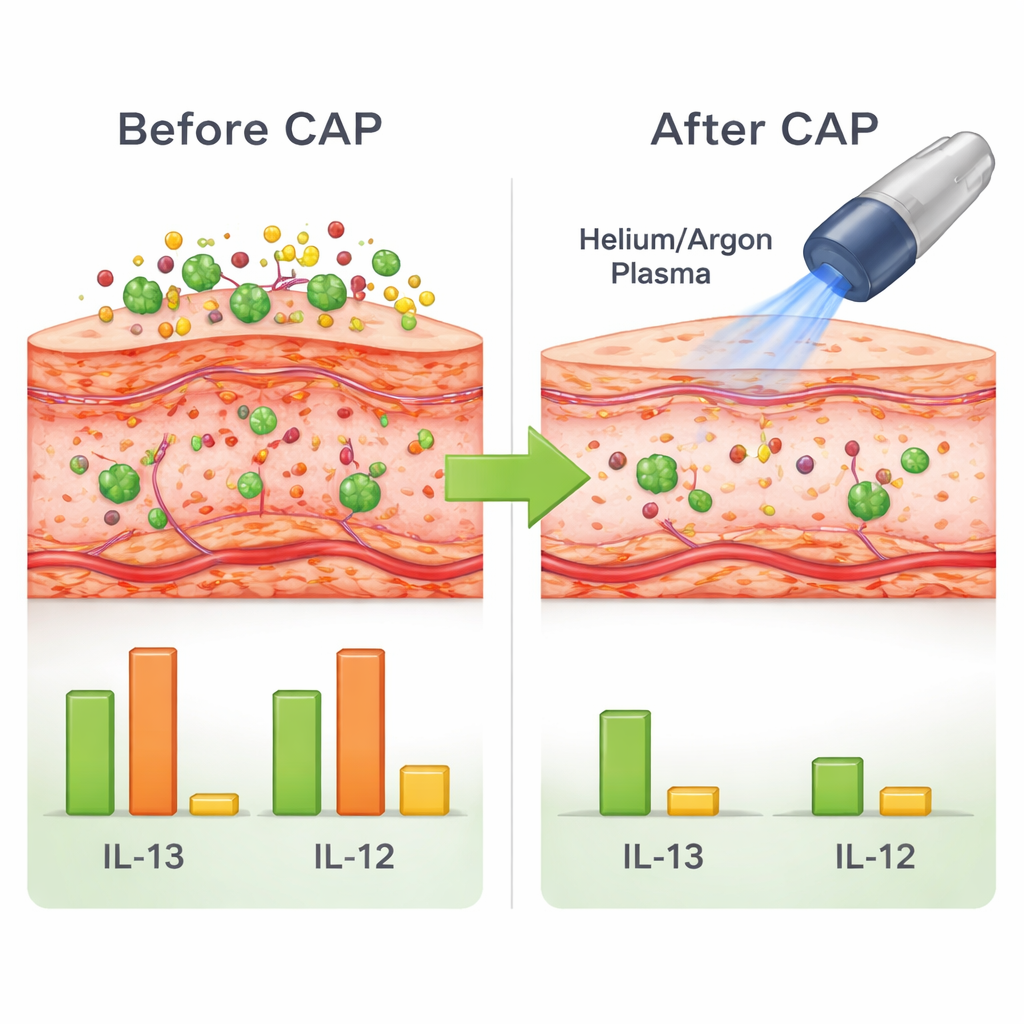
这对未来治疗可能意味着什么
综合来看,这些发现表明,可控剂量的冷大气等离子体不仅能清洁皮肤表面:它们可以缓解炎症、使血管生长恢复正常、加强皮肤的结构性“砂浆”,并降低在类湿疹状态中驱动瘙痒和过敏的关键信号。在这项小鼠研究中,氦气和氩气射流在多项皮肤健康指标上与标准处方软膏表现相当或更佳,而基于空气的装置则稍逊一筹。该研究尚不能证明此类等离子体治疗在人类湿疹中安全有效,但为进一步研究和未来的临床试验提供了有力依据,以评估这种冷而发光的气体是否可能成为对抗慢性瘙痒性皮肤病的新工具。
引用: Shakeri, F., Mehdian, H., Bakhtiyari-Ramezani, M. et al. A preclinical study of device dependent therapeutic effects of cold atmospheric plasmas on atopic dermatitis induced by DNCB. Sci Rep 16, 6697 (2026). https://doi.org/10.1038/s41598-026-36821-7
关键词: 特应性皮炎, 冷大气等离子体, 湿疹治疗, 皮肤炎症, 等离子体医学