Clear Sky Science · zh
白介素调节卵巢癌细胞的脂质代谢与铁死亡:通过调控 ALOX5–5‑HETE–PD‑L1 轴
为何这种植物分子对卵巢癌重要
卵巢癌是女性中最致命的癌症之一,原因在于通常发现较晚且常在治疗后复发。本研究探讨一种名为天花粉苷(tectorigenin)的天然化合物——存在于黄栀子(Belamcanda chinensis)中的成分——是否能通过剥夺肿瘤细胞的特定脂质并促使其进入一种依赖铁的细胞死亡方式来抑制卵巢癌。同时研究也考察了该化合物是否能削弱肿瘤用以逃避免疫监视的“隐身斗篷”。
肿瘤细胞内部的隐秘燃料来源
像许多癌症一样,卵巢肿瘤重塑了脂质代谢。癌细胞不仅将脂质用于能量,还将其囤积为新膜的构件并作为抵御损伤的缓冲。在体外培养的卵巢癌细胞中,外加单不饱和脂肪酸会导致游离脂肪酸、三酸甘油酯和胆固醇——这些关键的储脂形式——的积累。脂质过剩促进了细胞的生长和侵袭能力,并帮助其抵抗一种称为铁死亡(ferroptosis)的破坏性过程,在该过程中铁与受损脂质结合导致细胞膜破裂。换言之,异常的脂质代谢为癌细胞提供了生长优势和生存屏障。
将癌细胞推向自我毁灭
研究者随后对正常卵巢细胞和多株卵巢癌细胞系进行了天花粉苷的测试。在最高 200 微克/升的剂量下,该化合物对正常细胞无明显伤害,但明显抑制了癌细胞的增殖、降低了其穿膜侵袭能力并提高了程序性细胞死亡率。当癌细胞预处理以阻断铁死亡的药物时,它们表现得更具侵袭性。加入天花粉苷可以逆转这些效应:脂质储备减少、与铁和氧化相关的损伤标志物上升、细胞死亡增加。在携带人类卵巢肿瘤的小鼠模型中,注射天花粉苷使肿瘤缩小、肿瘤组织中的脂质含量下降,并增强了铁死亡的化学学标志,进一步表明该化合物能促使癌细胞走向这一依赖铁的死亡途径。
连接脂质与免疫逃逸的关键分子开关
为揭示天花粉苷在分子水平的作用机制,团队将大数据挖掘与药物–蛋白相互作用的计算建模相结合。研究锁定在一种名为 ALOX5 的酶上,该酶可将常见脂肪酸转化为一种信号分子 5‑HETE。在卵巢癌细胞和肿瘤样本中,ALOX5 的表达水平显著高于正常组织。计算对接和分子动力学模拟表明,天花粉苷能够稳固地结合 ALOX5,起到类似内部制动器的作用。当研究者在癌细胞内人为上调 ALOX5 时,脂质储备增加、铁死亡标志下降、细胞侵袭性增强。天花粉苷处理能逆转这些变化。敲低 ALOX5 则产生相反效应——脂质减少、铁死亡增加、生长能力减弱——明确将该酶置于该化合物作用的核心。
肿瘤如何失去对免疫系统的“护盾”
研究还将该脂质通路与一个重要的免疫检查点分子 PD‑L1 联系起来,肿瘤通过该分子关闭攻击性的免疫细胞。ALOX5 的产物 5‑HETE 能提升 PD‑L1 水平,强化这层护盾。当沉默 ALOX5 时,5‑HETE 和 PD‑L1 水平同时下降;当重新引入 5‑HETE 时,PD‑L1 再次上升,癌细胞对铁死亡的保护也部分恢复。天花粉苷在细胞培养和小鼠肿瘤中降低了 ALOX5、减少了 5‑HETE,并继而降低了 PD‑L1。这提示通过靶向单一代谢酶,该化合物既能破坏癌细胞基于脂质的防御,又能削弱其躲避免疫攻击的能力。
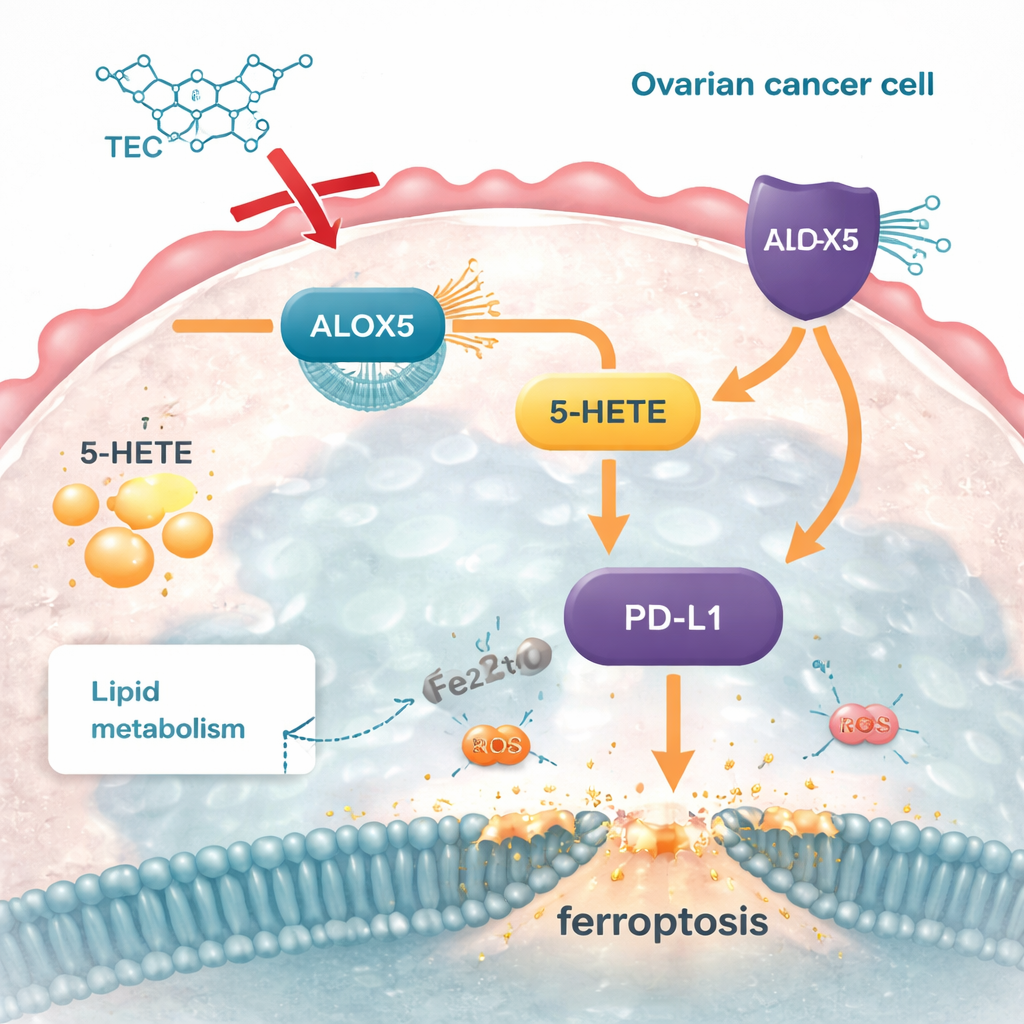
这对未来治疗意味着什么
简言之,该研究表明天花粉苷像一把精确的扳手,被投入癌细胞的脂质处理机器中。通过抑制 ALOX5,它切断了 5‑HETE 的生成,减少了过剩脂质储备,使细胞对铁介导的损伤更脆弱,并剥离了其部分免疫伪装。尽管这些发现来自细胞和小鼠研究——在人类中的有效性仍需大量验证——但它们指向一种有前景的策略:靶向 ALOX5–5‑HETE–PD‑L1 轴,既饿死卵巢肿瘤,也使其更易被机体自身防御或未来的免疫治疗清除。
引用: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
关键词: 卵巢癌, 脂质代谢, 铁死亡, ALOX5, 天然化合物治疗