Clear Sky Science · zh
HTG 与 TempO-Seq 靶向转录组分析方法的比较评估
这对癌症护理意味着什么
当医生和科学家研究癌症时,常常关注细胞的“信息分子”——RNA——以判断哪些基因处于活跃或沉默状态。这些模式可以揭示肿瘤的行为以及哪些治疗可能最有效。但大多数医院样本在福尔马林处理后存入石蜡包埋块,这会损坏脆弱的 RNA。该研究提出了一个具有重大影响的实际问题:在一种广泛使用的 RNA 检测方法从市场上消失后,较新的方法能否接替并从这些常规保存的样本中提供同样有用的结果?
两种读取基因活性的工具
多年来,许多实验室依赖一种称为 HTG EdgeSeq 人类转录组面板(HTP)的方法,从福尔马林固定石蜡包埋(FFPE)组织的微量刮取样本直接读取基因活性。这种方法几乎可以对全部人类基因进行调查,无需先提取 RNA,从而节省时间并保留宝贵的材料。然而,HTG EdgeSeq 背后的公司破产,研究人员不得不寻找替代方案。另一家厂商的新技术 TempO-Seq(TOS)承诺具备类似能力:它同样同时靶向大量基因,能处理来自 FFPE 样本的受损 RNA,并被设计为灵敏、可重复且相对经济。
将方法付诸考验
研究团队在一个非常务实的情境中对这两种技术进行了直接比较。他们分析了 21 例保存的子宫内膜癌样本,以及三种标准 RNA 参考材料,先用 HTG HTP 再用 TempO-Seq 进行测定。两种方法使用的靶向面板合计覆盖了 18,000 多个相同基因。科学家们施加了严格的质量控制,确保每个样本产生足够的测序读取并且测量稳定。他们还使用统计工具去除“批次效应”——由于在不同日期、仪器或平台上运行测试而产生的人工差异。
哪些一致、哪些不一致
当团队逐个基因地比较表达时,两种方法并不总是完全一致。每种技术在探针设计、样本制备和读取计数上的差异会使单基因比较产生噪声。然而,当他们检查结合多基因信息的更广泛模式时,情况发生了变化。多基因特征——例如用于将肿瘤分入分子亚型、估算样本中免疫细胞数量或推测肿瘤纯度的那些——在 TempO-Seq 与 HTG 之间表现出更强的一致性。在大多数情况下,即使研究者通过模拟较少的测序读取量来模拟不同仪器容量,得分或分类仍然相似。
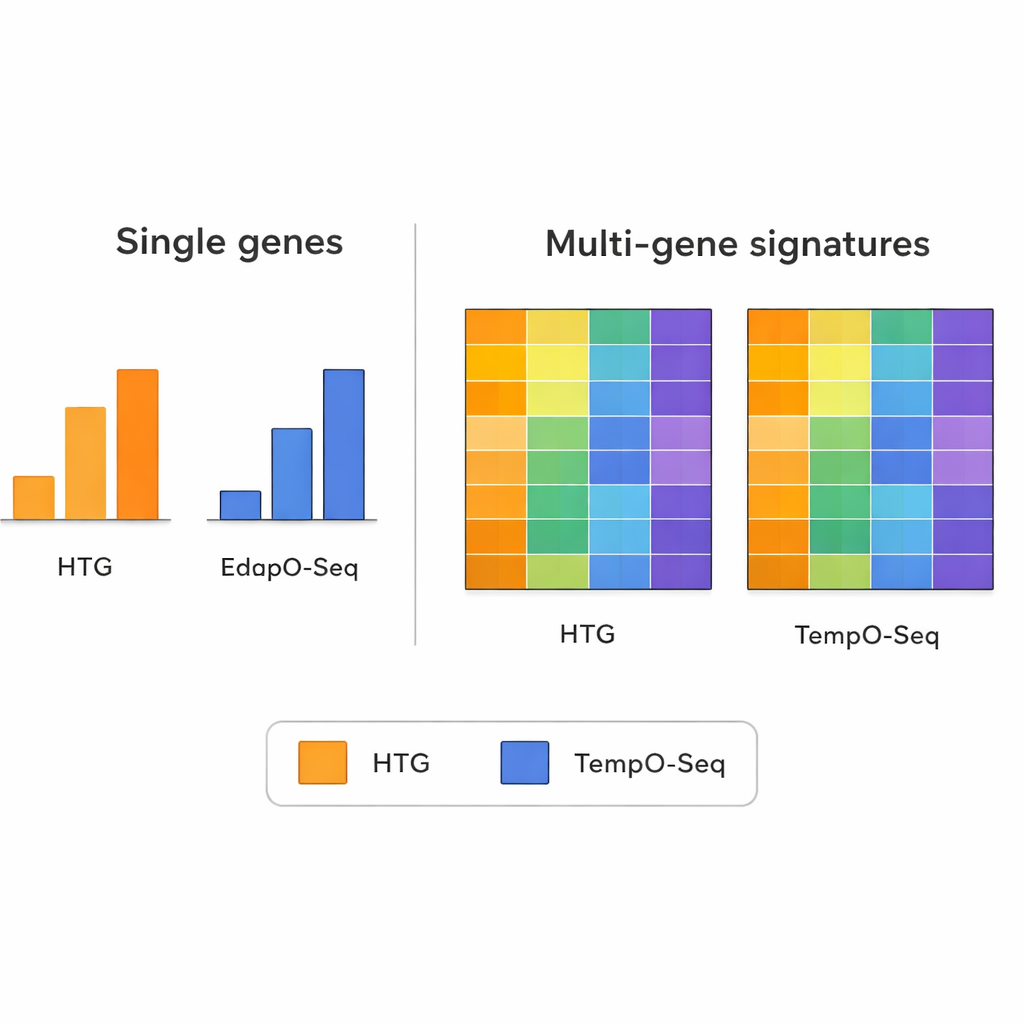
多基因模式作为可靠信号
该研究强调了现代基因组学中的一项重要原则:尽管单个基因的测量可能被技术性问题干扰,但将数十或数百个基因的信号合并通常能够平均掉这些噪声。作者使用了几种广为人知的多基因工具作为技术压力测试。这些工具包括一个将乳腺癌肿瘤归入内在亚型的面板、一个评估样本中免疫与结缔组织混入程度的算法,以及一种估算多种免疫细胞比例的方法。在这些复杂读数中,TempO-Seq 通常与 HTG 密切一致,表明即便某些细节存在差异,它也捕捉到了相同的生物学信息。
对未来的意义
对于依赖 FFPE 档案研究癌症的研究人员来说,失去一个可靠平台本可能是一次重大挫折。本次基准研究带来安慰:当目标是使用多基因生物标志物和广泛的表达模式——这些正是许多现代诊断与预后工具的基础——TempO-Seq 似乎是 HTG HTP 的可靠替代。作者提醒,直接跨平台比较单基因结果并不明智,因为每种方法以略有不同的方式靶向基因。相反,他们建议在跨平台工作时侧重于复杂的多基因特征。通俗地说,对于大多数真实世界的肿瘤学研究需求,尤其是研究者关心许多基因的整体模式而不是单个基因的确切数值时,新方法似乎能够承担起其前任的工作。
引用: Fernández-Serra, A., López-Reig, R., Romero, I. et al. Comparative evaluation of HTG and TempO Seq targeted transcriptome profiling methods. Sci Rep 16, 6108 (2026). https://doi.org/10.1038/s41598-026-36810-w
关键词: 转录组分析, 子宫内膜癌, FFPE 组织, 靶向 RNA 测序, 基因表达生物标志物