Clear Sky Science · zh
编码于前噬菌体的RexAB型噬菌体防御系统在假单胞菌Pseudomonas putida中的作用
隐藏在细菌体内的保镖
细菌不断受到被称为噬菌体的病毒猎杀,噬菌体能摧毁整个微生物群体。本研究考察了“沉睡”状态、已隐匿在细菌DNA中的病毒如何悄悄充当保镖,通过牺牲受感染的细胞来拯救其余细胞。理解这些天然防御策略对应噬菌体疗法、生物技术乃至维持工业用微生物稳定性都具有重要意义。
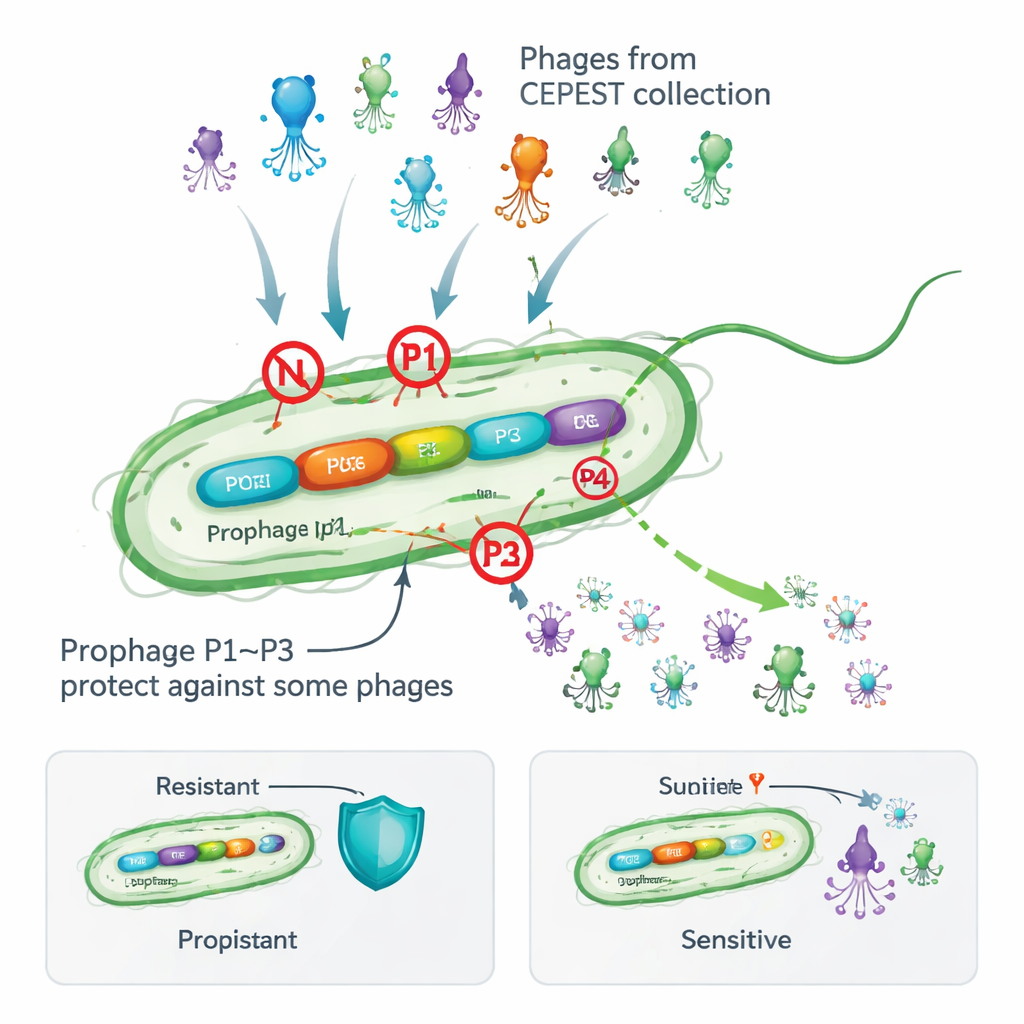
从敌人变为盟友的病毒
许多细菌携带温和噬菌体以称为前噬菌体的休眠形式嵌入染色体。乍看之下这似乎很危险:这些病毒寄生者可能苏醒并损害宿主细胞,还会增加基因组负担。然而对数千个细菌基因组的调查显示大多数物种保留此类前噬菌体,表明它们提供了某些优势。此前对土壤细菌Pseudomonas putida的研究表明,移除其四个隐匿(非产物性)前噬菌体会使细胞对名为 CEPEST 的实验性噬菌体库更易受攻击。这提示前噬菌体携带抗噬菌体武器,但具体的基因和机制尚不清楚。
三种常驻病毒提供针对性保护
作者通过逐一删除各前噬菌体并测试26种不同CEPEST噬菌体在细菌单层上的斑块形成能力,解析了每个前噬菌体的贡献。他们发现名为P1、P2和P3的前噬菌体各自提供保护,但仅针对特定的噬菌体群体,而P4则似乎中性。单独的P1可使某些噬菌体的感染率降低大约一千倍,P2提供较温和的保护,P3在对抗某些巨型“jumbo”噬菌体时极为有效。在大多数情况下,单个前噬菌体就能解释观察到的抗性模式,但对于少数噬菌体,多个前噬菌体似乎会协同作用。这些结果表明,即使是“沉默”的前噬菌体也能作为针对特定病毒威胁定制的盾牌。
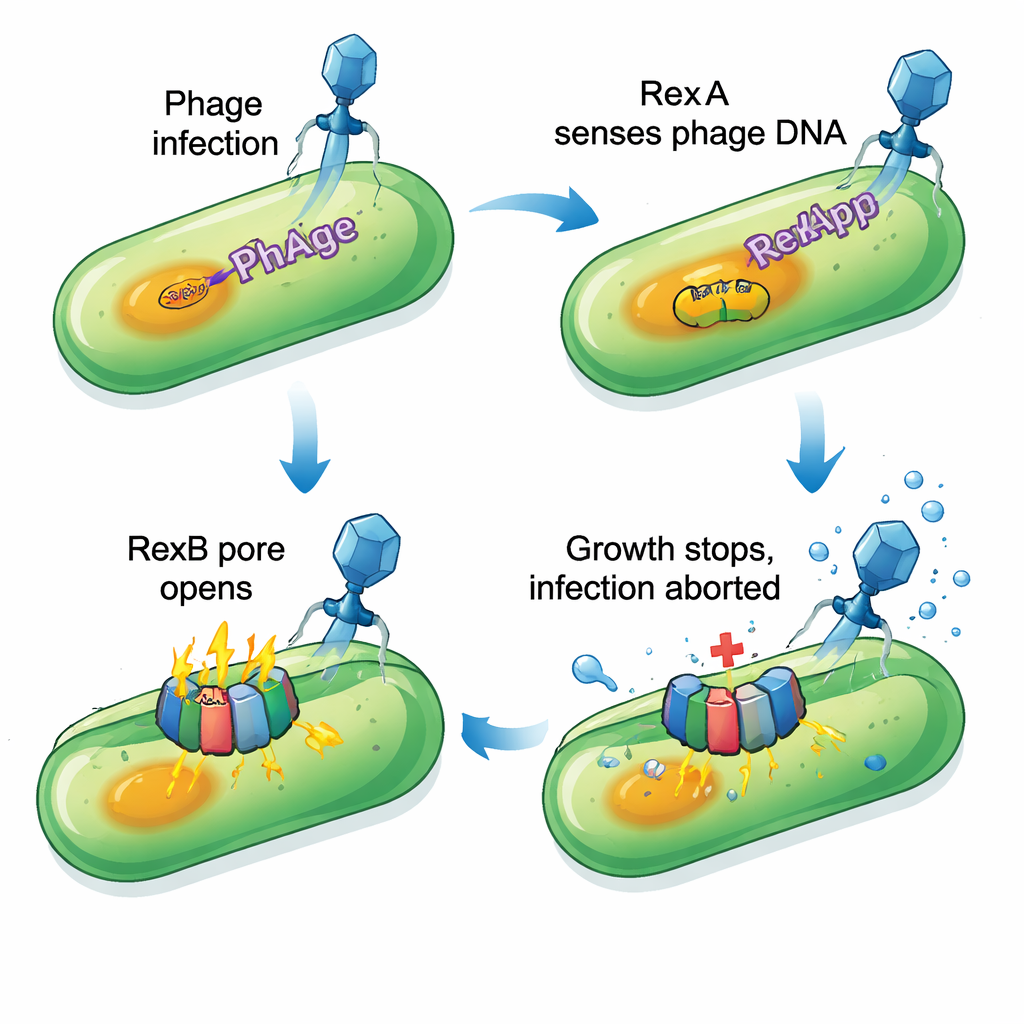
追踪一个由两部分组成的分子警报装置
研究小组聚焦于P1所提供的强大且相对广谱的保护,系统性地删除P1基因区块,直到防御消失。缩小范围后,他们发现仅失去相邻的两个基因PP_5643和PP_5644就能使细胞敏感性恢复到整个P1前噬菌体被删除的程度。生物信息学分析显示PP_5643类似于经典λ噬菌体研究中的DNA结合蛋白RexA,而PP_5644则像一个具若干跨膜螺旋、可能形成孔道的膜蛋白,类似RexB。二者合在一起符合一种众所周知的“自毁性感染”系统:一旦检测到特定噬菌体,受感染的细胞会有意停止自身生长,使病毒无法复制并扩散到邻近细胞。
该防御如何破坏受感染细胞
实验确认P1版本的RexA(称为RexApp)能以非序列特异性的方式结合DNA,这使其适合感知病毒复制时产生的不寻常DNA结构。其伴随蛋白RexBpp则嵌入细胞膜中。当人为过量表达RexApp时,仍携带rexBpp基因的细胞表现出严重生长停滞和膜损伤迹象:通常不能穿透完整膜的染料突然进入,且少量细胞质酶从细胞内泄漏。如果缺失或突变了rexBpp,过表达RexApp便不再对细胞造成伤害。这表明RexApp充当触发器,而RexBpp是损害细胞包膜的效应器。有趣的是,大多数受影响细胞并没有彻底破裂;相反它们进入深度放缓、几乎静止的状态,这种状态似乎使噬菌体无法完成增殖周期。
为何牺牲少数细胞能拯救群体
呈现出的图景是一种利他性的防御:当易感的噬菌体感染P. putida时,RexApp很可能检测到病毒的DNA–蛋白复合体并激活RexBpp,后者损害细胞膜并迅速停止生长。受感染的细胞为此付出代价,但噬菌体的生命周期被终止,较大的细菌群体因此获得保护。此类RexAB型系统目前仅在少数不同的噬菌体中被发现,但它们共享相同的核心逻辑——一个细胞内传感器连接到膜效应器,能够迅速将一个产病毒的细胞变成病毒的死胡同。对细菌而言,保留携带此类防御模块的隐匿前噬菌体可以抵消携带病毒DNA的成本,帮助它们在噬菌体无处不在的环境中生存。
引用: Rosendahl, S., Kängsep, A., Ainelo, A. et al. Prophage-encoded RexAB-type phage defense system in Pseudomonas putida. Sci Rep 16, 5898 (2026). https://doi.org/10.1038/s41598-026-36734-5
关键词: 细菌噬菌体防御, 前噬菌体, Pseudomonas putida, 自毁性感染(abortive infection), RexAB 系统