Clear Sky Science · zh
开发与验证一种用于临床前靶向放射性核素治疗的PSMA阳性三阴性乳腺癌小鼠模型
这项研究为何重要
三阴性乳腺癌是乳腺癌中最难治疗的类型之一。它易于快速扩散、可供患者选择的靶向治疗有限,且在标准疗法后常复发。与此同时,一类能够识别并结合特定分子PSMA的“智能”放射性药物已经彻底改变了晚期前列腺癌的治疗。这项研究提出了一个简单但有力的问题:我们能否建立一个真实可信的三阴性乳腺癌实验模型,该模型携带相同的PSMA靶点,从而公平地评估这些“智能”放射性药物是否也可能惠及患有这种侵袭性乳腺癌的患者?
从前列腺靶点到乳腺癌挑战
PSMA,全称前列腺特异性膜抗原,是一种位于某些细胞表面的分子结构。在很多前列腺癌中它表达丰富,可被放射性药物识别,这些药物既能在影像上显现肿瘤,又能将放射线直接递送到肿瘤部位。研究者最近发现,PSMA也在若干其他癌症的血管和细胞中不同程度地出现,包括三阴性乳腺癌。然而在这些非前列腺肿瘤中,PSMA通常表达零散且较弱,使得难以判断基于PSMA的治疗能否奏效。在将新疗法用于患者之前,科学家需要能忠实复制乳腺肿瘤中PSMA分布模式的动物模型——但实现这一点出乎意料地困难。
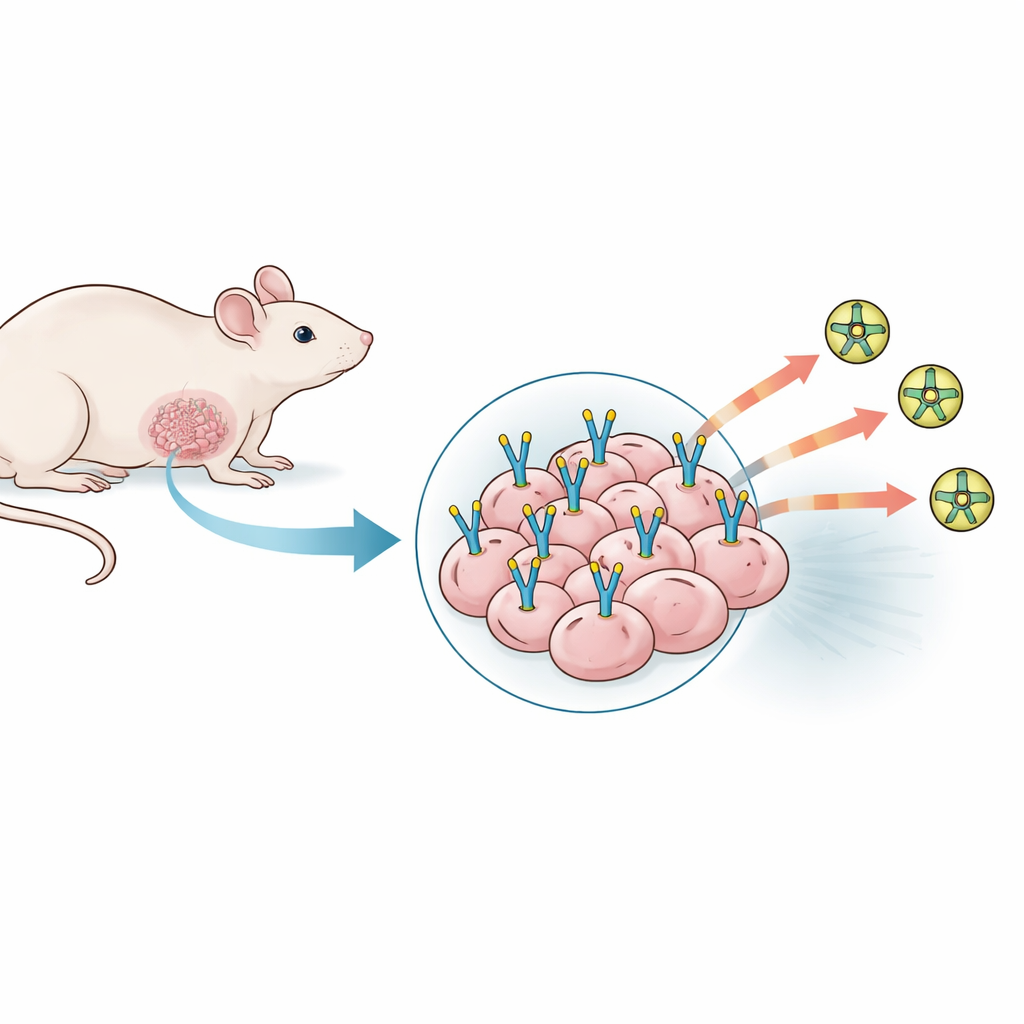
测试了许多不配合的肿瘤模型
研究团队首先考察了多种现成的三阴性乳腺癌小鼠模型,使用了小鼠和人来源的癌细胞系,并在不同部位和不同条件下植入。他们调整注入的癌细胞数量、添加促进血管生成的支撑凝胶,甚至混入人源血管细胞以期提升PSMA水平。对每一种模型,研究者都测量了肿瘤着床和生长的可靠性、在显微镜下检查肿瘤切片,并用一种寻找PSMA的PET示踪剂观察肿瘤在全身扫描中是否显影。尽管肿瘤生长良好且血管网络丰富,但这23种模型中没有一种在组织染色或PET成像上显示出有意义的PSMA表达。肿瘤看起来活跃且血供充足,但研究者需要的特定PSMA“停靠位”基本上缺失。
构建呈现正确靶点的肿瘤
面对这一障碍,研究者采取了更直接的路径。他们对一种广泛使用的人类三阴性乳腺癌细胞系MDA-MB-231进行了基因修饰,使其在细胞表面表达PSMA。经改造的细胞随后被植入免疫缺陷小鼠的乳腺脂肪垫,该部位更能模拟自然的乳腺环境。研究人员建立了两种模型:一种是所有肿瘤细胞均表达PSMA,另一种为“混合”肿瘤,含等比例的PSMA阳性和普通癌细胞,以模拟患者中可见的斑块式表达模式。两种模型的肿瘤着床和生长速度与未改造细胞制造的肿瘤相似,表明加入PSMA并未使癌细胞本身表现异常。
在扫描和显微镜下观察新靶点
当向这些小鼠注射PSMA示踪的PET示踪剂时,工程化肿瘤在扫描中明亮显影,肿瘤摄取量约为肝脏或肌肉的十倍。这一强烈且选择性的信号证实PSMA在癌细胞表面大量存在,并且可被循环中的药物触及。对肿瘤组织的显微分析也一致:PSMA染色强但不均匀,表现出强表达与弱表达的斑块,类似于人类三阴性乳腺癌中观察到的异质性模式。重要的是,新增的PSMA局限于肿瘤细胞,而非周围血管,使该模型专注于针对细胞的治疗。较大肿瘤内部的坏死区不摄取示踪剂,这与临床观察一致。
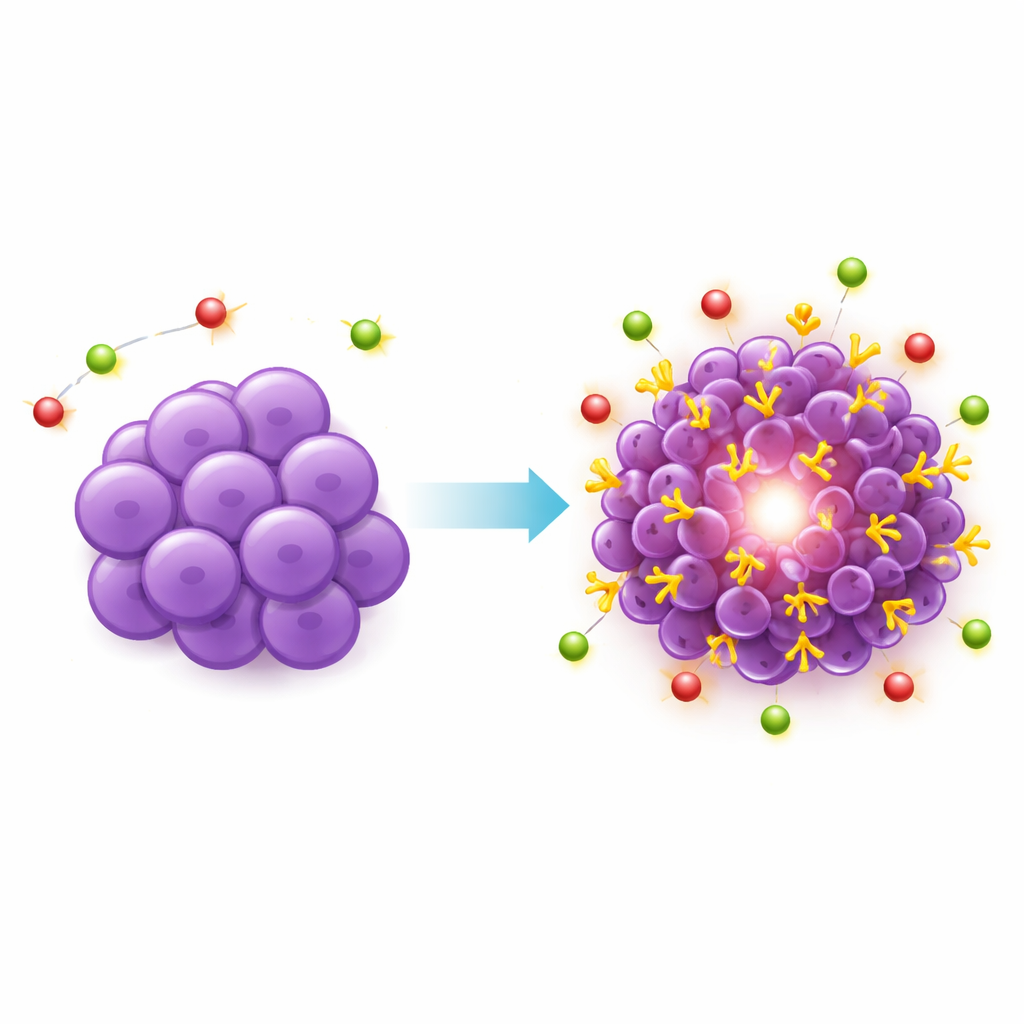
这对未来治疗意味着什么
通过系统地证明标准乳腺癌小鼠模型无法可靠表达PSMA,并构建出能够表达PSMA的新模型,这项工作为下一代靶向放射治疗提供了重要的实验评估平台。该PSMA阳性三阴性乳腺癌模型稳定、生长可预测,并呈现出高低PSMA区域的现实性混合,使其非常适合在将药物用于患者之前评估PSMA靶向药物的作用方式。尽管该模型无法涵盖人类疾病的所有方面——例如完整功能的免疫系统的影响——它仍然是一个有力的工具,可用于探索将PSMA基治疗在前列腺癌中的成功是否有望推广到患有这种高度侵袭性乳腺癌的人群。
引用: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
关键词: 三阴性乳腺癌, PSMA, 靶向放射性核素治疗, 临床前小鼠模型, PET 成像