Clear Sky Science · zh
敲低WNK1激酶长异构体可减轻小鼠抗肾小球基底膜性快速进展性肾小球肾炎
这对肾脏健康为何重要
快速进展的肾脏疾病可以在数周内摧毁器官的微小滤过单元,常导致透析或移植。该研究探讨了降低一种名为L‑WNK1的蛋白是否能在小鼠中减缓这种破坏。由于针对该蛋白的药物已在用于血压问题的开发中,研究结果提示可能出现一种保护受攻击肾脏的新途径。
肾小球内的“交通指挥官”
每只肾脏包含数十万个微小的滤过器或肾小球,用以清洁血液。在这些滤过器内,两类关键细胞协同工作:像互扣手指一样包绕血管的足细胞,以及衬在外壳的壁上皮细胞(PECs)。在一种称为快速进展性肾小球肾炎(RPGN)的危险病况中,足细胞受损,PECs 过度活跃,堆积形成阻塞滤过的新月体。L‑WNK1 是一种信号开关,最为人所知的是参与体内盐分与血压平衡,但实际上在这些肾小球细胞中也高表达。作者们提出疑问:L‑WNK1 过量是否加重 RPGN,降低其水平是否能减轻疾病。
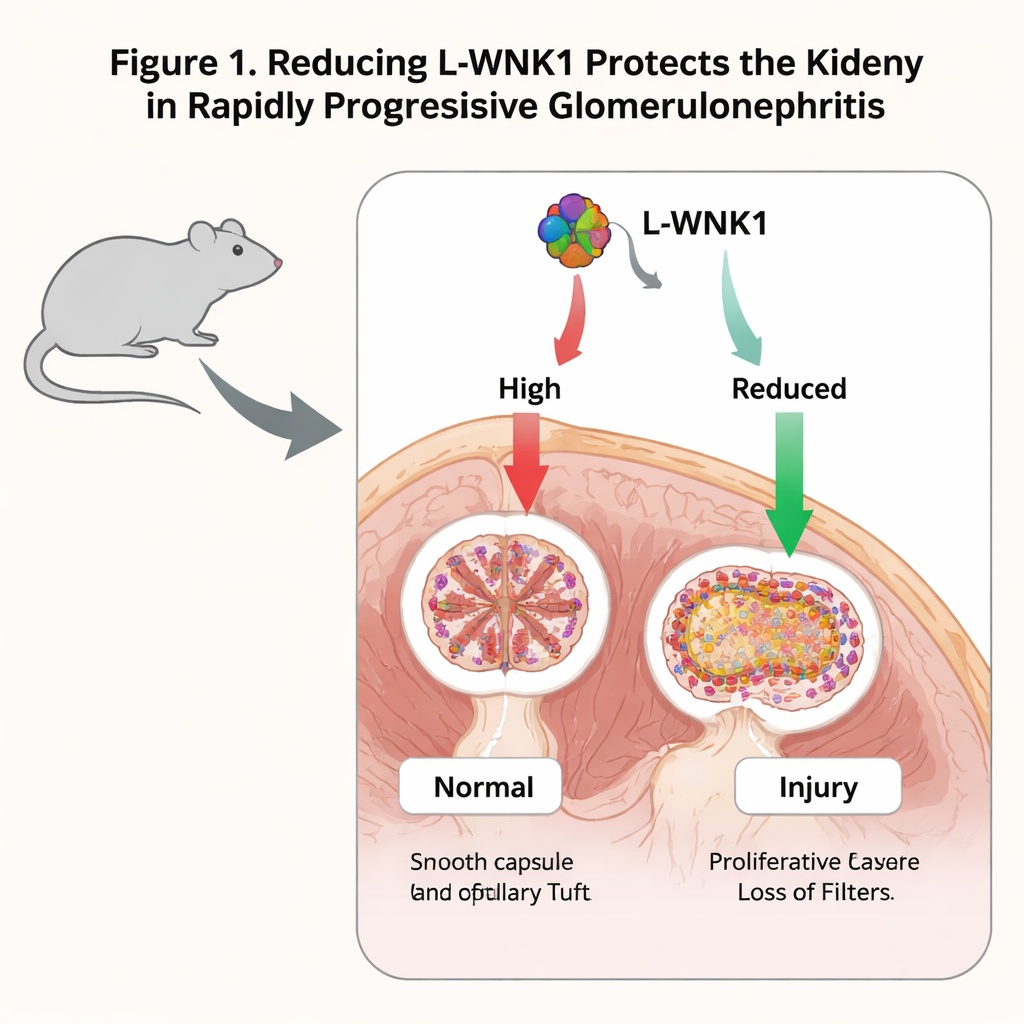
降低L‑WNK1缓解小鼠肾损伤
研究者首先使用一种经典的模型:由针对肾小球基底膜的抗体诱发的 RPGN 小鼠模型。他们发现受伤后肾小球中 L‑WNK1 水平升高,这一现象不仅出现在小鼠,也见于相关疾病患者的肾脏活检。为检验因果关系,他们研究了只带有一个正常 L‑WNK1 基因拷贝的杂合小鼠。这些动物在抗体诱发损伤后出现肾功能衰竭,但血液废物水平较低,肾组织中出现的新月体更少、纤维化程度也低于正常小鼠。炎症与纤维化标志物(如信号分子 MCP‑1、TGF‑β1 及胶原基因)亦有所减少。总体显示,部分丧失 L‑WNK1 使疾病变得更温和,而非更严重。
聚焦足细胞及其邻近细胞
鉴于足细胞对肾小球健康至关重要且高表达 L‑WNK1,团队随后使用遗传手段选择性在足细胞中敲除 WNK1。在正常条件下,这些小鼠肾脏健康,表明足细胞在日常发育和功能中并不依赖 L‑WNK1。当诱发 RPGN 时,足细胞特异性敲除小鼠相比对照组同样表现更好:血液检查有改善,且往往新月体更少、表达活化标志 CD44 的 PECs 数量也较少。然而,这种保护不如全身性降低 L‑WNK1 那样显著,部分炎症标志物水平并未下降。这提示 L‑WNK1 的作用不仅限于足细胞,还包括参与疾病的其他肾小球或免疫细胞。
减缓有害细胞迁移
为探究 L‑WNK1 可能如何驱动新月体形成,研究者转向细胞培养。使用一种抑制 WNK 激酶的小分子药物,他们处理培养皿中生长的人足细胞,观察其向人工“伤口”间隙爬行的速度。阻断 L‑WNK1 活性明显减慢了这些细胞的移动。在培养的 PECs 中也观察到类似效果:加入生长因子时,PECs 通常会扩展填补空隙,但在存在 WNK 抑制剂时这一反应被抑制。有趣的是,在他们的体系中该药物并未明显扰乱足细胞的内部支架,尽管早先在小鼠细胞中的工作提示可能存在主要的结构问题。这支持这样的观点:至少在活体动物中,L‑WNK1 在此处的主要作用可能是控制肾小球细胞和免疫细胞在损伤期间的迁移与反应,而非维持基础的滤过结构。
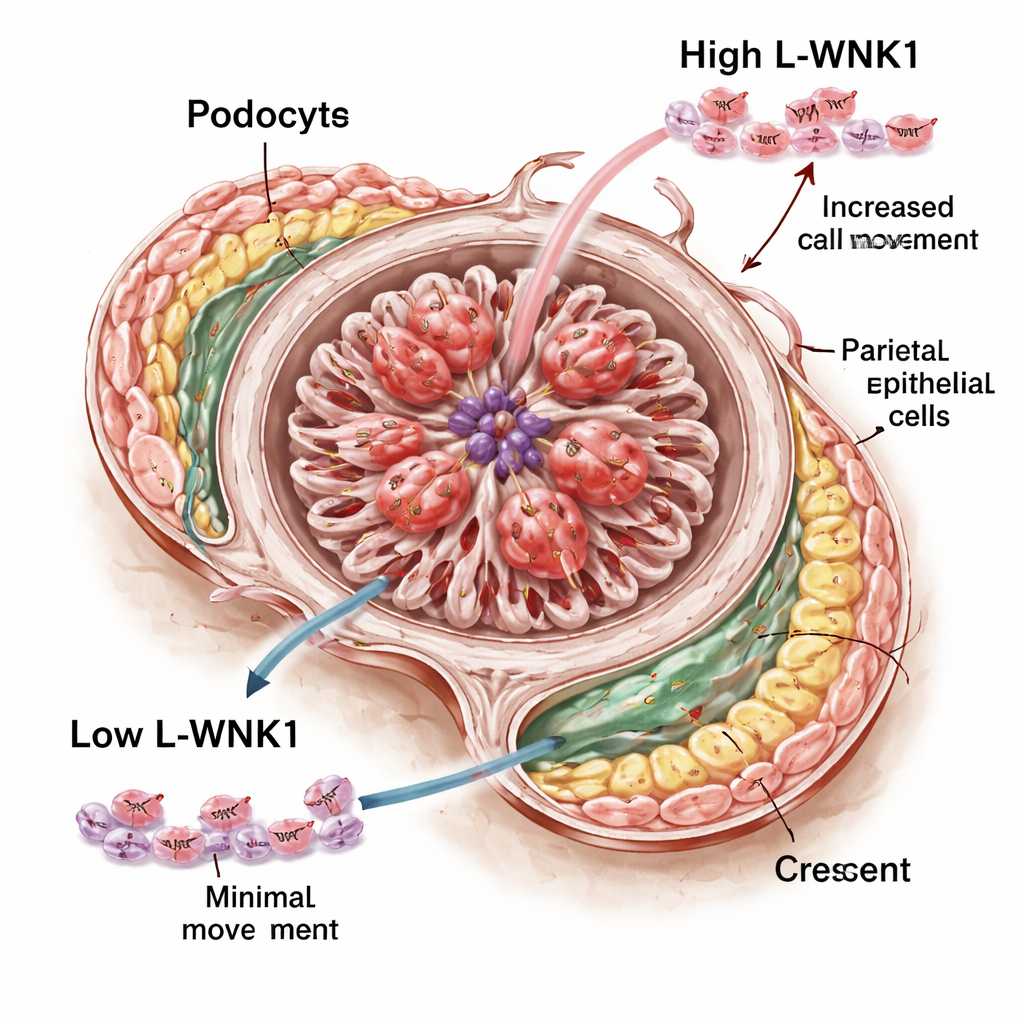
对未来治疗的意义
总体来看,该研究将 L‑WNK1 揭示为一种在暴力性肾脏炎症中加速病程的有害因子:当这种蛋白上调时,肾小球关键细胞的迁移与增殖会以堵塞和瘢痕化滤过器的方式进行;当其活性降低时,损伤则被缓和。由于 L‑WNK1 已作为降血压的药物靶点被研究,这些发现提出了一个可能性:精细调控的抑制剂将来或能帮助保护患有快速进展性肾脏疾病的患者。要把小鼠和细胞培养的结果转化为安全的疗法仍有许多工作要做,但 L‑WNK1 现在成为了对抗这一毁灭性疾病的一个有前景的新靶点。
引用: Mousseaux, C., Migeon, T., Frère, P. et al. Knock-down of the long isoform of the WNK1 kinase mitigates the anti-glomerular basement membrane glomerulonephritis in mice. Sci Rep 16, 7335 (2026). https://doi.org/10.1038/s41598-026-36715-8
关键词: 快速进展性肾小球肾炎, 肾脏炎症, 足细胞, 肾小球新月体, WNK1抑制