Clear Sky Science · zh
在失锚凋亡中识别并验证 SPP1 作为肠化生和胃癌的预后生物标志物
这对胃部健康为何重要
胃癌是全球致死率最高的癌症之一,主要原因在于其通常在晚期才被发现。在出现明显肿瘤之前,胃黏膜常经历一个警示阶段,称为肠化生——此时正常的胃细胞开始呈现类似肠道细胞的特征。本研究跟踪了从健康组织、经肠化生到胃癌的整个演变过程,旨在寻找组织中可测量的单一信号,用以早期标识高危人群,帮助医生预测哪些患者预后较差、可能需要更密切随访或新的治疗策略。
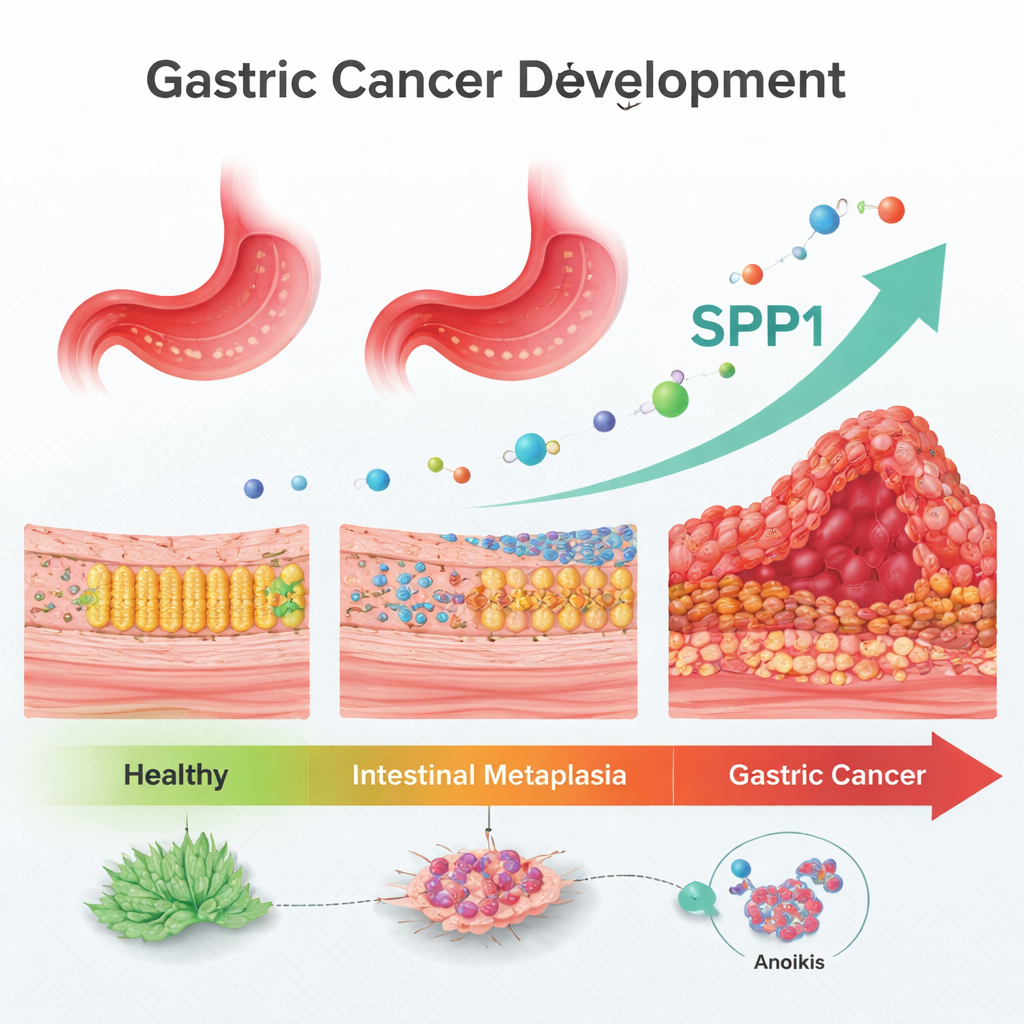
通往癌症道路上的踏脚石
临床上早已知道肠化生是癌前病变,但缺乏可靠的标志物来判断哪些患者最终会进展为癌症。研究者聚焦于一种称为失锚凋亡(anoikis)的细胞死亡方式,正常情况下它会消灭从组织原位脱落的细胞。癌细胞必须学会抵抗失锚凋亡,才能迁移、在血液中存活并播散到远处。研究团队通过挖掘来自数百名患者的大型公共基因数据库,寻找与失锚凋亡相关且在“Correa 级联”过程中(健康胃黏膜→肠化生→胃癌)呈持续变化的基因。
锁定一个关键的警示分子
借助先进的统计工具和网络分析,科学家多次筛选出一个突出基因:SPP1,其编码的蛋白也被称为骨桥蛋白(osteopontin)。在三套独立数据集中,SPP1 的表达在健康胃组织中始终较低,在肠化生中升高,在胃癌中最高。这种阶梯式的模式在校正了不同研究间的技术差异后仍然成立。对数千个基因的进一步计算机分析显示,高表达的 SPP1 常与免疫相关通路以及对环境和化学应激的反应变化同时出现,提示该分子可能在细胞存活、慢性刺激和免疫系统之间串联起作用,参与癌变过程。
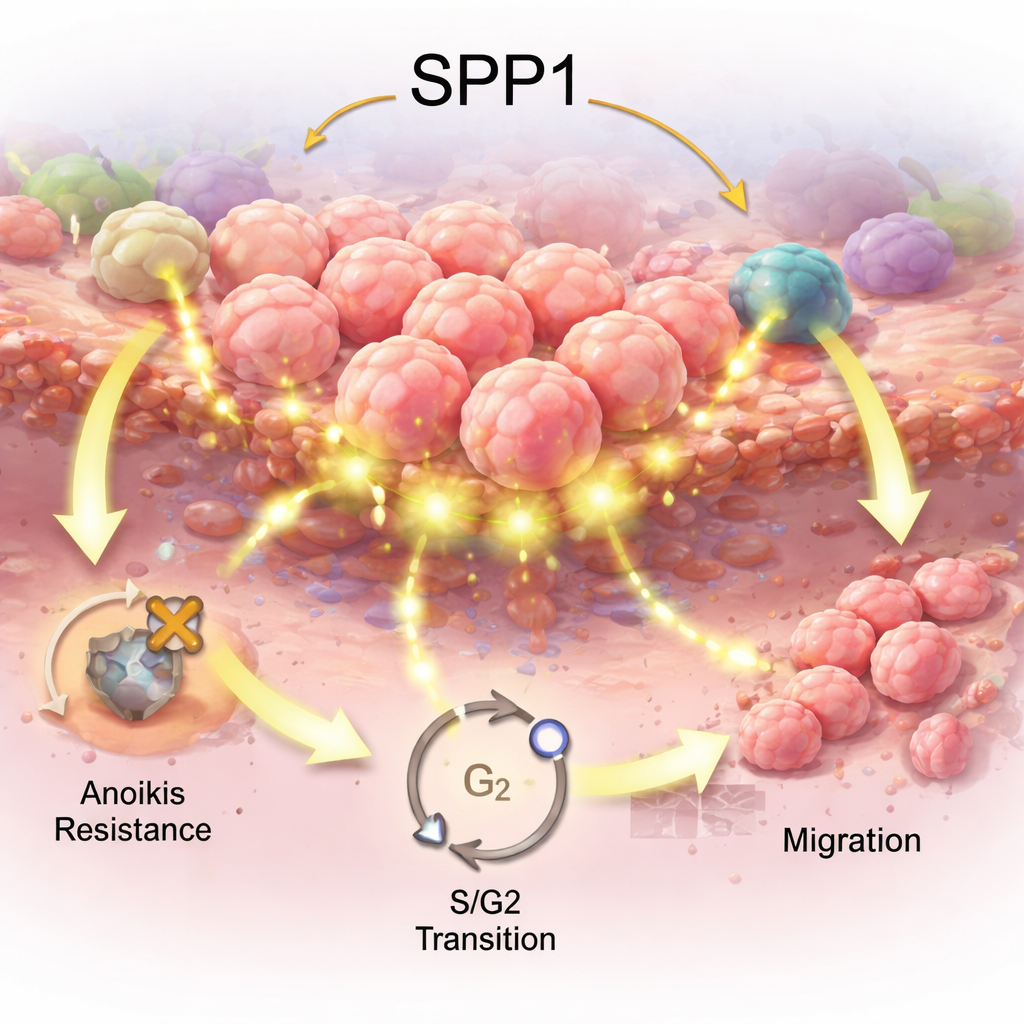
来自机体防御细胞的线索
接着,研究组考察了 SPP1 与浸润肿瘤的免疫细胞之间的关系。在整体肿瘤样本中,SPP1 表达升高与免疫细胞构成的变化相关,包括某些可抗肿瘤或可被肿瘤抑制的巨噬细胞和 T 细胞的增多。单细胞 RNA 测序(一种逐细胞读取基因活性的技术)显示,SPP1 在肿瘤相关巨噬细胞及肿瘤微环境中的其他细胞中被强烈激活。涉及 SPP1 与其配体受体 CD44 的信号似乎将这些巨噬细胞与辅助型 T 细胞联系起来,暗示该通路可能帮助形成一种有利于肿瘤生存而非清除的免疫“邻里”环境。尽管这些联系是相关性的,但它们指向 SPP1 可能在胃癌逃避免疫攻击中发挥作用。
从大数据到真实组织与细胞
为验证计算发现是否反映真实情况,研究者在 32 例人类胃组织样本中检测了 SPP1 。基因与蛋白水平的检测结果显示相同趋势:正常组织表达最低,肠化生中较高,胃癌中最高。肿瘤中 SPP1 表达较高的患者总体生存显著更差,统计模型表明 SPP1 有助于预测一年、三年和五年的结局。在细胞培养实验中,下调胃癌细胞系中的 SPP1 会减慢细胞增殖、降低迁移能力、增加程序性细胞死亡并导致细胞周期在关键阶段停滞。这些实验证据支持 SPP1 有助于癌细胞抵抗死亡并持续分裂的观点。
这对患者可能意味着什么
对非专业读者来说,可得出的结论是:在从“高风险但尚未癌变”的胃黏膜走向明确癌症的过程中,SPP1 表现得像一个不断响起的警报。该分子水平升高标志着更可能进展的组织和预后更差的患者。尽管仍需进一步研究——尤其是更大规模的患者队列和动物实验——未来在肠化生活检中监测 SPP1 有望帮助医生决定谁需要更紧密的随访或更早的干预。在已确诊的胃癌中,阻断 SPP1 或其关键配体的药物,可能通过使癌细胞更易于死亡并重塑周围免疫细胞以更有效地对抗疾病,从而削弱肿瘤的防御。
引用: Wu, K., Ye, Y., Pei, B. et al. Identification and verification of SPP1 in anoikis as a prognostic biomarker for intestinal metaplasia and gastric cancer. Sci Rep 16, 5842 (2026). https://doi.org/10.1038/s41598-026-36714-9
关键词: 胃癌, 肠化生, 生物标志物, 骨桥蛋白 SPP1, 肿瘤微环境