Clear Sky Science · zh
在念珠菌感染模拟唾液中胃蛋白酶驱动的正畸钛合金腐蚀:电化学与统计洞见
这对戴牙套的人为何重要
数以百万计的人依赖金属托槽、弓丝和小型种植体来矫正牙列。这些器件通常由被认为安全且耐用的钛合金制成。但在口腔内,它们置身于不断变化的唾液、食物酸和微生物的混合环境中。本研究提出了一个具有实际影响的问题:在反流病中,胃酸和消化酶进入口腔,而且一种常见的口腔真菌白色念珠菌加入其中时,正畸用钛合金会发生什么变化?
用于矫正牙列的金属
研究者聚焦于一种常用的正畸金属Ti‑6Al‑4V,这是一种以强度和生物相容性著称的钛合金。正常情况下,钛会形成一层极薄但坚韧的氧化膜,自我保护以减缓腐蚀并限制金属离子的释放。然而口腔远非稳定。唾液含有盐类、酸、酶和多样的微生物群,其酸度在人与人之间可发生剧烈变化。在患有胃食管反流病(GERD)的人群中,酸性胃内容物和胃蛋白酶常会到达口腔,降低唾液pH,并可能改变微生物与金属的行为。
在实验室模拟病态口腔
为探究这些情形,团队制备了人工唾液并对其进行改造以模拟受GERD影响的口腔。他们加入了胃蛋白酶,将酸度调整到约pH 4.9(类似于GERD唾液),并引入了白色念珠菌——这种真菌是许多口腔酵母感染的主要病原,尤其在佩戴正畸装置的人群中常见。将小型Ti‑6Al‑4V圆柱体在人体温度下浸泡于四种溶液中长达10天:单纯唾液、含胃蛋白酶的唾液、含念珠菌的唾液、以及同时含胃蛋白酶和念珠菌的唾液。研究者使用灵敏的电化学方法追踪金属—溶液界面的电流通过性,这反映了合金随时间抗腐蚀的能力。
消化酶何时成为金属的保护者
出人意料的是,仅有胃蛋白酶的情况下,它表现出强烈的保护作用。测量显示,在仅含胃蛋白酶的唾液中,钛合金的腐蚀速率显著下降,经过240小时保护率接近87%。数据与显微图像表明,胃蛋白酶分子会吸附到金属表面,形成一层蛋白膜,类似临时的透明保护层,减缓了侵蚀性离子和水的到达。这层蛋白膜使金属的电化学行为更为稳定并将腐蚀电位朝更安全的方向移动,证实在这些模拟条件下,消化酶更像是屏障而非攻击者。
真菌何时建立又失去屏障
白色念珠菌单独存在时也在一定程度上提供了保护,至少在初期如此。真菌附着于钛表面并分泌出一种由糖类和蛋白质组成的粘性混合物,形成生物膜。这层覆盖物物理上覆盖了大部分表面,并最初减缓了腐蚀,在某些时间点保护率超过80%。但随着暴露时间延长,这种益处逐渐减弱。真菌层变得斑驳且不均匀,抗腐蚀性逐步下降至约72%。研究表明,虽然微生物膜有时可作为屏障,其长期稳定性并不确定,最终可能促成表面损伤和金属离子释放。
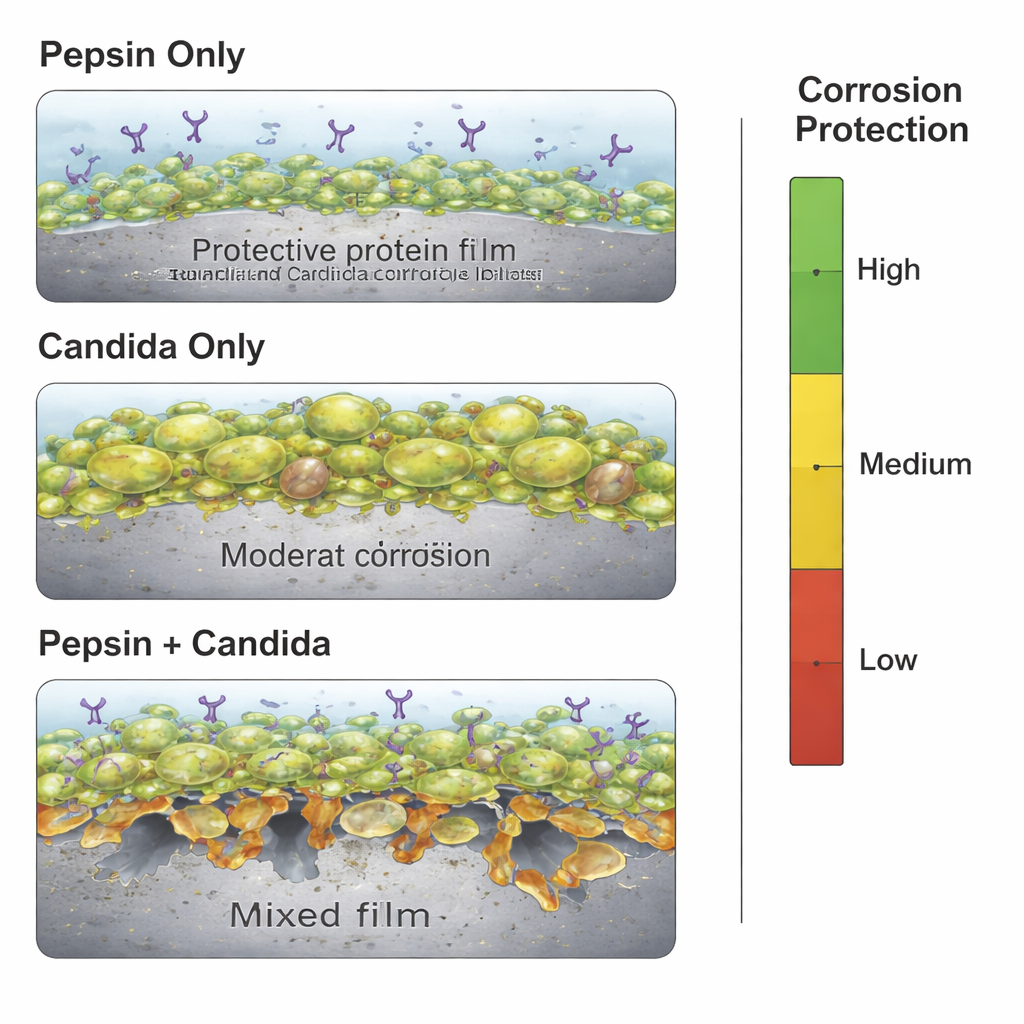
盟友何时变成敌人
最引人注目的结果出现在胃蛋白酶与念珠菌同时存在时。两者并未叠加保护作用,反而削弱了各自的保护效能。真菌仍然形成生物膜,胃蛋白酶仍然吸附到表面,但胃蛋白酶的蛋白切割活性开始分解真菌基质,产生裂隙并暴露裸露金属。同时,来自微生物的酸性代谢产物和被消化膜的碎片加剧了对合金的化学攻击。电化学测试显示,总体保护率下降到约56%,显著低于仅含胃蛋白酶或仅含念珠菌的情况。统计建模也证实,正是这些组分间的相互作用——而非单纯的暴露时间——主导了腐蚀行为的变化。
对患者和牙医的意义
对于既戴牙套或使用钛小型种植体又患有GERD或口腔念珠菌感染的人来说,这项工作传达了明确的信息。单一因素如消化酶或微生物膜有时可以帮助屏蔽牙科金属,但在受GERD影响的口腔中它们相互作用时,可能反而加速损伤。研究提示,控制反流和管理口腔念珠菌不仅关乎舒适,也可能对保持正畸钛合金的稳定性、降低早期种植失败或金属离子释放风险具有重要意义。简言之,健康且受控的口腔环境也更有利于那些用于矫正牙齿的金属。
引用: El-Kamel, R.S., Fekry, A.M. Pepsin-driven corrosion of orthodontic titanium alloys in candidiasis-simulated saliva: electrochemical and statistical insights. Sci Rep 16, 5937 (2026). https://doi.org/10.1038/s41598-026-36707-8
关键词: 正畸钛合金, 胃食管反流病与唾液, 白色念珠菌, 胃蛋白酶腐蚀, 牙科种植体