Clear Sky Science · zh
胆管癌来源的外泌体削弱了NK细胞的抗肿瘤功能
一种隐匿的癌症如何智胜免疫系统
胆管癌是发生在肝内胆管的癌症,早期难以发现且治疗困难。本研究探讨了这些肿瘤用以规避机体天然防御的一种微妙策略:它们释放称为外泌体的小包裹,悄然削弱自然杀伤(NK)细胞这一专门负责识别并杀死癌细胞的第一线免疫队伍。理解这种隐蔽策略可能为恢复免疫系统抗癌能力的治疗途径打开新方向。
机体的先遣癌症杀手
NK细胞属于先天免疫系统,是机体的快速反应部队。与许多需要时间识别特定威胁的免疫细胞不同,NK细胞能迅速攻击异常细胞,包括被病毒感染的细胞和癌细胞。它们通过附着靶细胞并释放毒性分子(如颗粒酶B)以及信号蛋白(如干扰素-γ,IFN-γ)来直接杀伤肿瘤细胞并召集其他免疫细胞参与。在多种血液肿瘤和某些实体瘤中,增强NK细胞活性已显示出作为治疗策略的潜力。但在像胆管癌这样的实体瘤中,NK细胞常在最需要它们的肿瘤部位显得稀少且反应迟缓。
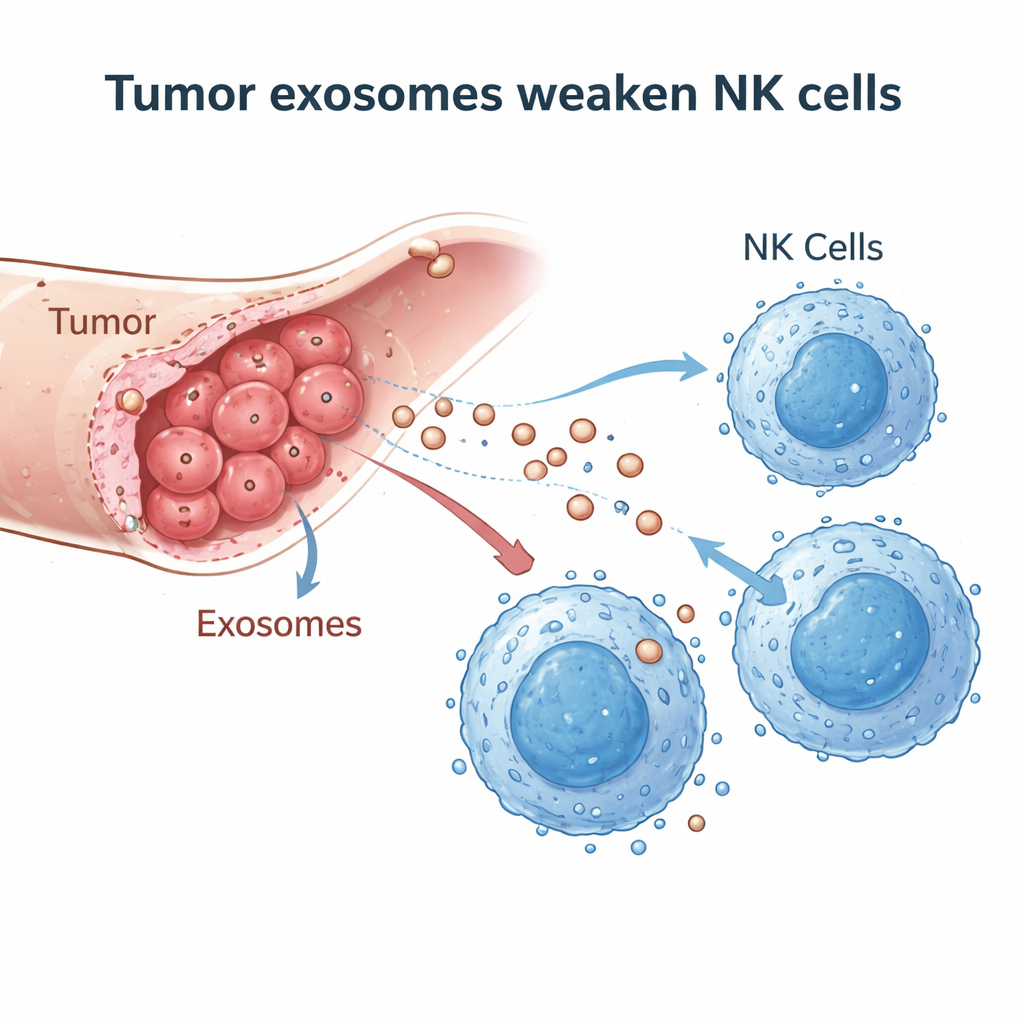
影响巨大的微小囊泡
研究者怀疑胆管癌细胞可能通过外泌体破坏NK细胞——外泌体是细胞释放的纳米级膜囊,内含蛋白质和遗传物质,用于细胞间通讯。他们从一株人胆管癌细胞系和胆管癌患者的血液中分离出外泌体,并用电子显微镜、粒子追踪和常规外泌体标志物确认了其形态和大小。在来自20名患者的肿瘤组织样本中,他们比较了癌变区域与邻近的非癌肝组织,发现浸润到肿瘤中的NK细胞显著减少,提示肿瘤微环境中存在使NK细胞远离或失能的因素。
关闭生存与杀伤信号
为观察这些肿瘤外泌体对NK细胞的影响,研究团队将一株NK细胞系(NK-92)暴露于来自肿瘤细胞和患者血液的外泌体。暴露后,NK细胞显示出更高水平的程序性细胞死亡,尤其是接受肿瘤细胞系外泌体处理时。在分子层面,NK细胞降低了关键“存活”蛋白(BCL-2和BCL-XL)的表达,使细胞更趋向于死亡。有趣的是,它们的总体增殖并未改变,这意味着外泌体主要使NK细胞更易死亡,而不是抑制其分裂。接受外泌体处理的NK细胞还减少了IFN-γ和颗粒酶B的释放,既削弱了直接杀伤靶细胞的能力,也削弱了协调更广泛免疫反应的能力。体外测定NK细胞对标准靶细胞的杀伤能力显示,接触胆管癌外泌体后其杀伤效力下降。
破坏免疫细胞间的协同
NK细胞需要相互粘附并与肿瘤细胞接触才能高效工作,这依赖于表面“粘附分子”,类似分子级的魔术贴。经肿瘤来源外泌体处理后,NK细胞失去了正常的簇状生长模式,呈现更为分散的形态。研究者发现若干重要粘附分子(CD11a、CD18和CD54)的基因与蛋白水平下降,而另一种粘附标志物CD2未见变化。这种粘附能力的丧失很可能让NK细胞更难到达肿瘤、与癌细胞形成稳定接触并实施致命打击。关键是,从胆管癌患者血液中分离的NK细胞也表现出相同特征:较弱的杀伤活性以及与健康志愿者相比降低的相同粘附分子水平。
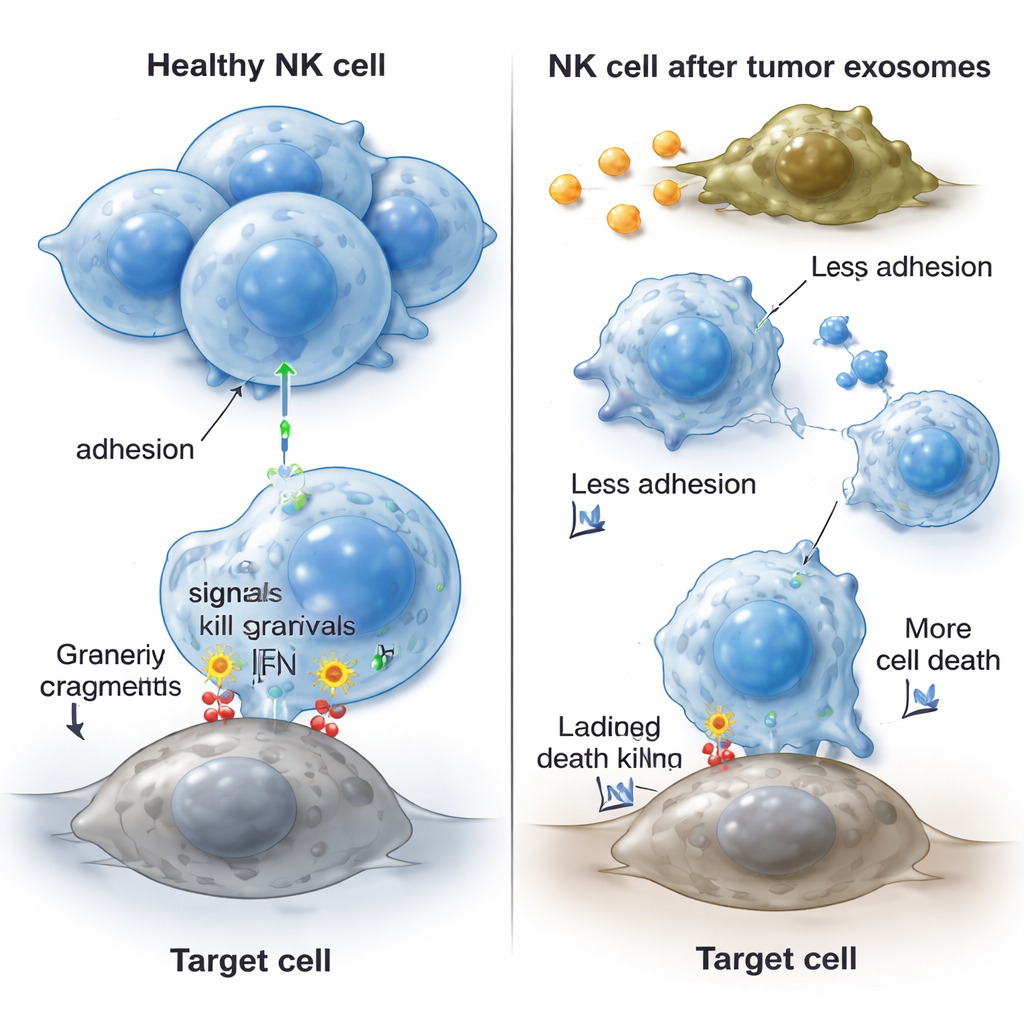
对患者和未来治疗的意义
综合来看,这些发现表明胆管癌利用外泌体作为分子级的破坏手段以逃避免疫攻击。这些微小囊泡促使NK细胞走向死亡,减少其关键杀伤因子的产生,并剥夺其使细胞聚集并接触肿瘤的粘附蛋白。其结果是在肿瘤内外功能性NK细胞减少,免疫反应被削弱,从而使癌症更易生长。虽然这项工作主要在受控的实验室条件下并使用有限的患者样本完成,但它指出了新的策略:阻断肿瘤外泌体、恢复NK细胞的存活信号或增强粘附分子,或可帮助重新唤醒免疫系统对抗这种致命的胆管癌的自然防御能力。
引用: Wang, X., Zhang, F., Cao, Z. et al. Cholangiocarcinoma derived exosomes attenuate the anti-tumor functions of NK cells. Sci Rep 16, 5810 (2026). https://doi.org/10.1038/s41598-026-36706-9
关键词: 胆管癌, 自然杀伤细胞, 外泌体, 肿瘤免疫逃逸, 肿瘤微环境