Clear Sky Science · zh
表达A组链球菌类胶原蛋白样蛋白1的乳酸乳球菌作为胰腺导管腺癌新型免疫治疗的应用
把“友好”细菌变成抗癌战士
胰腺癌是最致命的癌症之一,部分原因在于它藏身于强大的防御体系之后,压制机体免疫反应。本研究探讨了一种出乎意料的盟友:来自乳制品领域的常见“良性”细菌,经重新设计后可定向到胰腺肿瘤并帮助免疫系统更有效地攻击它们。研究人员借用一种来自致病链球菌的黏附表面蛋白,把无害微生物改造成在小鼠体内具有靶向抗癌作用的工具。
一种能智胜免疫系统的顽疾
胰腺导管腺癌的致死率极高,确诊后五年存活率仅约八分之一。其主要原因之一在于肿瘤微环境:一种致密、类似瘢痕的外壳,充斥着支持性细胞和分子,抑制免疫攻击并阻挡多种药物。在这些“同谋”中有中性粒细胞细胞外陷阱(NETs)——中性粒细胞向外释放的DNA和蛋白构成的网。在胰腺癌中,这些黏糊的网带来的是弊多于利:它们促进肿瘤生长、阻隔杀伤性T细胞,并与更差的预后相关。抑制NETs同时唤醒抗肿瘤免疫,已成为一个富有吸引力的策略。
借用黏附蛋白,但不带致病菌
早期研究表明,A组链球菌的一种表面蛋白Scl1既能附着在肿瘤相关的纤维上,又能抑制NET形成,从而在小鼠中延缓胰腺肿瘤生长。但A组链球菌同时也是引起咽炎和严重侵袭性感染的病原体,不适合作为活菌治疗。为保留有益蛋白而避免危害,研究团队将Scl1展示在被广泛用于食品且被认为安全的乳酸乳球菌表面。该新菌株被命名为Lactococcus::620,并在携带胰腺肿瘤的小鼠中进行了测试,既有简单的皮下肿瘤模型,也有更接近真实情况的胰腺内生长肿瘤模型。
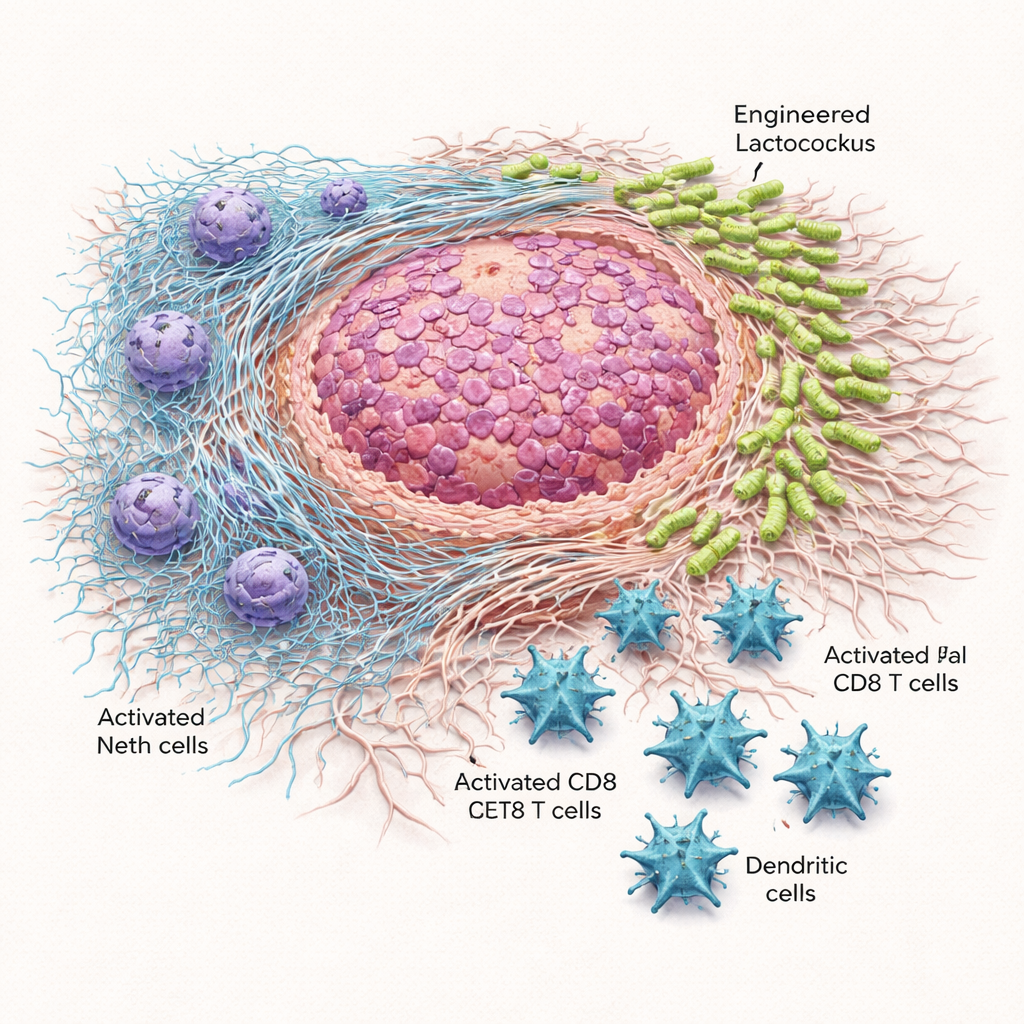
定向细菌削减肿瘤生长并延长生存
将单次剂量的工程菌直接注入皮下肿瘤或腹腔递送时,与给予普通乳酸乳球菌或盐水对照的小鼠相比,肿瘤生长更慢且重量更轻。在更具挑战性的胰腺模型中,需要每三天重复给药,但获益显著。Lactococcus::620使肿瘤缩小、重量下降并延长动物生存期,且未导致与治疗相关的死亡。对肿瘤组织的显微镜观察和培养显示,携带Scl1的细菌在肿瘤区域,尤其是在癌相关成纤维细胞铺设的纤维基质中稳定富集,而在很大程度上不累及脾脏。相比之下,未改造的乳酸乳球菌在体内分布更广,系统给药时有时会出现毒性。
解除有害网并让免疫细胞入场
工程菌还重塑了肿瘤周围的免疫格局。接受Lactococcus::620处理的小鼠肿瘤中含有更多的CD8“杀伤”T细胞和树突状细胞——这些是识别并清除癌细胞的关键执行者——且这些T细胞表现出更少的耗竭标志和更多与活性相关的分子。与此同时,NET活性指标下降。体外实验显示,暴露于Lactococcus::620的中性粒细胞释放的自由DNA减少,构建NET所需的过氧化物酶(myeloperoxidase)活性也较低。治疗小鼠的循环中与NET相关的DNA水平降低。关键的是,在不能形成NET的基因型小鼠中重复同样实验时,工程菌不再能减缓肿瘤生长。这种疗效丧失强烈表明,阻断NETs对于该疗法的作用至关重要。
这对未来癌症治疗的意义
综上所述,这些发现勾勒出一个新理念:利用一种安全的食品级细菌作为可编程的递送载体,将阻断NET并能靶向肿瘤的蛋白直接带入胰腺癌的敌对环境。在小鼠中,这一方法减轻了肿瘤负担、改善了生存,并为免疫细胞更有效地发挥作用创造了条件。尽管在将此策略用于人类之前仍需大量工作——包括在转移性疾病模型中的测试以及与现代免疫疗法的联合——该研究表明,精心设计的“良好”细菌有朝一日可能帮助我们在对抗这种高度难治的癌症时扭转局面。
引用: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
关键词: 胰腺癌, 益生菌疗法, 肿瘤微环境, 免疫调节, 中性粒细胞细胞外陷阱