Clear Sky Science · zh
血液中表面标志物:超级小体在结直肠癌诊断中胜过细胞外囊泡
为何微小血液颗粒可能改变癌症检测
结直肠癌是全球最常见的癌症之一,临床迫切需要更好的血检方法来及早发现疾病并监测治疗效果。本研究考察了一类新识别的超小型血液颗粒,称为“超级小体(supermeres)”,并表明它们可能携带比已知颗粒更清晰的癌症信号。作者还展示了一种快速传感器,能在不到半小时内用一小滴血直接检测这些超级小体,这可能为更快、更精确的癌症诊断铺平道路。
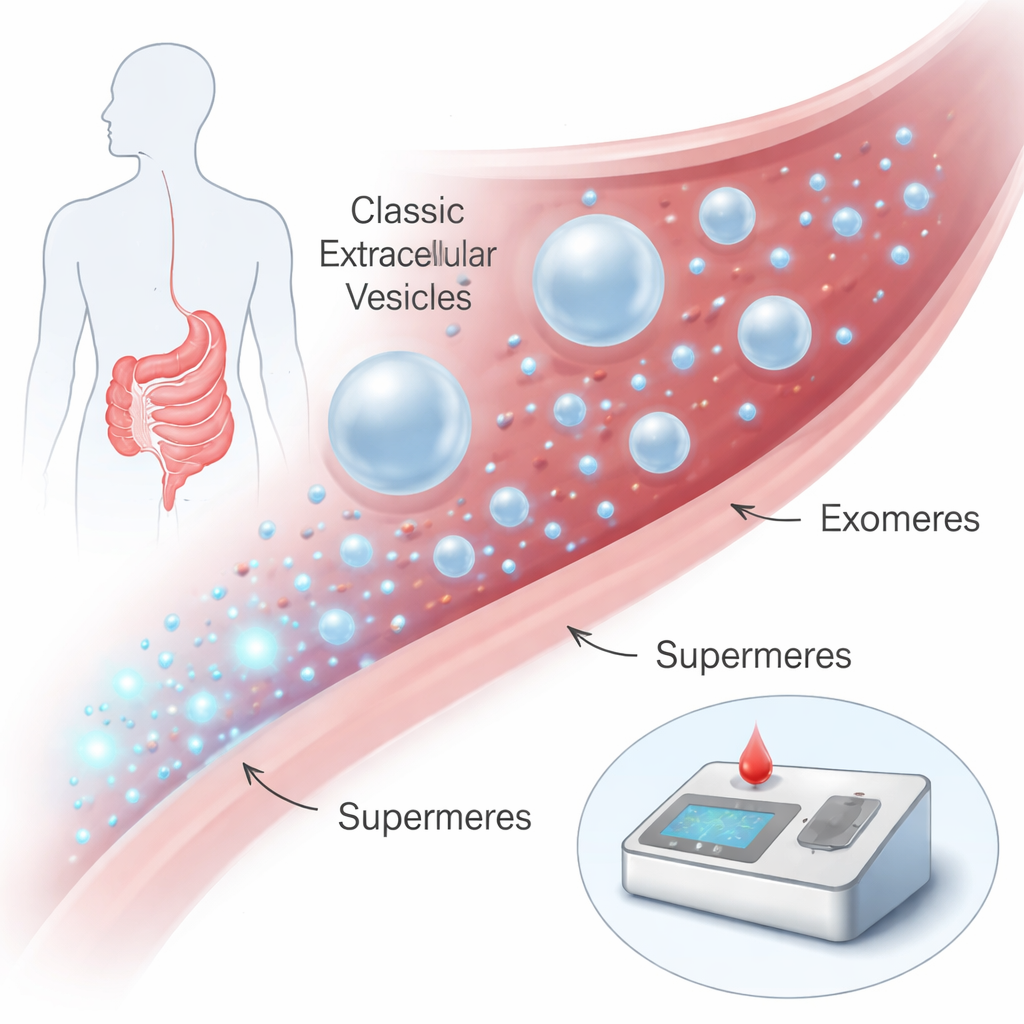
血流中的微小信使
我们的细胞不断向体液(如血液)释放纳米级小包裹。多年来,大多数注意力集中在有膜的颗粒,如外泌体和其他细胞外囊泡上,它们可以在细胞间运输蛋白质和遗传物质,并被作为疾病生物标志物加以研究。最近,研究者又发现了更小的无膜颗粒,称为外微体(exomeres),以及更小的超级小体。超级小体直径仅约15–25纳米——数千个可并排跨过一根人发的宽度——但它们富含与疾病相关的分子。早期工作提示超级小体可能特别富含癌症信号,但由于需要数日超速离心与专用设备,它们长期难以分离与研究。
超级小体的独特之处
研究团队从癌细胞培养物和人血液中仔细分离出三种主要纳米颗粒:小型细胞外囊泡、外微体和超级小体。他们证实每一组都有特定的尺寸范围,超级小体最小。然而关键差异在于电学特性。超级小体带有比其他颗粒强得多的负表面电荷——约为热随机运动开始显著影响的两倍——这一点主要归因于附着在表面的RNA链。当研究者用酶消化这些RNA后,电荷显著下降,表明表面RNA对超级小体的电静特征至关重要。蛋白质绘图显示,超级小体还具有自己的“身份证”:如HSPA13、ENO2和DDR1等蛋白在超级小体上高度富集,但在其他颗粒类型中几乎不存在,类似于识别常规细胞外囊泡的经典标志物。
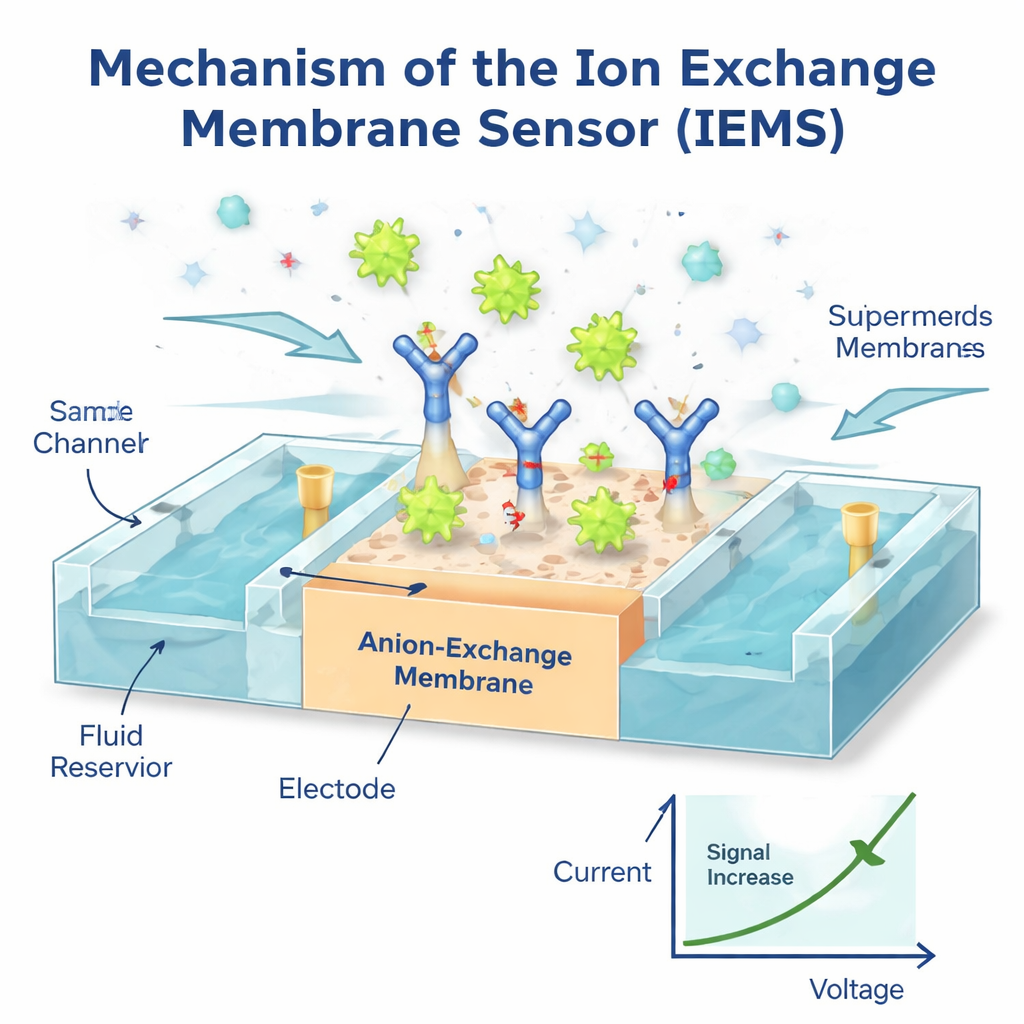
一种听“电荷”的快速传感器
为了利用这些独特性质,作者构建了一种离子交换膜传感器(IEMS),这是一种微小设备,通过带电颗粒结合到其表面时电流变化来感测。研究者在特殊膜上涂覆了能捕捉目标蛋白(例如癌症相关标志物)的抗体,从流动的血样中抓取靶分子。由于超级小体带电很强而大多数其他颗粒和游离蛋白带电较弱,只有被捕获的超级小体会显著改变膜的电流–电压特性。结果产生了强烈且选择性的电信号,反映携带该标志物的超级小体数量。使用该装置,团队能够在约30分钟内、仅用50微升样本检测到低至每毫升一百万个超级小体,检测范围跨越约千倍浓度,无需耗时纯化。向健康血浆中加入已知量超级小体的测试显示几乎完全回收,测量结果与更慢的高端光学仪器相匹配。
优于现有纳米颗粒标志物
在传统方法与快速方法并用下,研究者将超级小体与外微体和小型细胞外囊泡在结直肠癌患者与健康志愿者的血样中做了直接比较。他们关注几种出现在三种颗粒类型中的蛋白,包括已知肿瘤标志物如CEA和GPC1。几乎对所有共享蛋白,超级小体携带的信号在区分癌症患者与健康个体方面都表现得更好或不逊色,而外微体通常显示出较少的诊断价值。超级小体特异的蛋白如HSPA13、ENO2和DDR1尤其具有鉴别力:在健康血浆中几乎检测不到,但在结直肠癌中显著升高,在两组之间提供了极佳的区分度。引人注目的是,在两名于手术前后随访的患者中,肿瘤切除后超级小体水平显著下降,而传统囊泡的信号几乎无变化,这表明超级小体与肿瘤负荷高度相关。
这对未来癌症检测意味着什么
为在实际条件下检验他们的新传感器,团队使用IEMS测量了携带不同标志物的超级小体,样本来自结直肠癌、胰腺癌、胶质母细胞瘤患者及健康供者。快速、无需分离的读数与慢得多的超速离心加光学分析结果高度一致,证实速度并未以牺牲准确性为代价。在结直肠癌中,基于超级小体的测量优于血液总CEA水平——这是长期使用的临床标志物。总体而言,研究结果表明,超级小体并非另一种显微学趣闻,而是一个强大且易获取的癌症信息来源。如在更大且更具多样性的患者群体中得到验证,使用紧凑的基于电荷的传感器测量携标志物的超级小体,可能成为筛查结直肠癌、监测治疗并在更短时间、更少样本量和更低复杂度下实现个性化治疗的实用方法。
引用: Kumar, S., Sinclair, J.A., Shi, T. et al. Surface markers on supermeres outperform extracellular vesicles in colorectal cancer diagnosis. Sci Rep 16, 5989 (2026). https://doi.org/10.1038/s41598-026-36626-8
关键词: 结直肠癌, 血液生物标志物, 细胞外纳米颗粒, 超级小体, 生物传感器技术