Clear Sky Science · zh
基于全基因组CRISPR筛选构建并初步验证子宫内膜癌孕酮耐药关键基因网络
为何有些子宫癌对激素不再“听话”
对于许多仍希望保留生育能力的早期子宫内膜(子宫内膜)癌患者,口服模拟天然激素孕酮的药物可以在保留子宫的同时缩小肿瘤。然而多达三分之一的此类癌症要么从未响应,要么很快变得耐药,迫使患者转向手术或更强烈的治疗。本研究利用强大的基因编辑工具绘制出哪些基因使子宫内膜癌细胞不再对孕酮作出反应,这为未来开发检测方法和药物以延长该疗法有效期指明了方向。
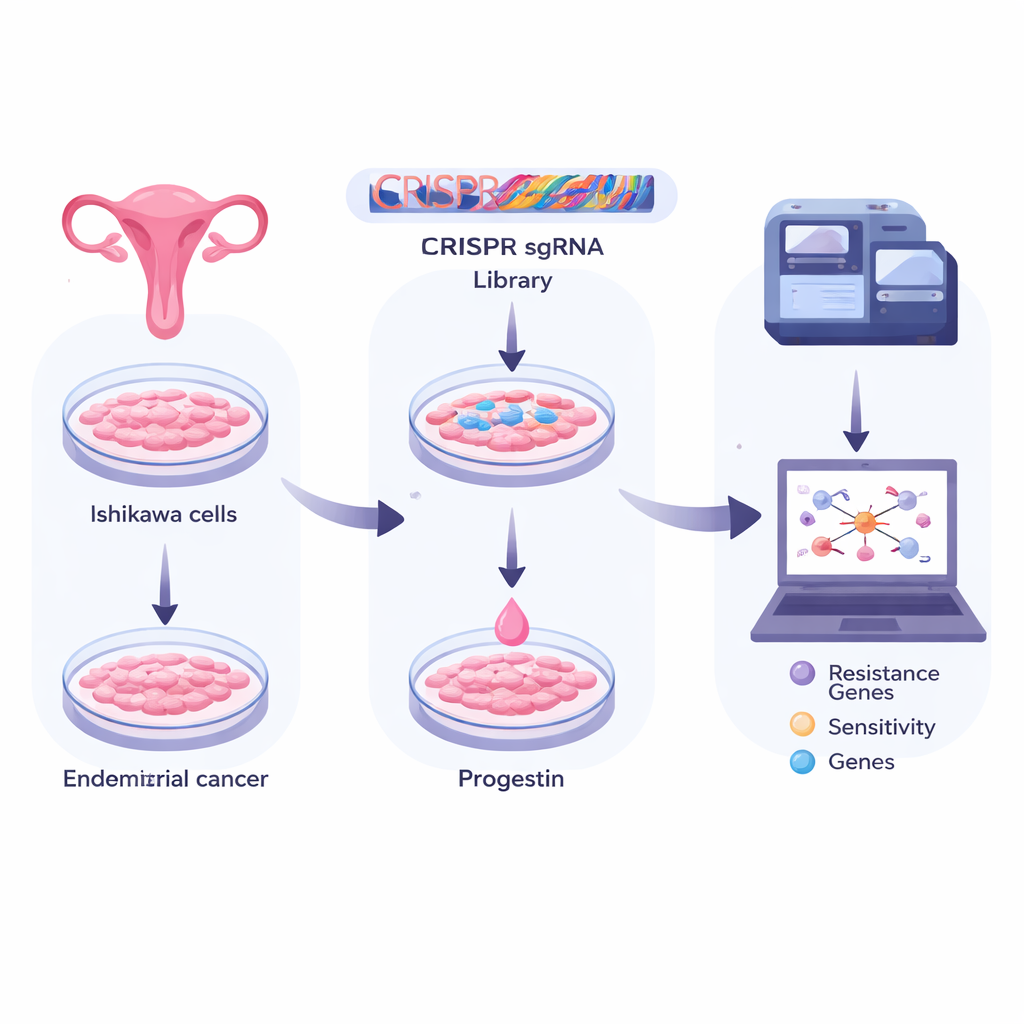
用“基因剪刀”全基因组搜索
研究人员使用了Ishikawa细胞,这是一种广泛使用的子宫内膜癌模型。他们用包含大量CRISPR“基因剪刀”的文库感染了数百万个此类细胞,每个剪刀都被设计去关闭不同的人类基因。这样就生成了一个巨大的细胞库,原则上每个细胞都有一个独特基因被敲除。然后团队将细胞分为若干组:一组冷冻作为基线,一组仅暴露于无害溶剂,另一组则在多天内用一种常见的合成孕酮(醋酸甲羟孕酮,MPA)处理。通过对每组中存活的CRISPR标签进行深度测序,他们可以看出哪些基因敲除帮助细胞在孕酮处理下存活或死亡。
分辨帮助或妨碍药物反应的基因
分析这批海量数据需要复杂的统计方法。团队采用了两种互补的方法,RRA和MLE,按基因对细胞抵抗孕酮(耐药基因)或更易死亡(敏感性基因)的保护强度进行排序。他们在两端各发现了数百个候选基因。许多基因在处理DNA复制与修复、RNA合成与加工以及细胞代谢的通路中聚集。换言之,使细胞读取、维护和执行遗传信息的基本机器似乎与子宫内膜癌细胞是否听从孕酮的“停止生长”信号密切相关。
将名单缩小到最重要的参与者
为避免追踪假阳性,科学家们将CRISPR筛选的命中基因与他们实验室早期的一个数据集交叉核对,该数据集中比较了普通癌细胞与随时间获得孕酮耐药的一株细胞。通过寻找在两次筛选中都出现并显示一致变化的基因,他们将名单提纯为大约五个似乎促进耐药的基因和二十个似乎增强敏感性的基因。公共癌症数据库显示,许多阻止耐药的基因在最常见类型的子宫内膜癌中表达更高,而若干促进耐药的基因则与较差的患者预后相关,这表明这些信号在真实肿瘤中也具有意义,而不仅仅是在体外细胞中。
在细胞和小鼠中验证关键基因
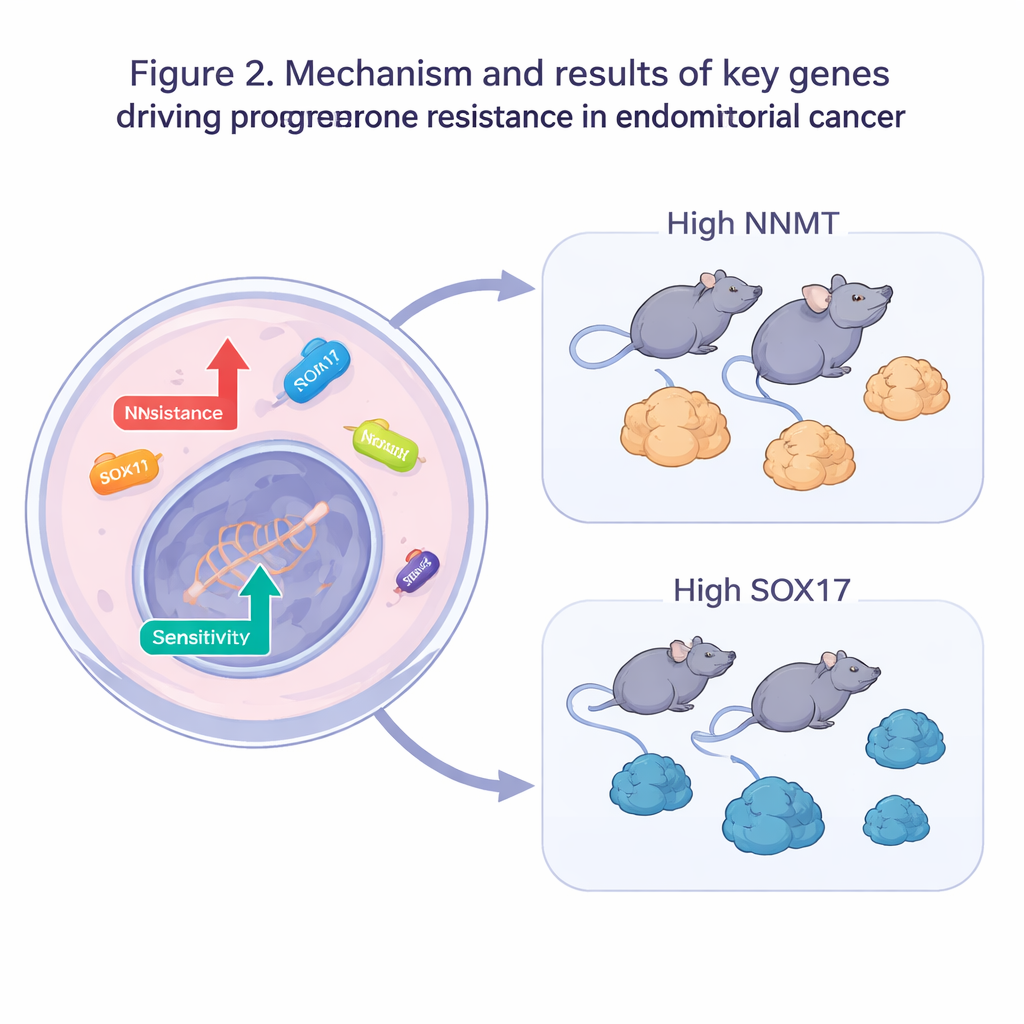
随后,团队从大数据转向动手实验。在孕酮耐药细胞中,他们分别关闭了五个疑似耐药基因中的每一个,或增强了五个疑似敏感性基因。当这些被改造的细胞暴露于孕酮时,更多细胞死亡,所需抑制生长的药物剂量显著降低,证实了单个基因的调控可以恢复对激素的敏感性。其中两个基因尤为突出:NNMT,参与细胞代谢;以及SOX17,一个帮助调控细胞发育与行为的基因。在小鼠肿瘤模型中,提高NNMT表达使肿瘤对孕酮反应减弱,而增强SOX17则使耐药肿瘤在相同治疗下缩小更多。
这些发现对患者可能意味着什么
简言之,研究构建了一个早期的“线路图”,说明子宫内膜癌细胞如何决定是否响应孕酮。结果表明,耐药不仅仅是失去孕酮受体,还涉及DNA和RNA处理方面的更深层变化以及诸如NNMT和SOX17等关键调控基因。将来,读取该基因网络的血液或组织检测可能帮助医生预测谁会从基于激素的保留生育治疗中受益。更有前景的是,抑制耐药基因或增强敏感基因的药物有望与孕酮联合使用,使这一温和治疗选项对更多患者且更长时间保持有效。
引用: Li, X., Wang, S., Qiu, Z. et al. Construction and initial validation of key gene network for progesterone resistance in endometrial cancer based on genome-wide CRISPR screening. Sci Rep 16, 8030 (2026). https://doi.org/10.1038/s41598-026-36534-x
关键词: 子宫内膜癌, 孕酮耐药, CRISPR筛选, 基因网络, 激素治疗