Clear Sky Science · zh
通过生物信息学分析鉴定高血压合并2型糖尿病患者的细菌关键基因和治疗靶点
你的肠道为何与血压和血糖相关
高血压和2型糖尿病常常同时出现,增加心肌梗死、中风和肾脏疾病的风险。长期以来,医生通常将这些疾病分开治疗,侧重于作用于心脏、血管或胰岛素的药物。本研究提出了一个不同的问题:我们肠道中生活的微小微生物——以及它们携带的基因——是否可能同时推动这两种问题,并且是否能揭示新的治疗途径?
肠道内部的隐秘世界
研究者分析了124名成人的粪便样本,将29名同时患有高血压和2型糖尿病的人与95名健康志愿者进行比较。通过对细菌标记的基因测序,他们构建了详细的微生物存在情况以及每个人肠道群落多样性的图谱。患有两种疾病的人表现出更丰富且分布更均匀的细菌群落,并且这些群落在聚类上与健康个体明显分开,这表明他们的肠道生态系统已发生重组,而不仅仅是轻微紊乱。
从有益到有害的微生物转变
当团队深入分析哪些细菌类型最为丰盛时,发现了明显的模式。在健康人群中,帮助产生短链脂肪酸的细菌——这些化合物有助于维持肠道黏膜健康并调控炎症和代谢——较为常见,包括拟杆菌属(Bacteroides)、普氏菌属(Prevotella)、玫瑰杆菌属(Roseburia)和阿克曼氏菌属(Akkermansia)等。在既有高血压又有糖尿病的人群中,许多此类有益微生物显著减少。与此同时,与炎症和代谢失衡相关的细菌(如大球菌属Megasphaera、乳酸杆菌属Lactobacillus、链球菌属Streptococcus和韦荣氏菌属Veillonella)更为常见。有19个细菌类群在患者与健康对照之间持续差异,提示肠道环境整体向有利于低度炎症和代谢压力的方向转变。
从微生物到分子“控制旋钮”
仅计数微生物无法解释它们如何影响机体,因此科学家使用计算工具推断肠道细菌可能的功能。他们预测了哪些代谢通路——一系列化学反应——在患者中更活跃或不活跃。在超过一千条通路中,有195条表现出显著改变,许多与细菌合成蛋白、能量代谢以及核苷酸和氨基酸等构件的处理有关。通过构建相应细菌蛋白相互作用的网络,团队确定了十个位于网络关键节点的“枢纽”基因。这些基因(如gltB、gyrB、fusA和mdh)像控制旋钮一样调节细菌的核心功能,例如能量生成、DNA复制、蛋白质合成以及脂肪酸和核苷酸代谢。由于这些活动与炎症、血管健康和葡萄糖控制紧密相关,微生物基因的变化可能通过级联效应影响血压和血糖。
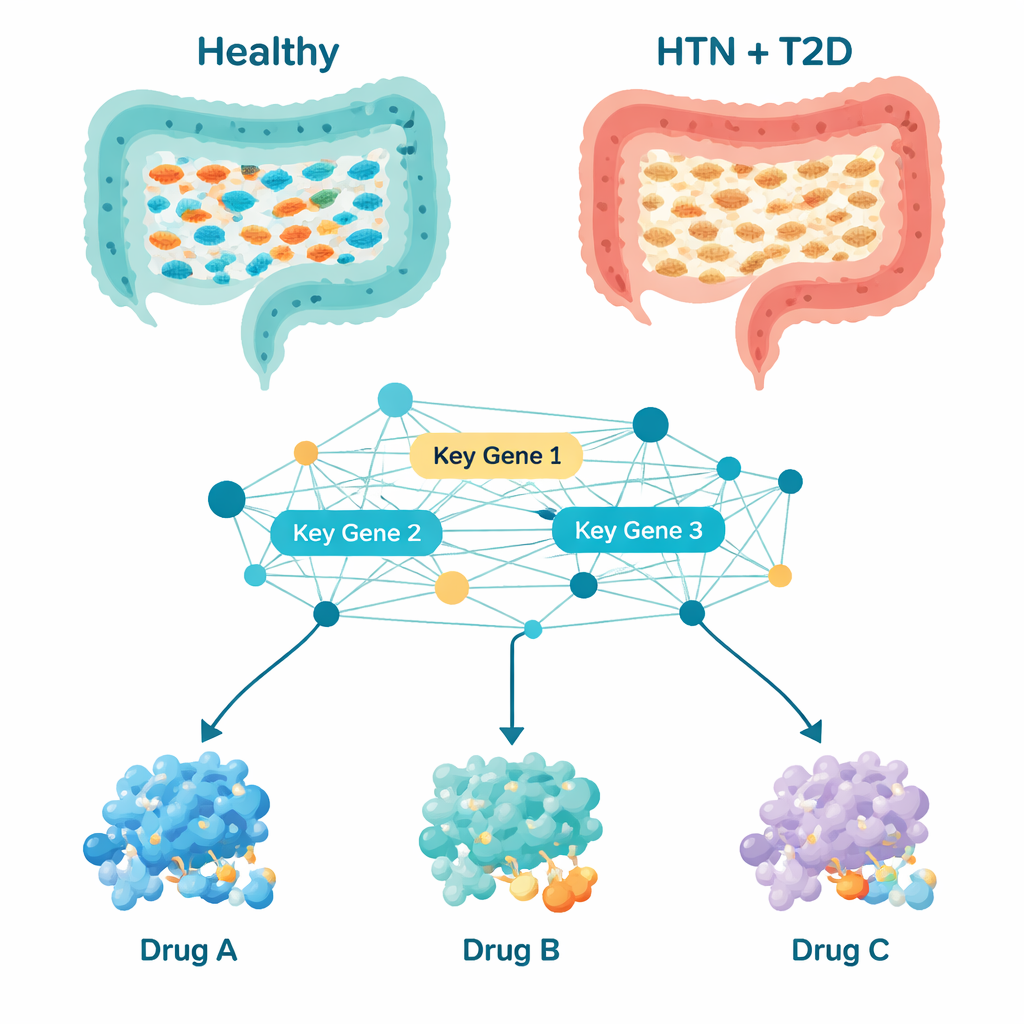
为现有药物寻找新用途
利用这份细菌“控制基因”名单,研究者进行了基于计算的药物筛选。他们收集了189种已用于高血压、2型糖尿病或相关代谢问题研究的药物,并使用分子对接——本质上是一个三维拼图——来评估哪些化合物可能最紧密地与这十个关键细菌基因所编码的蛋白结合。三种候选物脱颖而出:柑橘类水果中存在的植物来源化合物柚皮苷(Naringin)和新橙皮苷(Neohesperidin),以及已获批用于2型糖尿病的溴隐亭(Bromocriptine)。对这些复合物进行持续100纳秒(注:原文为“100亿分之一秒”,推测为100纳秒)级别的详细模拟表明,新橙皮苷和溴隐亭形成的复合物尤其稳定,意味着这些药物在体内可能可靠地结合并影响靶向细菌蛋白。对这些化合物的药物相似性以及吸收、分布、代谢和清除性质的额外评估指出,溴隐亭在近期转化为临床应用方面最为可行,尽管这三者都需要严格的安全性和剂量研究。
对未来医疗的意义
简而言之,这项工作绘制出一条三步链:既患高血压又患2型糖尿病的人往往具有独特的肠道微生物组;这种微生物组携带的一组细菌基因可能会推动代谢与血管走向有害方向;而一些现有药物似乎能够靶向这些细菌基因。该研究并未证明改变这些微生物或其基因能治愈疾病,也未在患者中测试任何治疗方法。但它为基于微生物组的诊断和治疗勾画了蓝图,未来医生或许可以通过改变肠道细菌或使用定制药物来减轻高血压与糖尿病并存的负担。
引用: Rahat, M.T.I., Sumi, M.S.A., Nurejannath, M. et al. Identification of bacterial key genes and therapeutic targets in hypertensive patients with type 2 diabetes through bioinformatics analysis. Sci Rep 16, 6431 (2026). https://doi.org/10.1038/s41598-026-36467-5
关键词: 肠道微生物组, 高血压, 2型糖尿病, 细菌基因, 药物再利用