Clear Sky Science · zh
识别LMNA心肌病中新型miRNA–mRNA互作网络的整合方法
为何这些微小的心脏调节因子很重要
扩张型心肌病是一种严重疾病,心脏腔室扩大且变弱,常导致心力衰竭、危险性心律失常,甚至猝死。对许多家庭而言,这种疾病具有遗传性,其中LMNA基因的变异是一个常见原因。本研究提出了一个看似简单但影响重大的问题:在因LMNA突变受损的心脏中,哪些基因被打开或关闭,又有哪些微小RNA在操纵这些开关?通过详尽描绘这些分子间的对话,研究指向了预测、监测并可能在未来治疗这种侵袭性心脏病的新路径。
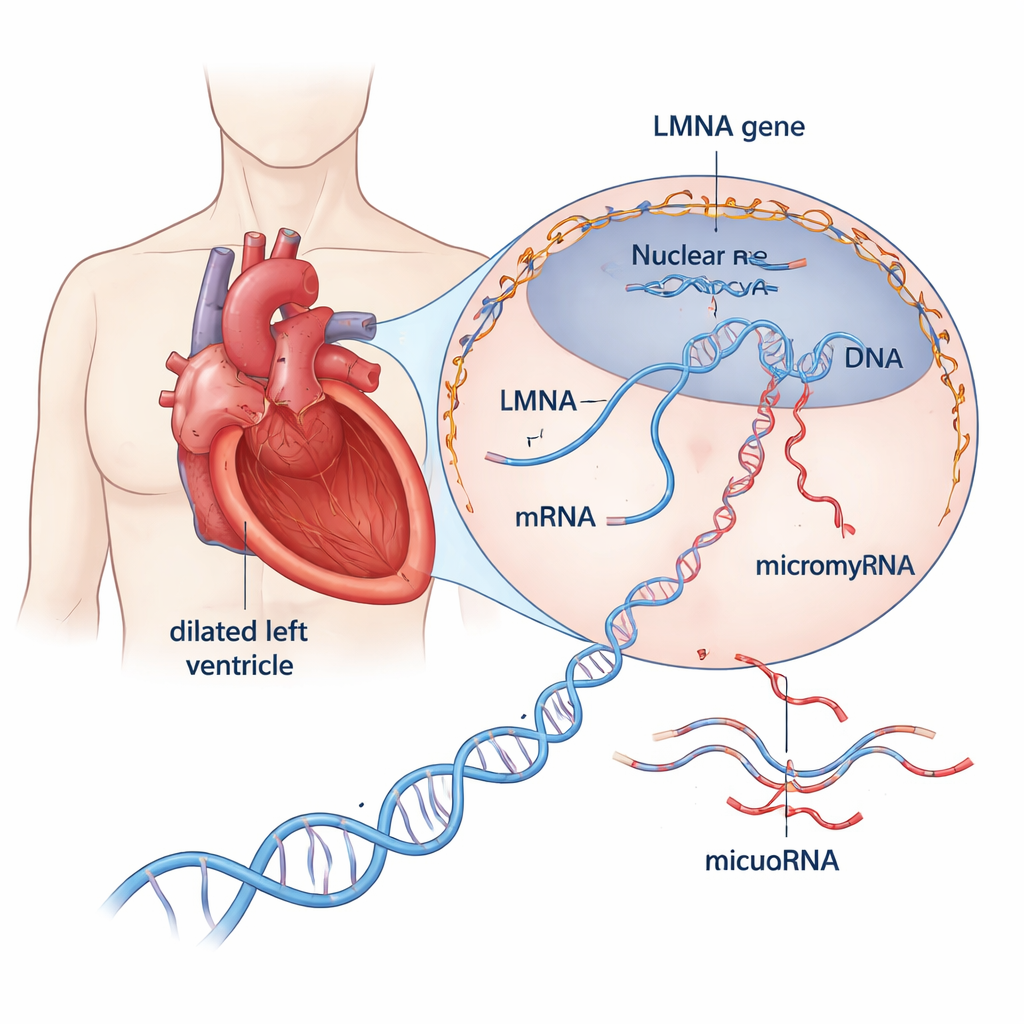
对一种危险心脏病的更深入观察
扩张型心肌病使心脏的主泵室扩张并变薄,削弱其将血液输送全身的能力。大约三分之一到一半曾被称为“特发性”的病例现在被发现具有遗传基础。在30多个相关基因中,LMNA尤为突出:该基因的有害变体约占遗传性病例的10%,并与疾病进展迅速、早发性心律问题以及较高的猝死风险相关。LMNA编码形成包围细胞DNA的结构蛋白,帮助维持细胞核形态并影响哪些基因处于活跃状态。然而,缺陷LMNA蛋白如何驱动心脏走向衰竭仍不清楚。
追踪小鼠心脏内的信息流
为此,研究人员使用了携带已知LMNA突变(R249W)的小鼠模型,这些小鼠会发展出与人类疾病相似的扩张型心肌病。在50周龄——小鼠表现为心室扩大、泵血功能下降并出现纤维化瘢痕时,团队提取了心组织并检测两类RNA:信使RNA(mRNA),其携带制造蛋白质的指令;以及微小RNA(miRNA),短小的不编码蛋白的链,通过阻断或降解特定mRNA来微调基因活性。通过高通量测序和严格的统计筛选,他们鉴定出在突变心脏中变化的2,148个基因和与健康小鼠相比上调或下调的53种miRNA。
病变心肌细胞内发生了哪些变化
当研究人员将变化的基因归入生物学通路时,出现了若干主题。许多改变的基因与心肌收缩、细胞之间及其与周围支撑基质的粘附、电信号在心脏中的传导,以及细胞处理脂肪以产生能量的方式有关。这些发现与LMNA相关疾病的临床特征相吻合:组织僵硬、纤维化;有利于心律失常的电传导紊乱;以及能量代谢受损。利用既定数据库的通路分析证实在细胞外基质重塑、电压门控离子通道、心脏中的类突触式通信和脂肪酸代谢方面富集——提示LMNA突变破坏的是多个相互关联的系统,而非单一故障点。
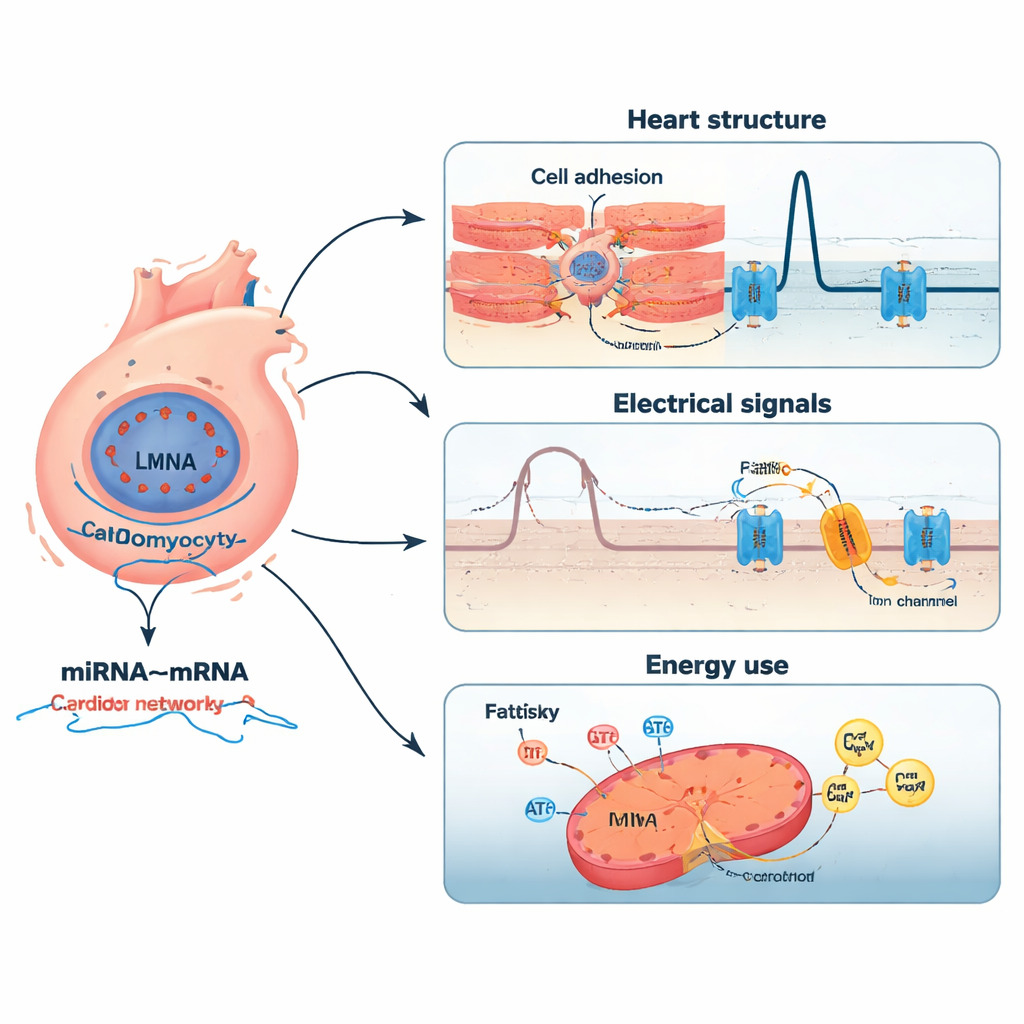
微小开关与其靶标的网络
研究进一步将miRNA与其可能的mRNA靶标配对。通过相关性分析并与大型实验验证的相互作用数据库交叉核对,作者组装了一个高可信度的网络,包含2,197对miRNA–mRNA,涉及12种关键miRNA。部分miRNA活性增强,似乎抑制了对心脏发育、钙处理及抗氧化应答至关重要的基因;另一些miRNA活性降低,可能解除对参与细胞黏附、炎症和心脏结构支架重塑基因的抑制。例如,一种miRNA(miR-183-5p)与Wnt信号通路中的受体相关,该通路影响细胞间通信;另一种(miR-3473a)则连接到一个对心跳节律至关重要的钙释放通道。总体来看,这些网络描绘了微小RNA调节因子的细微变化如何放大LMNA突变的影响。
从分子图谱到未来治疗
对非专业读者来说,结论是:这项研究提供了一张详细地图,展示了LMNA突变如何在基因调控层面重塑心脏的内部线路。与其说是单一“有害基因”,不如说是信息层级的级联改变——许多由miRNA协调——影响心脏结构、电稳定性和能量利用。尽管研究在小鼠中进行并大量依赖计算分析,但它突出了若干特异的miRNA–基因配对,作为未来血液生物标志物或靶向治疗的有希望候选对象。长期来看,调控这些微小RNA开关可能帮助医生更好地预测高风险人群、更精确地监测疾病进展,并为受LMNA相关心肌病影响的家庭设计更个体化的治疗方案。
引用: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
关键词: 扩张型心肌病, LMNA基因, 微小RNA, 基因调控, 心力衰竭