Clear Sky Science · zh
从计算QSAR建模到体外MTT测定:针对三阴性乳腺癌(TNBC)和皮肤癌的新型uPAR先导化合物的实验验证
这项研究为何重要
像三阴性乳腺癌和某些类型的皮肤癌因扩散迅速且常对常规疗法产生耐药而极难治疗。本研究探讨了癌细胞表面一个有前景的新靶点——称为uPAR,并展示了如何将计算机辅助药物设计与实验室实验相结合,发现可能减缓或阻止这些侵袭性肿瘤扩散的新药物候选分子。
帮助癌症扩散的“门道”
为了让肿瘤变得致命,癌细胞必须从原发部位脱落、侵蚀周围组织、进入血液并在远处器官定植。uPAR在这一过程中起重要辅助作用。它位于癌细胞表面,与伙伴蛋白协同激活可溶解周围支撑结构的酶,从而使细胞更易移动和侵入。uPAR在三阴性乳腺癌细胞和某些皮肤癌细胞中含量特别高,其丰度与更快的生长、更强的侵袭性和更差的患者预后相关。因此,uPAR是一个有吸引力但迄今为止未被充分利用的抗癌药物靶点。
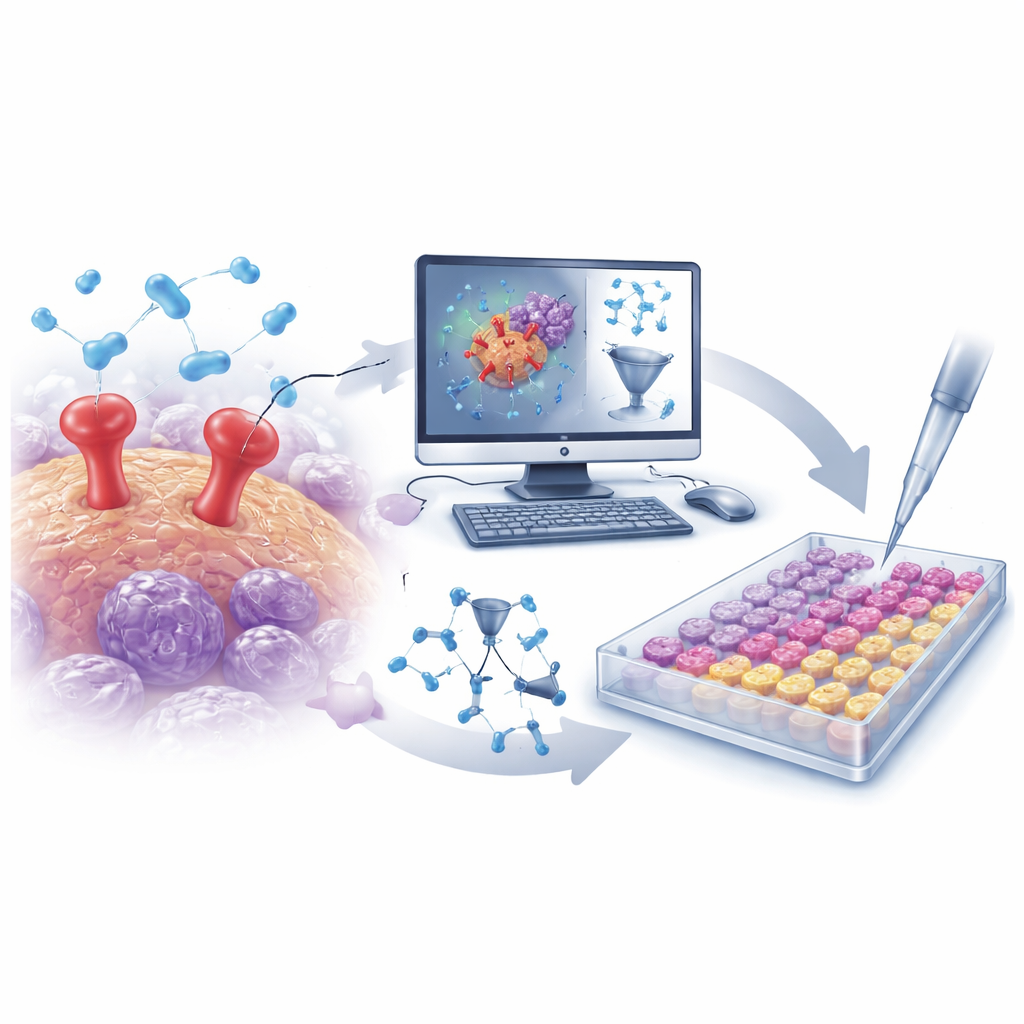
用智能算法挖掘大规模化学数据
研究人员首先从公共数据库汇集了500多种已知的uPAR阻断分子。将每个分子的结构转化为数千个数值描述符,这些描述符捕捉诸如大小、形状、电荷分布和柔性等特征。基于这些数据,团队建立了定量构效关系(QSAR)模型——这是一种能学习哪些结构特征倾向于使分子成为更强uPAR抑制剂的数学工具。经过谨慎的验证以避免过拟合,该模型在未知化合物上表现出较高的预测能力,并强调了若干会增强或削弱uPAR阻断作用的关键特征。这些见解指导了寻找新型、更优设计分子的工作。
从虚拟筛选到真实试管
借助训练好的QSAR模型,团队对约3万种针对蛋白酶的分子库进行了虚拟筛选。模型迅速将这一庞大候选池缩小到一小组可能的uPAR抑制剂。与此同时,计算对接模拟用于评估每个候选分子与uPAR结合位点的契合程度,分子动力学模拟则测试这些对接复合体随时间是否保持稳定。通过这套综合的体内外(in‑silico)筛选,两种突出的分子脱颖而出:D685‑0061被QSAR模型标记为抑制性很强的分子,而C878‑1660则通过对接和模拟显示出与uPAR形成特别稳定相互作用。
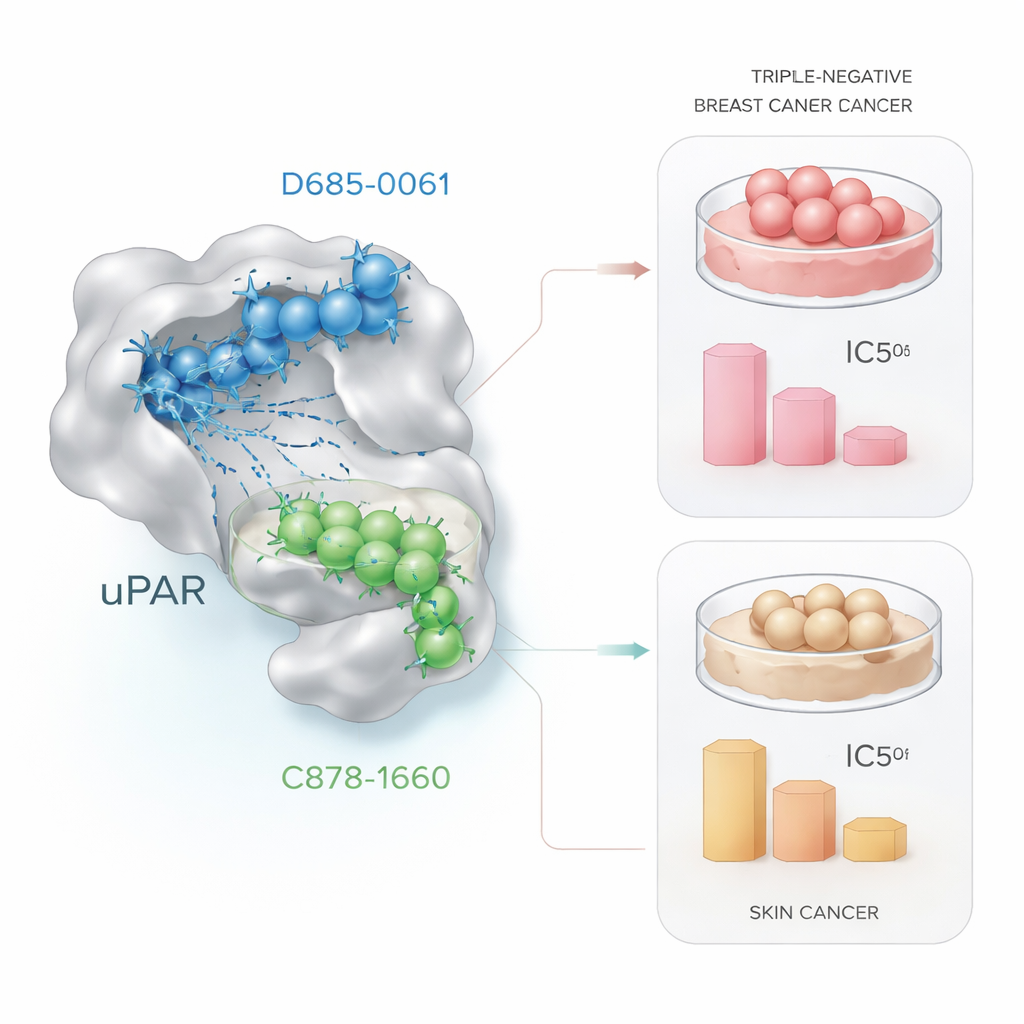
在癌细胞中检验候选分子
计算机预测只有在能转化为真实生物学效应时才有意义。为此,研究人员将活癌细胞暴露于逐渐升高剂量的两种先导分子,并采用一种常规实验方法MTT测定来评估细胞存活率。在三阴性乳腺癌细胞(MDA‑MB‑231)中,D685‑0061更有效地杀死细胞,其在约21微摩尔时使细胞活力降低约一半,而C878‑1660则大约需要四倍剂量。在显微镜下,接受D685‑0061处理的细胞显示出程序性细胞死亡的明显特征,如变圆、从基底脱落并碎裂。相比之下,在皮肤癌细胞(A431)中,C878‑1660杀伤力更强,在约19微摩尔时实现50%细胞死亡,而D685‑0061约需28微摩尔,同样伴随明显的剂量依赖性损伤。
对未来癌症治疗的意义
这项工作并未立即带来一款新药,但它确实提供了两个有前景的起点,以及同样重要的一套强有力的发现蓝图。通过将大数据建模、三维模拟和严谨的细胞实验相结合,研究表明uPAR可以被选择性地用小分子靶向,损伤侵袭性的乳腺和皮肤癌细胞。D685‑0061和C878‑1660现为先导化合物,化学家可以进一步改造以提高效力、改善安全性并优化体内药代动力学。从长远看,基于这种方法开发的药物有望阻断由uPAR驱动的癌症扩散,将一些当今最危险的肿瘤转变为更易管理的疾病。
引用: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
关键词: uPAR抑制剂, 三阴性乳腺癌, 皮肤癌, 计算机辅助药物设计, MTT细胞活力测定