Clear Sky Science · zh
密度泛函理论研究:环磷酰胺和巯基嘌呤在共价三嗪框架(CTF-2)上的吸附及其药物传递应用
为何更“聪明”的化疗很重要
化疗药物能挽救生命,但它们往往像泛光灯而非聚光灯——在攻击癌细胞的同时也损伤健康细胞。这会导致严重副作用,从疲劳和感染到器官损伤。本文所述的研究探索了一种超薄、高孔隙的材料——共价三嗪框架(CTF-2),将其比作一种“智能海绵”,能够更安全、更高效地承载两种长期使用的抗癌药物——环磷酰胺和巯基嘌呤(Purinethol),并在类似肿瘤的环境下释放它们。
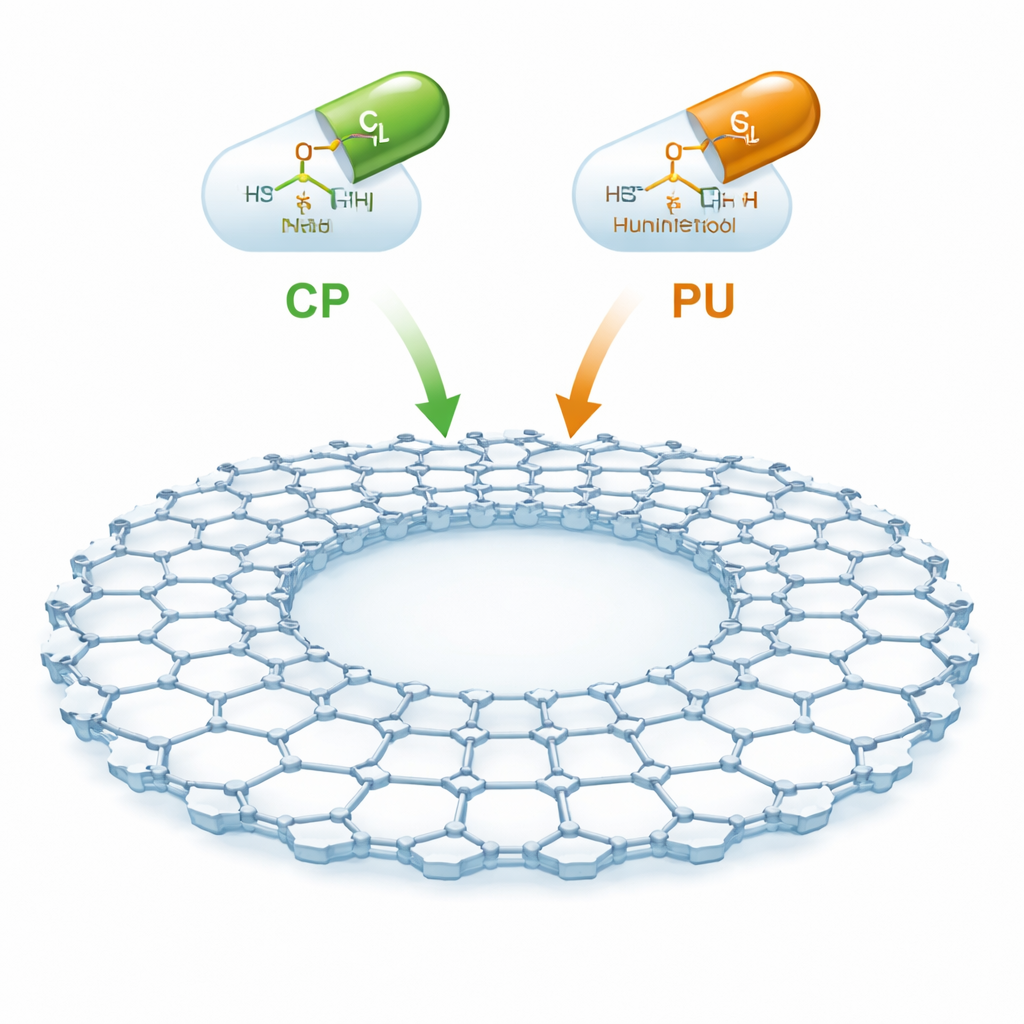
一种新型的分子海绵
CTF-2 是一种由碳和氮环通过共价连接构成的人工材料,形成扁平的片层网络,含有大的中心腔体和大量空隙。由于它薄、稳定且多孔,具有巨大的内表面积可用于捕捉药物分子。作者关注两种重要的抗癌药:环磷酰胺,广泛用于血液癌和实体瘤;以及巯基嘌呤(亦称巯基嘧啶或 mercaptopurine),用于白血病和某些炎性肠病。其思路是将这些药物以温和的方式停靠在 CTF-2 表面,使其能在血液中被输送并更有选择性地释放,从而减少对健康组织的损伤。
用计算实验探测看不见的相互作用
研究团队没有在湿实验室中直接实验,而是使用先进的量子级别计算(密度泛函理论及相关方法)来评估每种药物与 CTF-2 的吸附强度及复合物的结合机制。他们优化了 CTF-2 与每种药物的构型,测量接触处原子间的距离,并计算药物附着到框架时的能量得失。对环磷酰胺,计算得到的吸附能约为 −1.04 电子伏特,略强于对巯基嘌呤的 −0.82 电子伏特。这些数值在校正技术性误差并模拟水溶剂效应后仍然明显有利,表明两种药物结合足够牢固以便装载,但又不会强到无法随后释放。
温和的力在发挥关键作用
研究表明,药物与 CTF-2 之间的“胶合剂”并非强的共价键,而是一种由非共价弱相互作用构成的网络。通过对电子密度的专门分析——实际上是描绘共享电子分布的图谱——研究者发现以色散力(范德华力,类似壁虎能贴附墙面的弱作用)和温和的静电相互作用为主。这些相互作用发生在药物与框架上氢、氮、氧、硫、碳原子之间的短距离但非成键距离处。把总体吸引力分解为不同成分的附加计算证实,静电和色散(范德华)力提供了大部分稳定的拉力,而斥力则阻止药物过度嵌入或不可逆地结合。
稳定装载与可调释放的信号
团队还检查了药物吸附到 CTF-2 时电子如何迁移,以及这如何改变基本的电学特性。他们观察到药物与框架之间存在小但明确的电荷转移,并且填充态与空态之间的能隙略有缩小。这意味着材料在装载后反应性和导电性会发生细微调节,对未来的传感或诊疗学(theranostics)应用有益。关键是,当模拟肿瘤附近更酸性的环境(通过添加额外质子)时,计算所得的结合变弱且接触距离增大。简单来说,模拟结果表明 CTF-2 可在类似血液的正常条件下牢牢携带药物,但在肿瘤样的酸性环境中更容易释放它们——正是靶向传递所期望的行为。
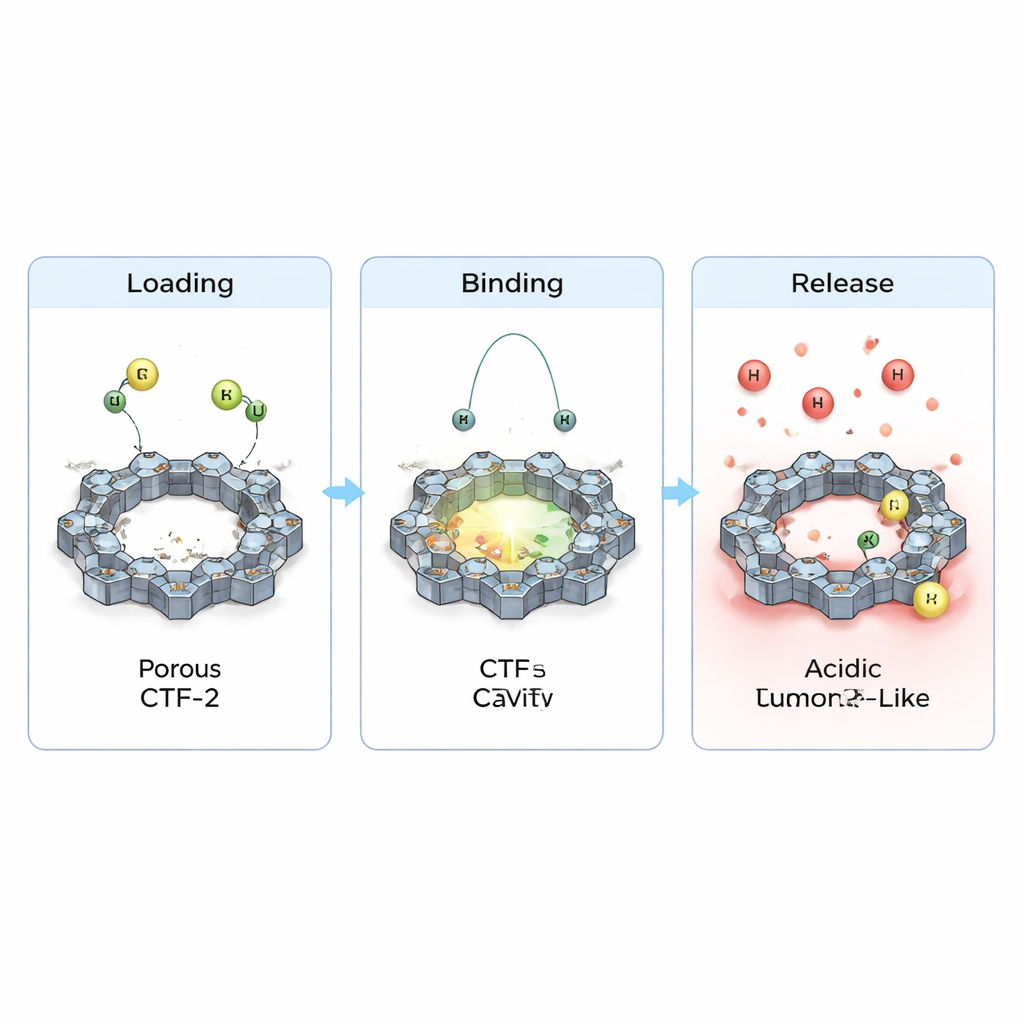
这对未来癌症治疗意味着什么
综合这些计算结果,CTF-2 被描绘成一种有前景的环磷酰胺和巯基嘌呤载体:它能将药物稳定地装载到多孔表面,保护药物在循环过程中不被过早释放,并在肿瘤局部化学环境变化时释放药物。尽管本工作是理论性的、需要实验验证,但结果表明,像 CTF-2 这样精细设计的富氮框架可能有助于把历来有效却不够精准的化疗药物转变为更“智能”的药物——在最需要的部位递送高效剂量,同时减轻对健康细胞的附带伤害。
引用: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
关键词: 纳米载体, 药物递送, 癌症化疗, 共价三嗪框架, 计算建模