Clear Sky Science · zh
一种带有专家修订的交互级联深度学习框架,用于精确分割纹状体亚区
为什么绘制微小脑区很重要
纹状体是埋藏在大脑深处的一个小结构,在运动和动机中起核心作用,并在帕金森病等疾病中受到严重影响。医生常用 PET 和 MRI 扫描来测量该区域的化学变化,但纹状体被划分为许多难以精确观察和描绘的微小亚区。本文介绍了一种新的计算机辅助方法,称为 StriaSeg‑iARM,能帮助专家更准确、更高效地绘制这些边界,即使面对因衰老或疾病而改变的大脑也能适用。
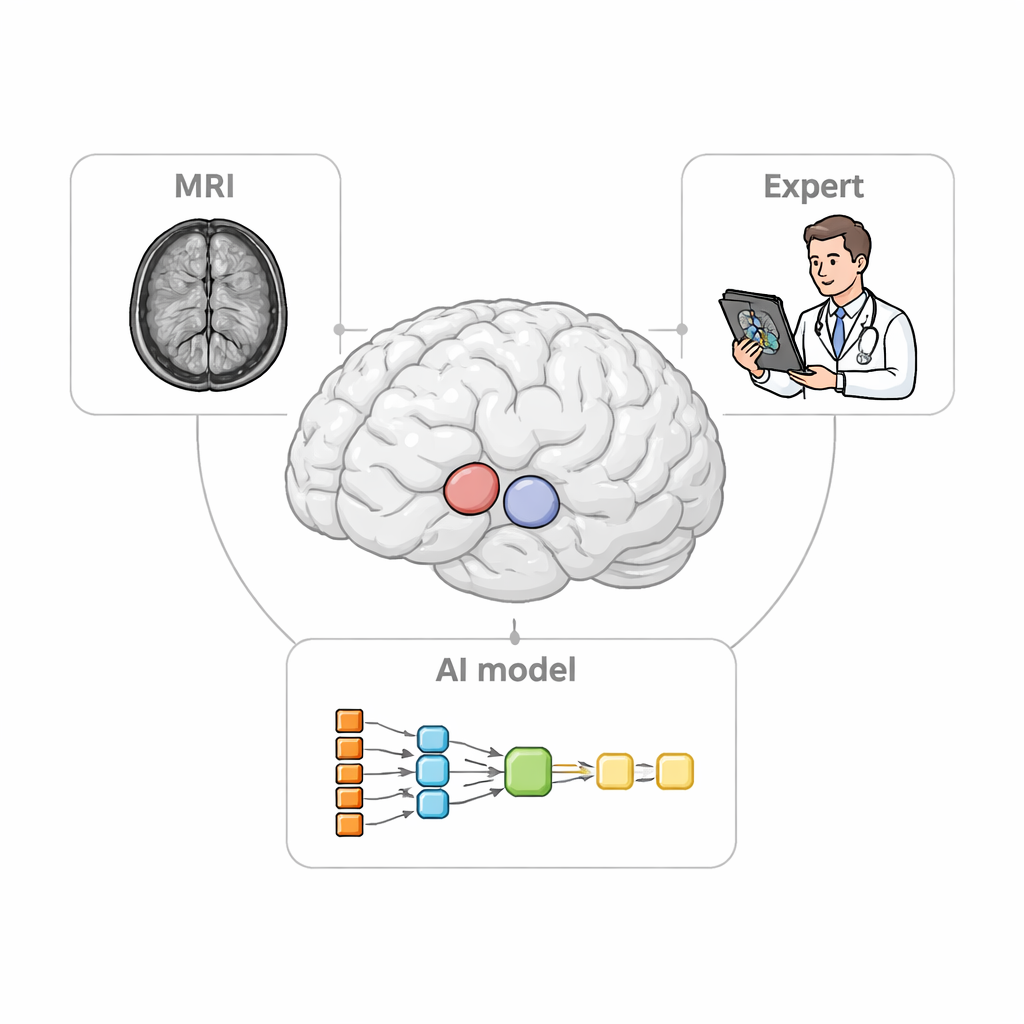
肉眼可见的临床问题
在评估如帕金森病之类的病症时,神经学家依赖 PET 扫描来追踪多巴胺相关信号在纹状体不同部位的变化。要正确做到这一点,首先必须在 MRI 上定义小的三维“感兴趣区”,这些区域作为 PET 数据的测量容器。手工描绘这些区域既慢又枯燥,而且不同专家之间可能存在差异。现有软件通常只能自动定位较大结构,在脑萎缩或畸变的患者中常常表现不佳——这在晚期神经退行性疾病中很常见。这些缺陷会模糊真实的损伤模式,削弱影像作为诊断工具的效力。
更智能的两步助手
研究者将 StriaSeg‑iARM 设计为一个两阶段的深度学习系统,直接在个体的大脑空间内工作,而不是将扫描图像强行配准到标准模板。在第一阶段,程序在三维 MRI 中定位整体纹状体。在第二阶段,它将该结构在双侧脑部划分为 12 个解剖学定义的亚区。这两阶段之间的关键创新是一项交互步骤:专家可以快速检查并在必要时修正第一阶段产生的粗略轮廓,然后再运行更精细的细分。该方法融合了自动化的速度与受过训练的人类观察者的判断力。
在真实大脑中的训练与测试
为了教会系统识别目标,团队汇集了来自多家医院和不同扫描仪的数百例 MRI 扫描,并为 12 个纹状体亚区制作了精确的人工描绘。随后他们在两个外部数据集上测试了模型,这些数据集均包含 MRI 和多巴胺相关 PET 扫描:一组来自病程相对早期的帕金森患者与健康志愿者,另一组来自较年长、受影响更严重且脑萎缩明显、诊断混合的临床人群。在这些具有挑战性的病例中,StriaSeg‑iARM 在与人工专家描绘的匹配度上持续优于传统基于图谱的方法和更简单的一阶段深度学习模型,表现为更高的一致覆盖度、更精确的边界和稳定的体积测量。
为脑化学扫描带来更准确的测量
鉴于最终目标是量化 PET 信号,作者还考察了不同分割方法如何影响 PET 读数。使用每个亚区示踪剂结合度的标准度量,他们比较了自动结果与基于人工描绘的结果。图谱方法倾向于低估结合度,尤其在病变更严重的患者中;而基础的深度学习模型在某些区域仍表现出明显偏差。相比之下,级联模型——尤其在使用交互修正步骤时——产生的 PET 值与专家参考高度一致,偏差和离散度均极小。团队还表明,第一阶段的一个简单不确定性评分可以标记出大约四分之一最难处理的病例,这些病例确实需要专家修订,而其余病例可以保持全自动处理。
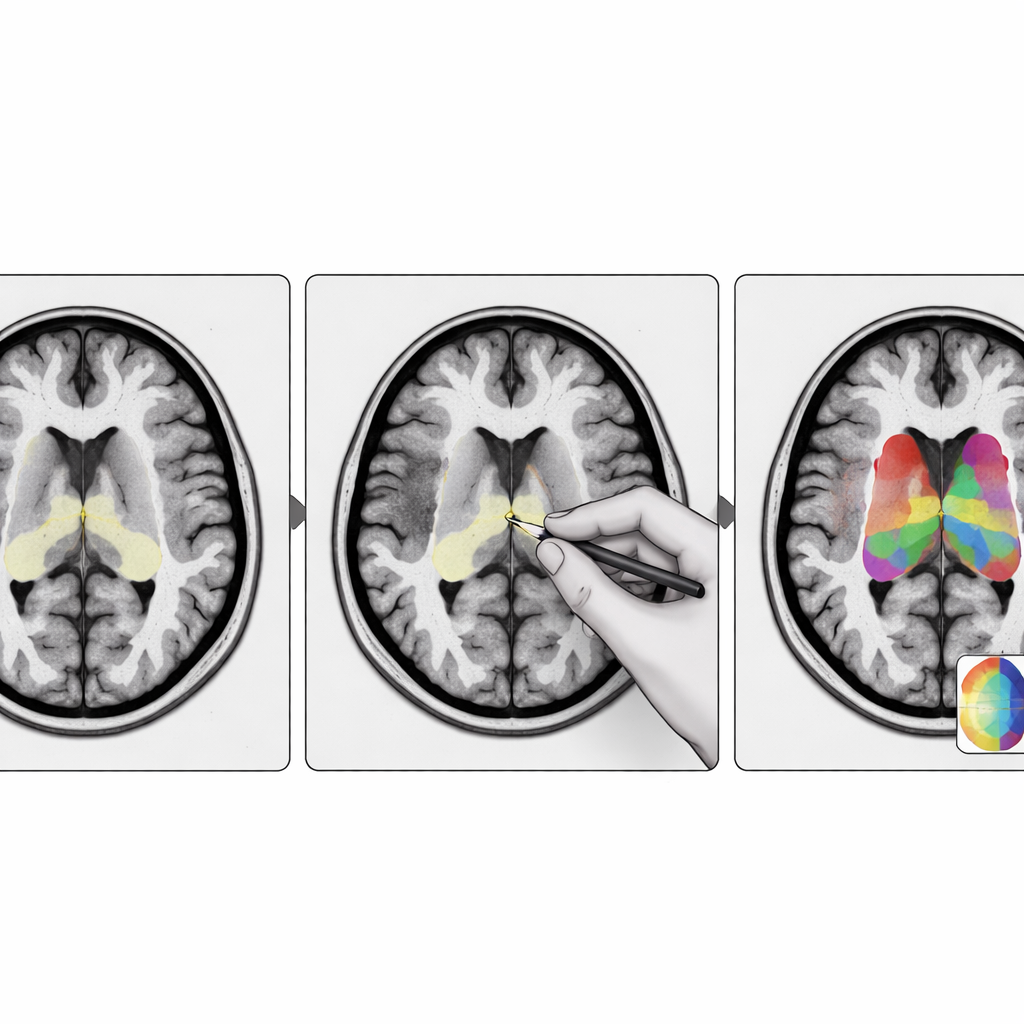
这对患者和临床医生意味着什么
对非专业人士来说,核心结论是更好的数字化小脑区地图可以提高化学脑扫描的可信度。StriaSeg‑iARM 提供了一个灵活的框架,深度学习模型完成大部分工作,但专家仍可在疑难病例中介入修正而无需重新训练系统。这种自动化与专家监督相结合的方法提高了用于诊断和追踪诸如帕金森病等疾病的测量精度,并可推广到其他器官和疾病,其中微小、难以观测的结构同样包含重要线索。
引用: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
关键词: 帕金森病影像学, 纹状体分割, 放射学中的深度学习, 脑部 PET MRI, 神经退行性生物标志物