Clear Sky Science · zh
产生两种细菌素——capidermicin 和 micrococcin P1 的 Staphylococcus capitis 菌株显示广谱抗菌活性
为何微小皮肤细菌对超级细菌威胁至关重要
抗生素耐药性感染在全球范围内不断增加,临床可用的可靠药物正在减少。一种有前景的思路是动员我们自身的“有益”微生物来对抗有害病原体。本研究关注一种常见的皮肤细菌 Staphylococcus capitis,并发现某一特定菌株(称为 HBC3)天然产生两种强效的杀菌分子。二者联合作用可抑制危险的医院病原体,包括耐甲氧西林金黄色葡萄球菌(MRSA),提示这些友好皮肤细菌本身可能成为未来对抗感染的工具。
一种寄居皮肤却暗藏火力的细菌
S. capitis 通常静静地存在于我们的皮肤上,尤其是头皮,通常无害。研究者对收集自人鼻腔的 18 个 S. capitis 菌株进行了筛查,以判断是否有能抑制 MRSA 的菌株。结果一株 HBC3 脱颖而出。在体外试验中,它强烈抑制了多种革兰氏阳性细菌,包括 MRSA、万古霉素耐药肠球菌(VRE)、化脓性链球菌、单核细胞增生李斯特菌(Listeria monocytogenes),以及可引起严重疾病的芽孢杆菌和梭状芽孢杆菌属。值得注意的是,它对几种常见革兰氏阴性细菌如大肠埃希菌和肺炎克雷伯氏菌没有明显作用,这提示其为针对性强但有力的抑制,而非无差别杀伤。 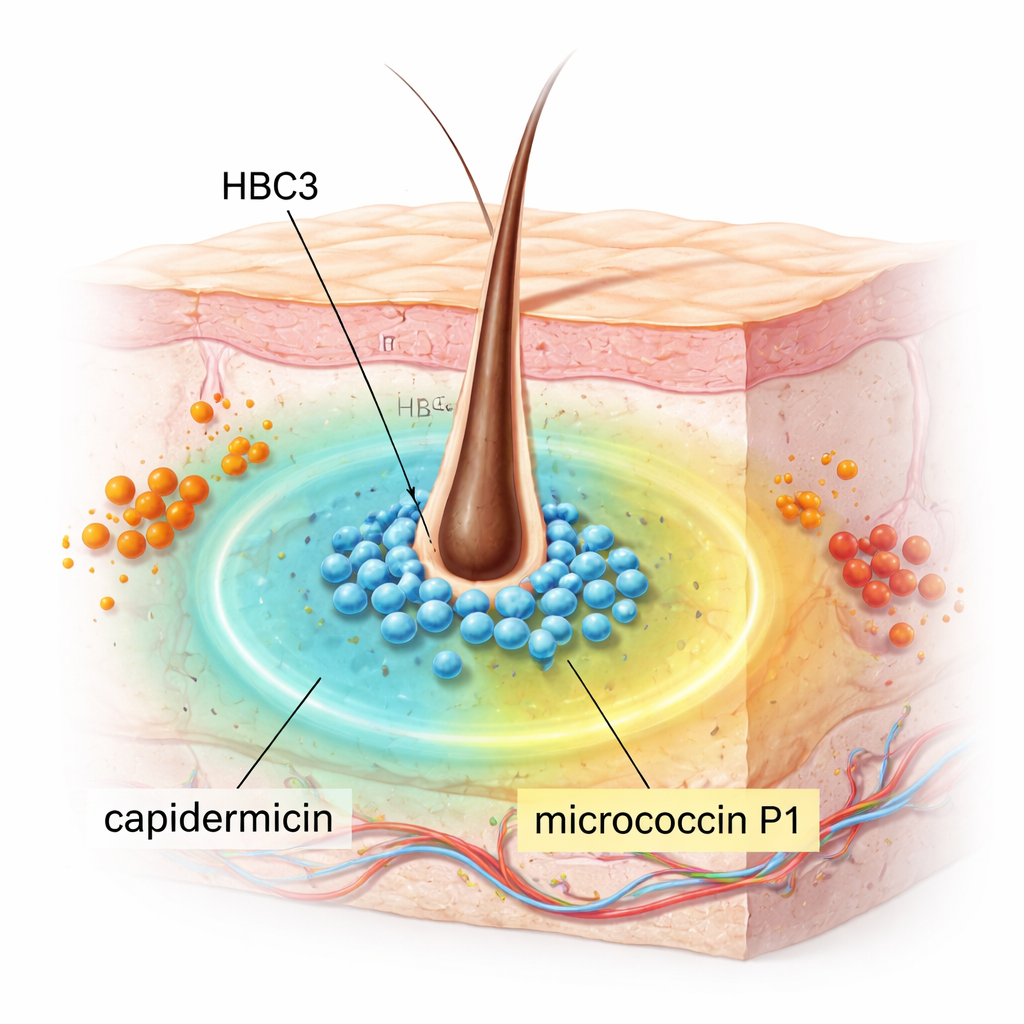
单一遗传“迷你染色体”携带两种天然抗生素
为弄清 HBC3 如何展现这种广谱抗菌能力,团队解读了其全基因组。他们发现了一个小型环状 DNA 元件,一个名为 pHBC3_1 的质粒,携带了合成两种不同细菌素的完整指令——细菌产生的类似抗生素的肽分子。其中一种是 capidermicin,一种带正电的小肽,曾在其他 S. capitis 菌株中被报道;另一种是 micrococcin P1(MP1),属于硫肽类,可阻断靶细菌的蛋白质合成,此前尚未在 S. capitis 中报道。当从 HBC3 中去除该质粒后,该菌株完全丧失了抗菌活性,证实这些基因对其防御能力至关重要。
不同靶向,共同目标
研究人员通过分别纯化每种细菌素,测试了它们抑制不同微生物的能力。MP1 在低浓度下对许多革兰氏阳性球菌(包括 MRSA 和肠球菌)表现出广泛且强烈的活性。相比之下,capidermicin 更擅长针对杆状革兰氏阳性细菌,如凝固芽孢杆菌和李斯特菌,但在本研究使用的条件下对葡萄球菌效果较弱或无效。当团队将两种肽联合用于对抗凝固芽孢杆菌时,观察到加和效应:合用时更低的剂量即可比单独使用任一肽获得更强的生长抑制。这种互补性靶向意味着 HBC3 通过部署两种针对不同细菌形态和细胞表面的分子武器,能够抑制更广泛的竞争对手。 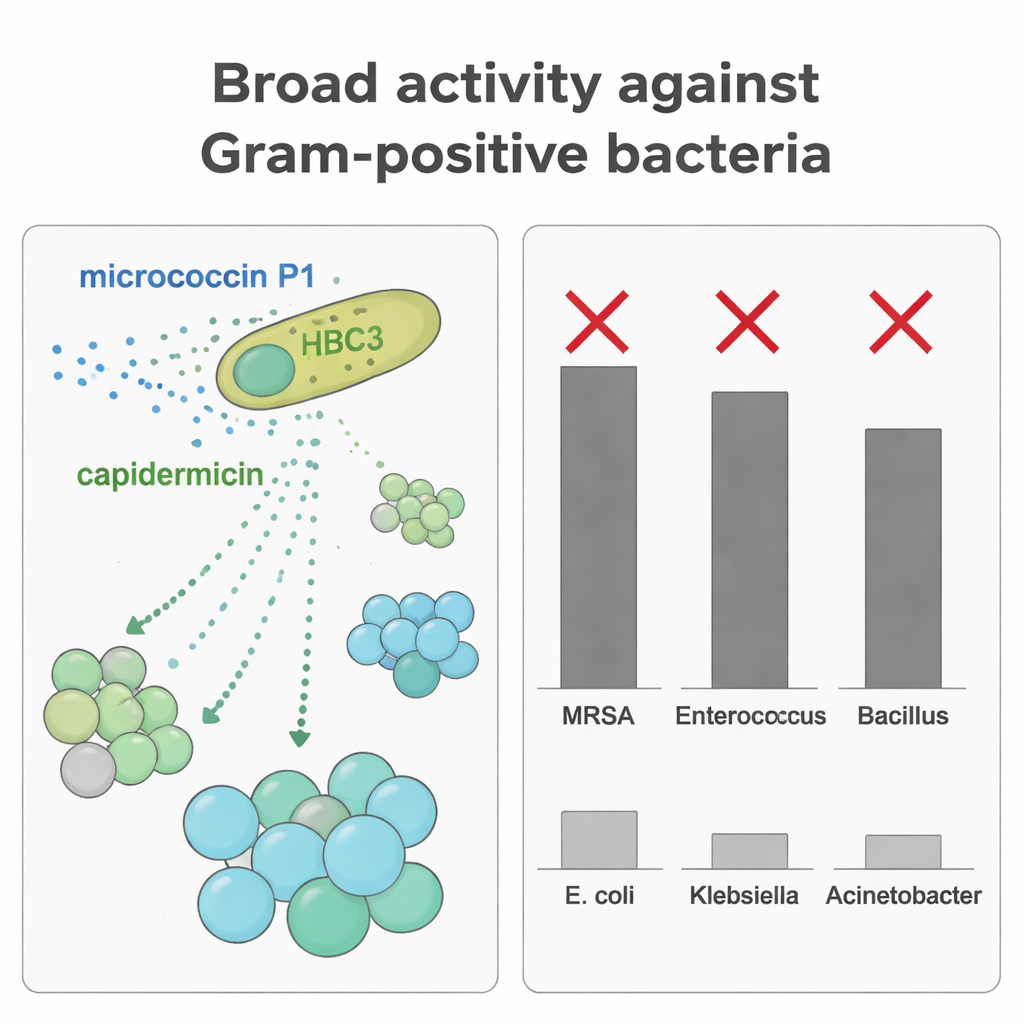
在拥挤的微生物群落中赢得生存空间
为模拟真实竞争情形,研究者将 HBC3 与 MRSA、VRE 和凝固芽孢杆菌在同一平板上共培养。携带正常质粒的 HBC3 几乎完全消除了混合群落中的这些病原体,而缺失该质粒的变体则允许它们繁荣生长。基因比较显示,这个双细菌素质粒很可能源自过去对不同质粒的融合与重排,并受可移动 DNA 元件的帮助,这些元素能在细菌间移动基因簇。这一复合质粒赋予 HBC3 在皮肤或黏膜等微生物竞争激烈的环境中明显优势,在这些场所众多微生物为营养与生存空间竞争。
从皮肤盟友到未来益生菌?
研究得出结论,S. capitis HBC3 在一份罕见的质粒上携带两种不同的细菌素组合,使其能够强烈抑制多种临床重要的革兰氏阳性病原体,包括抗药性菌株。因为 HBC3 本身不属于已知的高风险谱系,且未检测到携带耐药基因,它可能成为开发靶向益生菌或去定植(decolonization)制剂的候选者——例如被设计用于选择性降低皮肤或鼻腔中的 S. aureus,同时保留更为无害的共居菌。在实现此类应用之前,还需对安全性、在动物与人体内的有效性及对正常微生物组的长期影响进行细致评估,但该工作强调了我们的微生物如何可能帮助应对持续的超级细菌危机。
引用: Ohdan, K., Suzuki, Y., Kawada-Matsuo, M. et al. Staphylococcus capitis strain producing dual bacteriocins, capidermicin and micrococcin P1, shows broad-spectrum antimicrobial activity. Sci Rep 16, 6835 (2026). https://doi.org/10.1038/s41598-026-36393-6
关键词: 细菌素, Staphylococcus capitis, micrococcin P1, capidermicin, 抗生素耐药性