Clear Sky Science · zh
双1,2,4-三唑衍生物作为治疗肺炎的潜在抗氧化剂
为何保护肺部免受“生锈”侵蚀很重要
人们常把肺炎简单地看作一种可用抗生素治愈的严重肺部感染。但许多重症肺炎患者死亡的原因并不仅仅是病原体本身,而是机体的过度反应。当免疫细胞与侵入的细菌或病毒作战时,会释放出高度活泼的分子——像化学“火花”一样,这些分子会损伤肺组织,犹如铁锈侵蚀金属。该研究探索了一类实验室合成的新分子,称为双1,2,4-三唑,旨在既作为强效抗氧化剂,又能阻断细菌的致病武器。目标是开发可与抗生素配合使用的附加药物,在抗感染的同时保护肺组织。
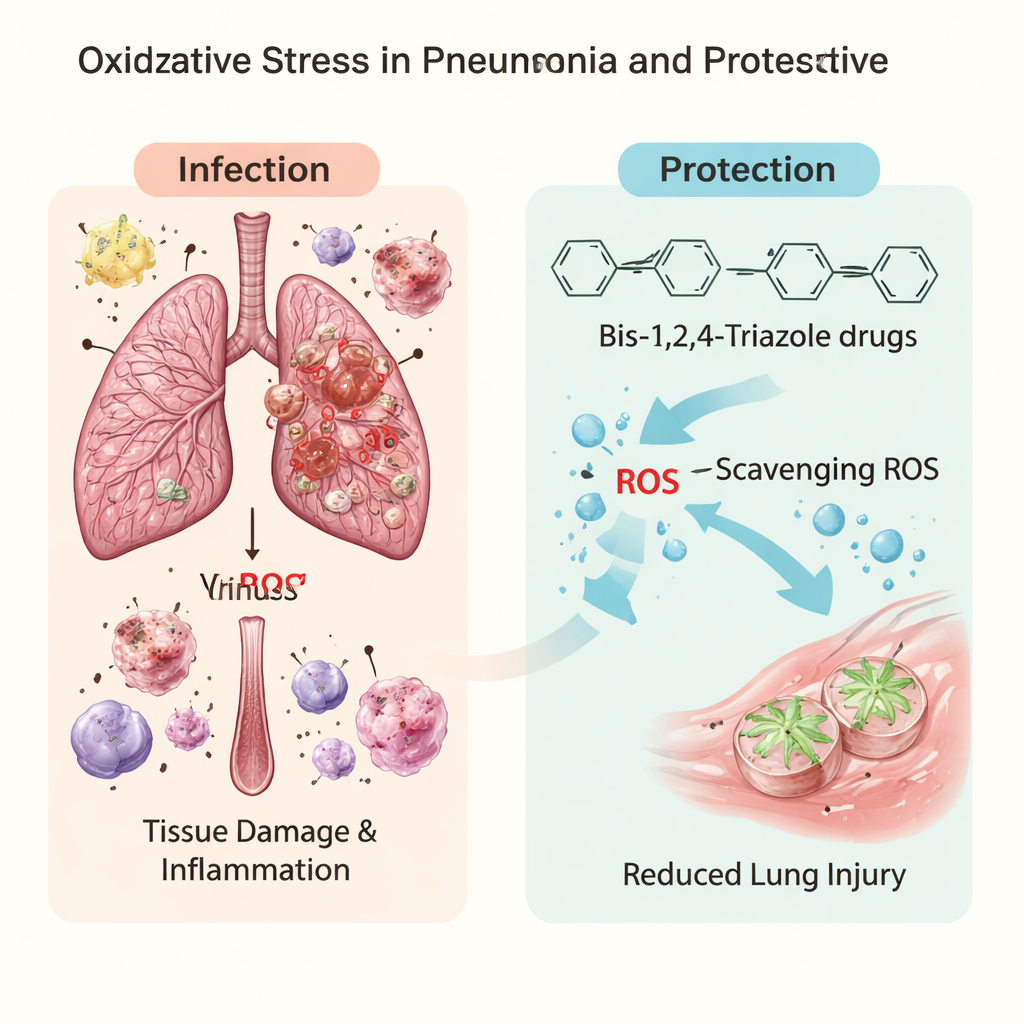
肺部感染期间的隐性损伤
当微生物侵入肺部时,免疫细胞会释放一阵阵活性氧和活性氮物种(统称ROS/RNS)。在少量时这些物质有助于杀灭病原体;但过量时会攻击机体自身的脂质、蛋白质和DNA。近期临床研究显示,重症肺炎患者(包括COVID-19肺炎)常有明显的氧化应激和氧化还原失衡的标志。这种化学性超负荷削弱了肺部脆弱的气囊,加剧失控的炎症,并促成急性呼吸窘迫综合征。这促使研究者思考:是否可以用有针对性的抗氧化剂充当火线隔离带——在这些活性分子烧穿肺组织之前将其清除。
设计用于保护肺部的新小分子
研究团队将注意力集中在一种称为1,2,4-三唑的环状化学结构上,这类结构已常见于多种药物中。研究者不是使用单一环,而是把两个环连接起来形成双1,2,4-三唑,这种结构能与细胞亲水和亲脂部分以及金属离子相互作用。此前已有六种此类化合物被合成,并显示出抗微生物活性以及抑制与炎症和癌症相关酶的能力。在本项工作中,作者考察了通过调整例如碳链长度或在连接环上引入硝基等特征,是否能使这些分子在中和ROS并干预与肺炎相关的细菌毒力因子方面表现优异。
在实验室测试抗氧化能力
为评估这六种分子清除自由基的能力,研究者使用了一种标准的显色测试,采用一种稳定自由基DPPH。抗氧化剂清除该自由基时,溶液会由紫色褪为黄色,褪色程度可被精确测量。所有六种双三唑均显示出剂量依赖的清除自由基活性,但其中两种表现突出:一种带有柔性六碳(己基)链,另一种带有对位硝基苯基环,它们的表现最接近经典抗氧化剂维生素C。这两种化合物达到与维生素C相同50%清除率时,大约需要维生素C两倍的浓度,但仍足够强,值得作为有前景的药物候选。它们的结构似乎有助于嵌入肺部富脂膜并稳定所捕获的自由基。
抑制细菌“武器”同时保持类药物特性
除了抗氧化活性外,研究团队还用计算模拟评估这些新分子是否能干扰肺炎链球菌的两种关键蛋白:NanA(帮助细菌附着并侵入组织)和肺炎溶血素Ply(一种在细胞膜上打孔的毒素)。在计算机模拟中,表现最好的硝基苯基化合物结合最紧密,在蛋白活性口袋内形成多个氢键和堆积相互作用。虽然不如某些笨重的天然多酚那样粘附,但这些双三唑表明其紧凑的骨架能够占据NanA和Ply的易损区域。对吸收、代谢和毒性的并行计算模型预测,所有六种化合物,尤其是两种领衔分子,具有较高的肠道吸收预测值、低毒性、不易显著干扰常见药物代谢酶且不易影响心律通道——这些都是“类药物”特征的关键要素。
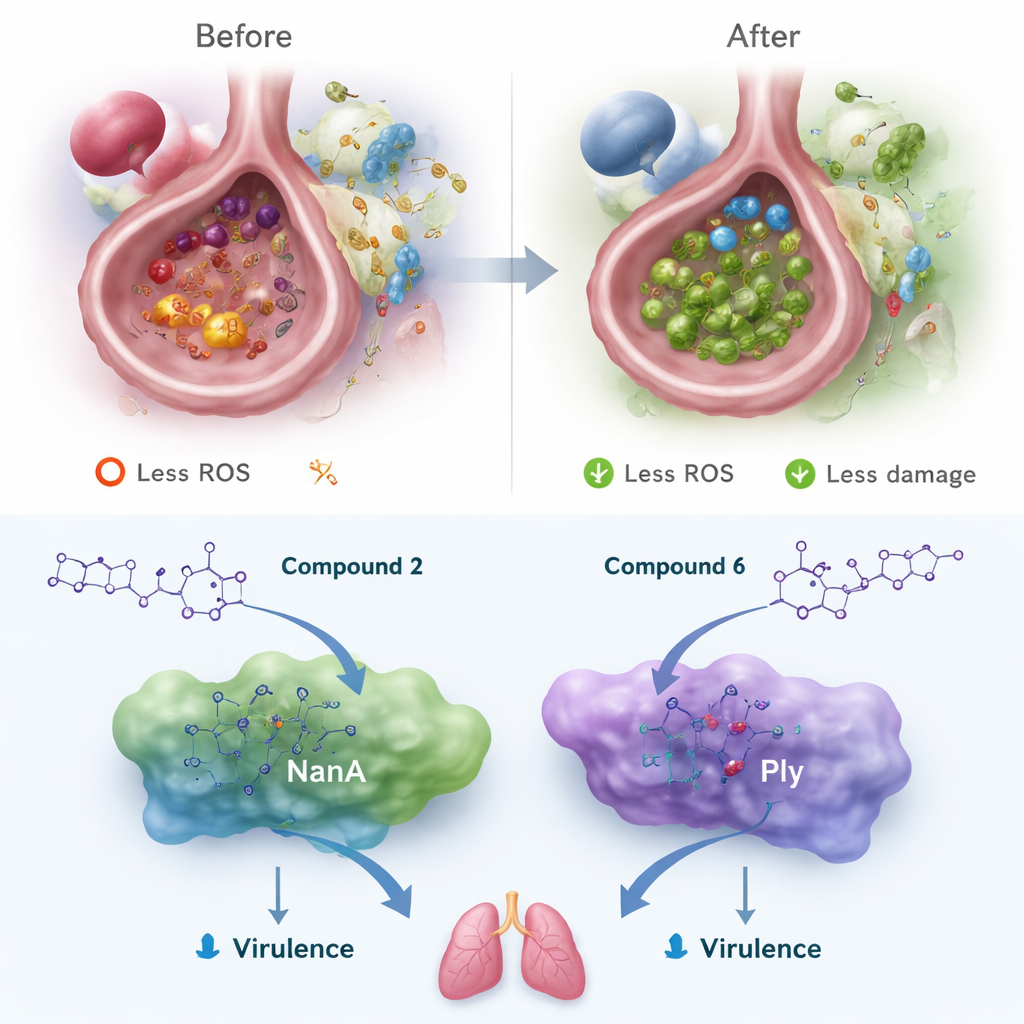
这对未来肺炎治疗可能意味着什么
综合来看,结果表明双1,2,4-三唑——尤其是两种表现最好的分子——可作为肺炎治疗中双重作用助剂的早期原型。原则上,此类化合物既能清除侵蚀肺组织的有害活性分子,又能削弱加重疾病的细菌工具,同时具备口服安全性并在体内大多不进入脑组织。该工作仍处于临床前阶段:这些化合物接下来必须在人体肺细胞和动物肺炎模型中进行安全性测试,其结构也可能需要改造以提高效力和溶解度。但该研究向非专业读者传达了一个明确信息:未来的肺炎治疗可能不再仅依赖抗生素,也可能包括保护肺部免受自身免疫反应附带损伤的小分子药物。
引用: Korol, N., Symkanych, O., Pallah, O. et al. Bis-1,2,4-triazole derivatives as potential antioxidants for pneumonia therapy. Sci Rep 16, 5640 (2026). https://doi.org/10.1038/s41598-026-36386-5
关键词: 肺炎, 氧化应激, 抗氧化剂, 细菌毒力, 药物设计