Clear Sky Science · zh
部署高通量虚拟筛选(HTVS)方法以识别具有抗癌潜能的新型乳酸脱氢酶(LDH)抑制剂
这项研究对癌症治疗的重要性
癌细胞常常重塑其能量代谢途径,这一转变可被利用来设计更智能、更具选择性的药物。本研究探讨了一种关键代谢酶——乳酸脱氢酶(LDH),它帮助肿瘤在恶劣环境中生存并抵抗治疗。研究人员结合先进的计算筛选和实验室验证,鉴定出两种新的小分子能够抑制LDH,并在前列腺癌细胞系中显示出有希望的抗癌效应。
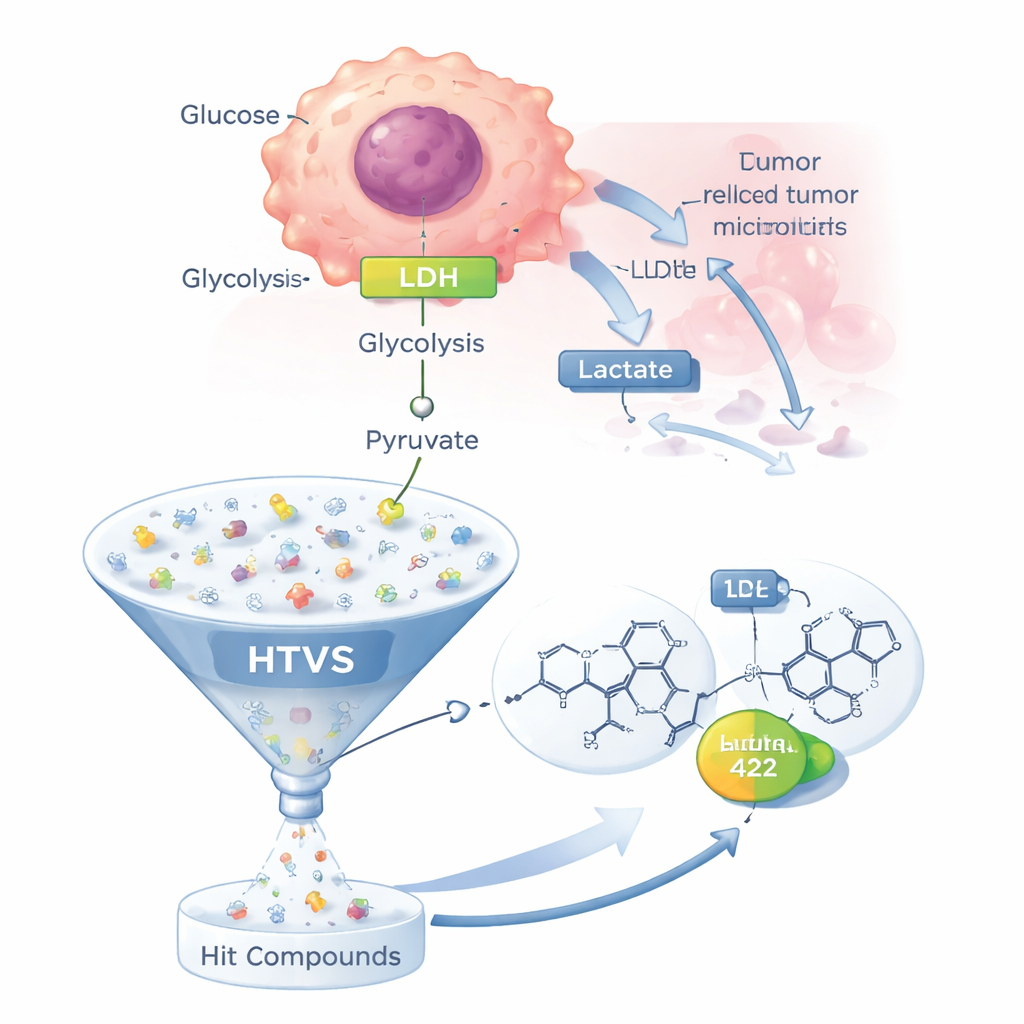
癌细胞的异常代谢
大多数健康细胞在粒线体中高效利用氧气来产生能量。然而,许多癌细胞即便在氧气充足的情况下,也高度依赖一种效率较低的途径——糖酵解,这一现象被称为沃伯格效应。在这一路径中,葡萄糖被分解为丙酮酸,随后由LDH将其转化为乳酸,而不是进入粒线体。乳酸被泵出细胞,使肿瘤微环境酸化,帮助癌细胞逃避细胞死亡、削弱免疫攻击,甚至减弱许多化疗药物的疗效。由于LDH位于这种改变代谢的核心,且尚无针对LDH的获批药物,它已成为开发新型抗癌疗法的高优先级靶点。
用计算方法筛选近五十万分子
研究团队没有在实验室中逐一测试潜在候选物,而是采用了高通量虚拟筛选(HTVS)策略。他们从文献中收集了28种已报道的LDH抑制分子,并从中提取出一个“药效团”——一种抽象的三维特征模式,任何有效的LDH抑制剂很可能具有这些特征。接着,他们将该模型应用于一个约50万种类药物相似分子的商业数据库,筛选出与这些关键特征匹配的候选物。大约11万种分子通过了第一轮过滤,随后基于常用的“类药性”规则进一步筛选,将候选名单缩减到2337个更现实的分子以用于与LDH酶的分子对接。
聚焦最佳结合者
下一步是估算这些候选分子与LDH活性位点的结合紧密度。通过多个层级的计算对接,研究人员预测每个分子如何与酶口袋内的特定氨基酸相互作用。这个多阶段流程逐步将数千个候选者缩减为59个有前景的分子,随后再精简到5个结合预测尤其强的“命中”分子。其中两种,标记为化合物15和422,尤为突出:基于分子动力学模拟的计算结果表明,它们随时间能与LDH形成异常稳定的复合物,维持与活性位点关键残基的接触,同时保持蛋白质整体结构的合理性。
从筛选走向真实癌细胞
为评估这些命中分子在生物系统中的效应,科学家购买了化合物15和422并在前列腺癌细胞系DU-145和PC-3中进行了测试。两种分子在细胞内以纳摩尔浓度抑制LDH活性,并且也直接减缓了纯化LDH酶的活性,尽管其效力略逊于已知的实验性抑制剂GNE‑140。在细胞生长测定中,这些化合物在低微摩尔剂量下降低了癌细胞存活率,效果接近GNE‑140。更多实验显示,处理稍微增加了氧化应激,扰乱了线粒体膜电位——这是能量工厂受损的标志,并在DU‑145细胞中诱导了程序性细胞死亡(凋亡),其中化合物15的活性更强。
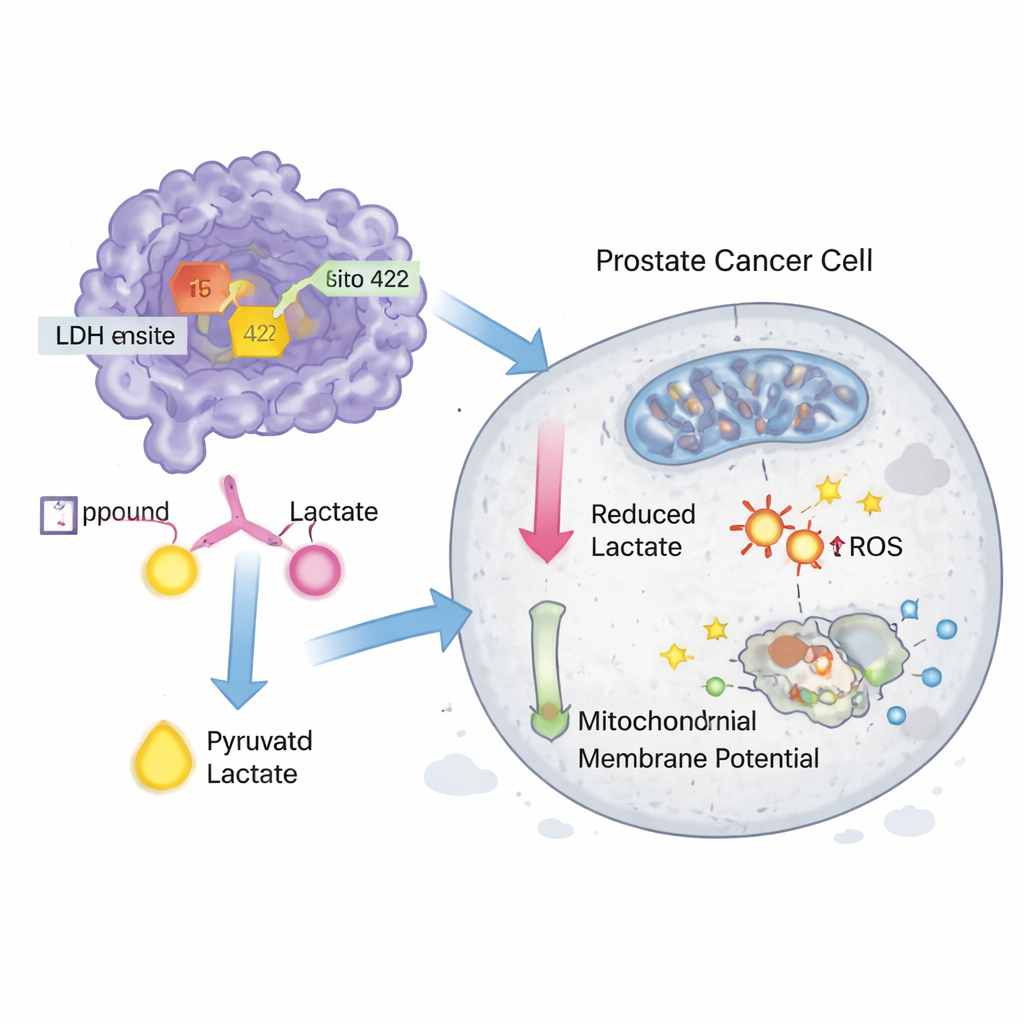
这对未来抗癌药意味着什么
虽然这些分子尚非即刻可用的药物,但它们为药物设计提供了有价值的起点。化合物15和422的化学性质表明,它们在溶解度、渗透性及整体“类药性”方面可能优于一些现有的LDH抑制剂,使其成为进一步优化的有吸引力先导化合物。该研究展示了如何以已知结构特征为指导,通过大规模计算筛选发现能够削弱癌细胞、切断其异常能量供应的新型LDH抑制剂。通过后续对其结构的精细改造、更严格的直接结合测定及动物体内研究,这些化合物有望发展为通过靶向肿瘤独特代谢脆弱性来攻击肿瘤的新型抗癌药物。
引用: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
关键词: 乳酸脱氢酶抑制剂, 癌症代谢, 虚拟筛选, 前列腺癌, 抗癌药物发现